第一节 神经元和神经胶质细胞
神经系统由中枢神经系统(central nervous system)和周围神经系统( peripheral nervous system)两部分组成,前者是指脑和脊髓部分,除含有大量完整的神经元和神经胶质细胞外,还包括传出神经元的胞体部分。周围神经系统主要包括由传出神经元的长突起所组成的神经干、周围神经节和散在分布于全身各组织器官内的神经丛和神经末梢。神经系统的细胞主要包括神经细胞(neurocyte)和神经胶质细胞,神经胶质细胞与细胞间液共同构成神经元生存的内环境。
一、神经元及其一般生理功能
神经元由细胞体(soma)、树突(dentrites)、轴突(axon)和轴突末梢(axonal terminals)组成。典型的神经元具有四个功能区,分别为信号输入区、触发信号区、传导信号部位和输出信号区。信号输入区主要位于树突和胞体,它们分布有大量的突触,是接受传入信息的输入部位,该区可以产生突触后电位(局部电位),是神经系统形成网络样结构的重要基础。整合区或信号触发区位于轴突始段,众多的突触后电位在此发生总和,当达到阈电位时在此首先产生动作电位。信号传导区位于轴突,动作电位以“全或无”的方式不衰减的传向所支配的效应器。无髓鞘神经纤维或郎飞结处的电压门控性Na+通道,是传导动作电位的结构基础,不同信息在同一个神经细胞内的传导过程是借助膜电位变化进行编码的。轴突末梢的突触小体则是信息输出区,信息传递主要通过胞吐方式释放不同种类的神经递质实现。有些神经元除能传递信息外,还能分泌激素,将神经电信号变为体液信号。
(一)神经元胞体的结构与功能
神经系统的灰质主要由神经细胞组成,但也有一些树突和轴突。而神经系统的白质则完全由神经轴索组成。神经元的胞体有锥体形、卵圆形、纺锤形和星形等多种形状,它是神经元的代谢和营养中心,也是反射的中枢部位。胞体的结构与一般细胞相似,有细胞膜、核仁、细胞质和细胞核。
1.神经细胞膜的结构和功能 神经细胞体和突起表面的膜,呈连续完整的细胞膜,是神经细胞的重要组成部分,除突触部位的胞膜有特殊的结构外,它与所有细胞膜一样,属液态镶嵌模型的单位膜结构。具有高度分化的分子构成和多种独特的生理功能。神经元对信息的识别和结合、跨膜物质转运、能量转换、神经冲动的产生与传导以及跨膜信息传递等生理功能均与细胞膜的特殊结构有关。
神经细胞膜的主要成分是脂质(40%~50%)、蛋白质(30%~40%)和糖(1%~5%)。通常膜的功能越复杂,蛋白质所占比例越大,不同种类的膜蛋白主要构成膜上的受体(receptor)和离子通道(ionic chanel)。神经细胞膜的脂质中,含唾液酸的酸性鞘糖脂,因其最早发现于神经节细胞而得名为神经节苷脂,在神经组织中含量最高,是神经细胞膜的组成部分;根据分子结构中的唾液酸不同,神经节苷脂可分为单唾液酸、双唾液酸、三唾液酸、四唾液酸神经节苷脂(GM、GD、GT、GQ)等。神经节苷脂具有识别细胞间活性物质的作用。例如GM1分子中的半乳糖是霍乱毒素结合的部位。GD16和GT1有破伤风毒素β亚基结合的位点,破伤风毒素与之结合后,可抑制其神经末梢释放抑制性递质(甘氨酸),对脊髓前角α运动神经元抑制性作用减弱,导致骨骼肌的阵发性痉挛。随着人们对神经节苷脂研究的不断深入,它在医药及保健食品工业的应用研究已经取得了很大进展。目前已分离出多种神经节苷脂,用于治疗神经病变。
2.细胞质与细胞核
(1)细胞质 细胞核以外的胞质(核周质)呈胶体状,细胞核以外的胞体部分称为核周体(perikaryon)。细胞质中的高尔基器、线粒体、溶酶体、核糖体等细胞器的功能与其他组织细胞的相同。所不同的是神经元胞浆中尚含有内涵物,包括一些致密小体和色素颗粒如脂褐素。内涵物出现于成年期,随年龄增长而增加。它还含有丰富的细胞骨架维持着细胞形态,细胞骨架分别由微丝(microfilament)、微管(microtuble)、中间丝(神经细丝,neurofilament)等丝状结构组成。
1)尼氏小体:在光学显微镜下可见大量被碱性染料染色的尼氏小体(Nissl's bodies),它由许多平行排列并互相联系的粗面内质网和游离核糖体(free ribosome)组成。尼氏小体是神经元合成蛋白质最活跃的部位,仅存在于胞体和大树突干中,不存在于轴丘及轴突中。尼氏小体处合成的蛋白质经细胞内部的运输系统运送到轴丘及轴突,用以补充神经元正常生理活动中不断消耗的蛋白。
脊髓前角大的运动神经元中尼氏小体较大,呈斑块状;而在小的神经元如小脑蒲肯野细胞的尼氏小体多呈细小颗粒状,分布均匀。正常状态下,不同部位的尼氏小体一般都有各自固定的形态,当神经元受到损害或轴突被切断时,尼氏小体解体,以至溶解消失,称为染色质溶解(chromatolysis),可作为神经元受损的标志。
2)高尔基器:神经元的高尔基器发达,位于核周质中部,并伸入树突的分支内,它参与多肽类激素、肽类递质或其他神经分泌颗粒合成过程。最初合成的肽链没有活性,经过高尔基器的内切酶裂解、加工及修饰,达到一定的氨基酸数量及序列时,即形成具有生物活性的肽链。当神经元轴突断裂时,高尔基器分散在细胞周边,随后断裂消失,这种现象称为高尔基网溶解。
3)线粒体:神经元内的线粒体多呈细长的棒状,分布于胞体、树突及轴突,在尼氏小体区域和轴突末梢聚集较多;它是神经元氧化磷酸化产生能量的中心,其数量多少代表代谢旺盛的程度。线粒体的内膜上有电子传递系统及氧化磷酸化系统。基质内含有琥珀酸脱氢酶、三羧酸循环酶系、氧化酶系等。
阿尔茨海默病患者在出现神经元丢失、认知功能明显减退等临床病理症状之前,海马和大脑顶颞叶皮层的糖代谢已出现异常,氧化磷酸化系统遭到破坏[1]。因此认为线粒体损伤是AD潜在的发病原因之一。AD线粒体损伤最主要表现为电子传递链(ETC)的损伤,而ETC损伤主要是电子传递酶—细胞色素C氧化酶(cytochrome C oxidase,COX)的缺陷,该缺陷在受神经纤维缠结影响的神经元中表现尤为突出。
4)神经微管和神经细丝:在Cajal法染色的切片上,可观察到神经细胞体和突起的胞质内存在着直径2~3μm的银染丝状纤维结构,称为神经原纤维(neurofibrils)。电镜下,可见神经原纤维由微管和神经丝组成,这些结构在核周体内交织成网,分别向树突和轴突延伸,在突起中平行排列,可达到突起的末梢部位。神经原纤维是形成神经元的细胞骨架,起到维持神经元形态和物质转运的作用,并对细胞的运动和分裂发挥重要作用。
神经微管长度变化很大,最长可达数米,它是一种外径约25 nm、内径约15 nm的中空管状结构,其主要成分是微管蛋白(tubulin),由α-和β-微管蛋白聚合而成。微管与轴浆内的快速运输有关,并起支持作用。因此神经元各部分的营养和功能的发挥有赖于微管物质运输作用。轴浆流的方向主要是由胞体走向末梢(顺向),也有逆行的(逆向),而双向运输的成分并不相同(图4-1-1)。快速顺向轴浆运输的主要物质是有膜结构的细胞器,如线粒体、递质囊泡和分泌颗粒等。快速逆向运输的速度比顺向运输慢,它主要运输可被轴突、末梢摄取的物质。
实验中常用秋水仙碱阻断囊泡的轴浆运输,使免疫组织化学显示胞体中含有递质的种类,因此它是最重要的微管工具药物。破伤风毒素及辣根过氧化物酶等可逆向运输到胞体,后者被用来跟踪末梢的神经元起源。
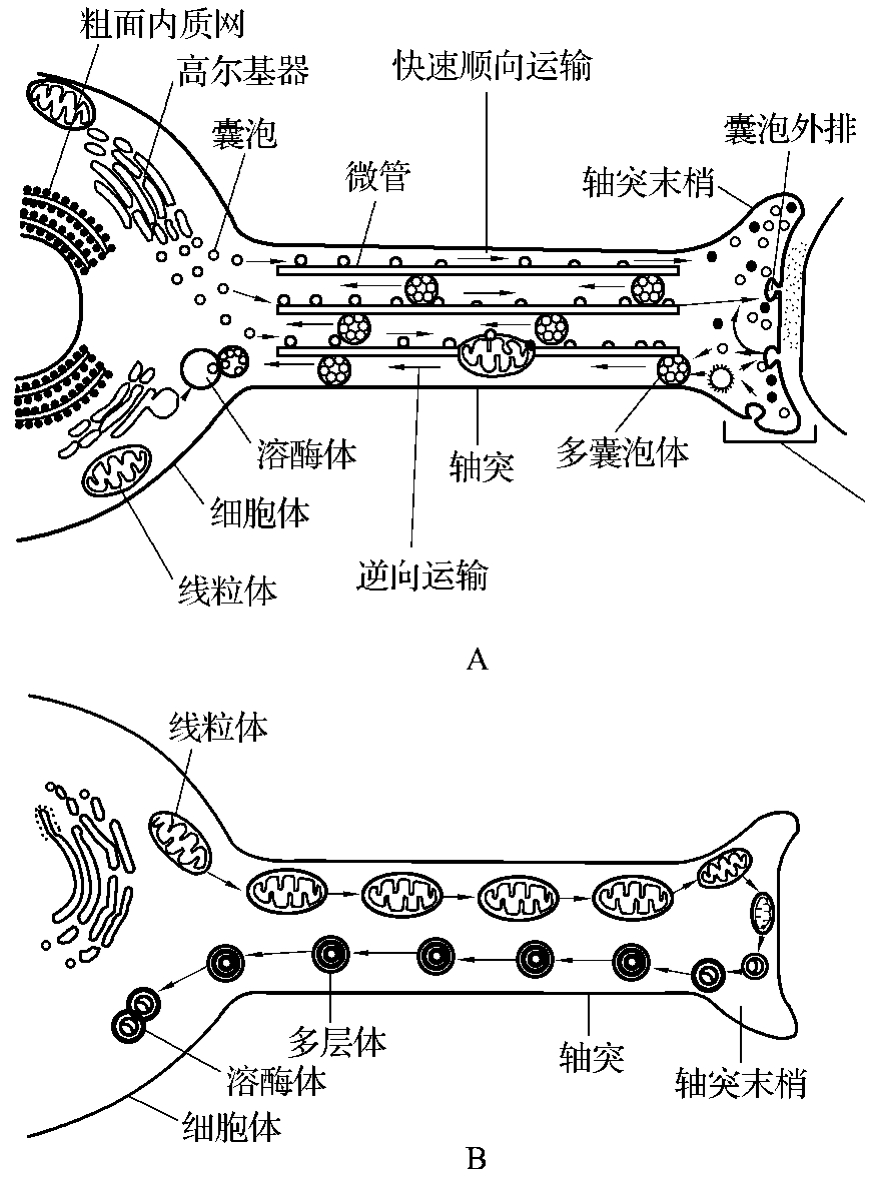
图4-1-1 快速运输示意图。A.快速顺向轴浆运输; B.快速逆向运输的模式图
顺向轴浆运输的机制是微管提供了轨道,被运输的细胞器通过一种类似于肌凝蛋白的驱动蛋白(kinesin)在轨道上移动而进行运输的。其运输过程是位于微管上的一种微管结合蛋白(microtubule-binding protein)与驱动蛋白经局部耗能后相互作用的结果。驱动蛋白具有一个杆部和两个球头部。杆部尾端的轻链可连接于被运输的细胞器,头部构成横桥(cross-brid),具有两个功能:一是具有ATP酶活性,二是具有与微管上的微管结合蛋白可逆结合的位点。当一个横桥与微管结合蛋白结合时,ATP酶被激活,横桥分解ATP而获能,促使驱动蛋白的颈部发生扭动,于是另一个横桥即与微管上的下一个位点结合,如此不停地交替进行,细胞器便沿着微管(轨道)输送到轴突末梢(图4-1-2A)。逆向轴浆运输是通过胞质动力蛋白将神经营养因子等物质从轴突末梢向胞体方向进行运输(图4-1-2B)。
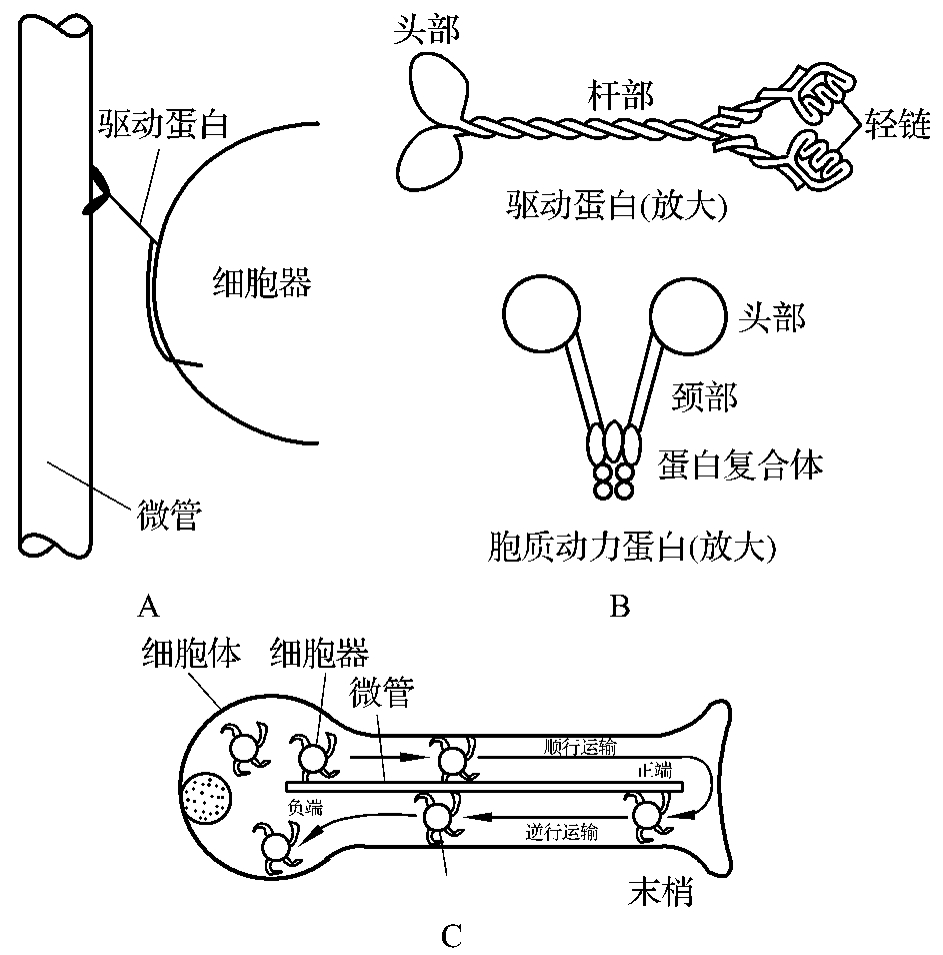
图4-1-2 微管运输细胞器的示意图及两种动力分子的模式图。A.驱动蛋白沿微管运输细胞器;B.驱动蛋白和胞质动力蛋白分子的模式图;C.微管运输细胞器的示意图
神经元中还有一种微管相关蛋白质(microtubule-associated protein,MAP),其功能是促进微管装配,并与微管定位有关。在神经轴突中含有低分子量的MAP,称为tau蛋白(tau protein),在神经轴突和树突内含有高分子量的MAP,包括MAP1、MAP2和MAP4。
tau蛋白的生物学功能是诱导与促进加速微管蛋白的聚合而形成微管表面的束状细丝,称为旁臂,按其间距(4~48 nm)规则排列,横向连接相邻微管以稳定微管作用,防止解聚,维持其结构的稳定性。tau蛋白是一种含磷蛋白质,约每分子tau蛋白修饰有2~3分子的磷酸基团,tau蛋白磷酸化和去磷酸化之间的平衡调节着细胞骨架稳定性,影响轴突形态。tau蛋白与各种磷酸酶和激酶的结合不仅可以调节自身磷酸化,也可以使这些磷酸转移酶定位到细胞内对应底物,调节其他蛋白的磷酸化状态。tau蛋白只有一级结构,最突出的特点是含有352~441个氨基酸残基,在蛋白质羧基端具有3~4个氨基酸残基的重复区,这些重复区参与构成tau蛋白的微管结合区,它不具备二级结构(如α螺旋或β片层结构)[2]。但在AD患者,由于神经细胞内不同蛋白激酶和磷酸化酶系统对tau蛋白的超磷酸化作用,引发tau蛋白的结构和构型改变,使每分子tau蛋白连接有9~10个磷酸基团[3]。这种过度的磷酸化使tau蛋白失去了其生物学功能,易从微管上解离下来聚集成双螺旋丝(paired helical filament PHF)结构,它是形成神经原纤维缠结(neurofibrillary tangle,NFT)的主要组成纤维,也是AD的主要神经病理学特征之一。tau蛋白的超磷酸化进而影响它与微管蛋白结合和微管聚集能力,使微管结构崩解,阻断细胞核与轴突之间的蛋白运输通路,使细胞调节与合成蛋白的功能降低,发生神经元退变,诱发AD的某些症状。有研究证实,AD患者脑脊液tau蛋白含量显著高于正常人[4]。海马处的神经元纤维缠结与AD患者的认知与记忆障碍密切相关。
在神经轴突和树突内的MAP1在微管间形成驱动蛋白的横桥,但并不使微管成束。仅存在于树突中的MAP2与依赖于cAMP的蛋白激酶有高度亲和性,在微管间形成横桥,能使微管成束。微管是细胞的重要骨架蛋白,对维持细胞结构,细胞内蛋白质运输(如轴浆转运)至关重要,因此,细胞骨架损害常常干扰轴浆运输,而导致许多重要的神经疾病,如老年性痴呆、下肢痉挛性截瘫等。
微丝(microfilament)是最细的丝状结构,直径约5 nm,长短不等,集聚成束状分布,交织成网,广泛的分布在神经元的胞质和突起内,在有髓鞘的轴突中含量较多。其主要功能具有收缩作用,适应神经元生理活动的形态改变。
(2)细胞核 神经元的细胞核位于胞体中央,但有个别神经元的胞核位于胞质的某一侧,显得特别大,核膜明显。电镜下,核染色浅淡,核中的染色体分布稀疏,核蛋白稀少,这是因为大多数神经细胞不再进行分裂活动。通常核的中央有一个大而圆的核仁,有时可见2~3个核仁。核仁由低致密度并密集排列的细丝和颗粒构成,细丝与颗粒上存有核糖和核蛋白,故核中大部分核糖核酸位于核仁内,因而神经细胞核仁较大,说明神经细胞蛋白质合成功能活跃。由于神经细胞不能再进行分裂再生,它在一生中必须不断地合成蛋白质,以补充它们的损耗。
(二)神经元的轴突与树突
1.轴突 典型的神经元轴突分支少,但较长(图4-1-3)。胞体发出轴突的部位常呈圆锥形,称为轴丘(axon hillock),电镜下轴丘内几乎没有游离的核糖体和粗面内质网。在轴突的起始部无髓鞘包裹的部位称为始段(initial segment),该段膜的电压门控钠通道密度较大,诱发动作电位的阈值最低,因此是神经元产生动作电位的起始部位。每一个神经细胞有一个从轴丘发出的轴索,用银浸润法,可看到神经原纤维贯穿整个轴索。轴索由胞体发出后,直径较恒定,不因距胞体远近而变化。轴突离开细胞体一段距离后才获得髓鞘,成为神经纤维,神经纤维由神经元的长轴突外包胶质细胞组成。髓鞘具有保护神经元并使神经冲动在轴突上快速传导的作用。包裹中枢神经纤维轴突的胶质细胞是由少突胶质细胞突起末端的足板包卷轴突而形成。一个少突胶质细胞有多个突起可分别包卷多个轴突,其胞体位于神经纤维之间。中枢神经系统内的有髓鞘轴突的外表面没有基膜。施旺细胞(Schwann cell)是周围神经纤维的鞘细胞,其长轴与轴突平行,包裹着周围神经纤维的轴突,形成髓鞘。由于施旺细胞包在轴突的外面,故又称神经膜细胞(neurilemmal cell),它的外面包有一层基膜,在周围神经再生中起重要作用。施旺细胞及其外面的一层基膜统称神经膜(neurilemma)。在神经纤维上髓鞘分成许多节段,各节段间的无髓鞘缩窄部称郎飞结(Ranvier node),轴突的侧支均自郎飞结处发出。相邻两个郎飞结之间的一段神经纤维称结间体(internode)。轴突越粗,其髓鞘也越厚,结间体也越长。有髓神经纤维轴膜的动作电位在相邻的郎飞结间呈跳跃式传导,结间体越长,跳跃的距离也越大,传导速度也就越快。神经轴索与髓鞘有极密切关系,所以致病因子常易造成二者的共同损害。髓鞘的损害常较轴索为重,如多发性硬化及多发性周围神经炎等。当轴索损害时则髓鞘很难幸免,如内囊受损后脊髓内的皮质脊髓束即出现脱髓鞘现象。这些都说明髓鞘较轴索更易受损。髓鞘完全受损则不能再生,若损害不重而轴索又保存较好时,可以恢复。
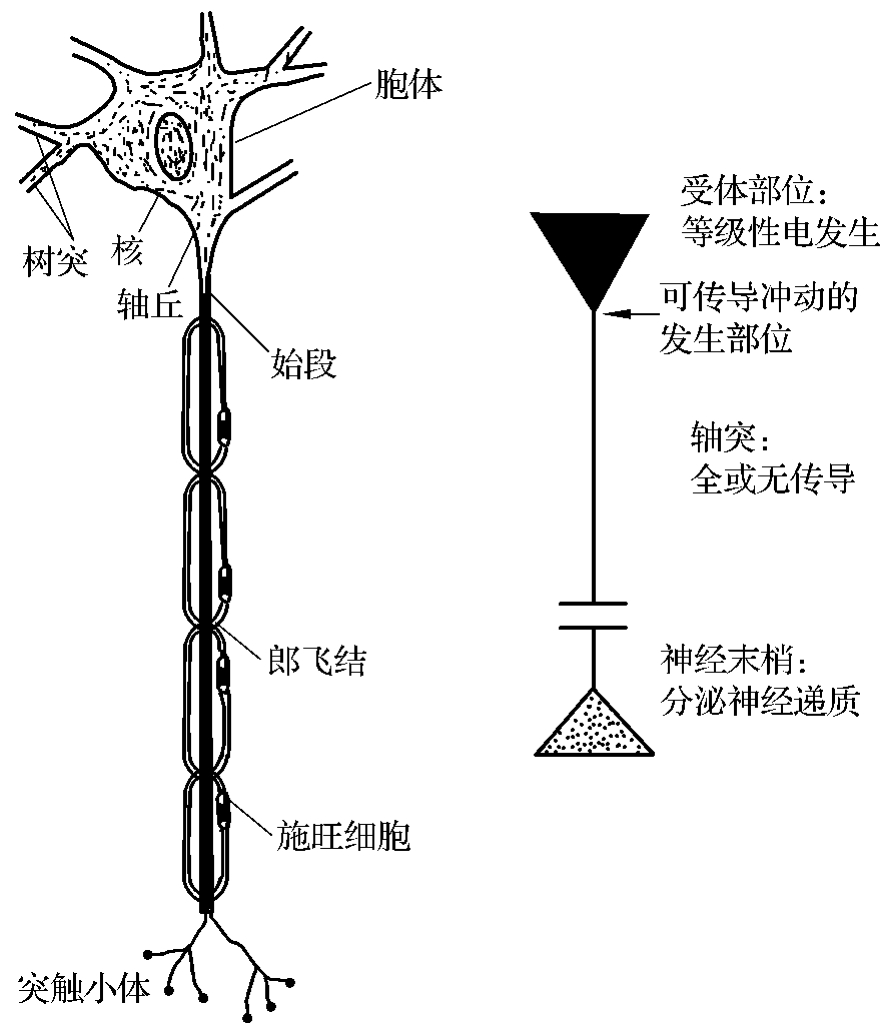
图4-1-3 有髓运动神经元及神经元的功能分段
轴突的末端分支较多,其末梢部分失去髓鞘,形成细的轴突终末,每个分支末梢的膨大部分称为突触小体(synaptic knob),它与另一个神经元相接触而形成突触(synapse)。神经元的胞体与轴突是一整体,胞体与轴突间经常进行双向的物质运输和交换。轴突表面的细胞膜称轴膜,内含的胞质称轴质,轴质内有许多与其长轴平行的微管和微丝、线粒体、滑面内质网和递质囊泡等。轴突内无尼氏体和高尔基复合体,故不能合成蛋白质,轴膜更新所需的蛋白质、神经递质囊泡及合成递质所需的酶等,由胞体输向终末。轴突终末内的代谢产物或由轴突终末摄取的物质如蛋白质、小分子物质或由临近细胞产生的神经营养因子、微生物或如破伤风毒素、狂犬病毒等进入轴突终末,沿轴突被逆向运输到神经元胞体,对神经元活动产生影响。轴浆运输与神经冲动传导无关,因为持续用局部麻醉药阻断神经冲动的传导,并不能使轴浆运输停止,其所支配的肌肉也不会发生代谢改变而萎缩。实验中若切断运动神经后,肌肉内的糖原合成减慢、蛋白质分解加速,肌肉逐渐萎缩;如将神经缝合再生,则肌肉变化可以恢复。目前认为,由神经元胞体合成的营养性物质借助于轴浆运输到神经末梢并经胞吐形式释放至所支配的效应器。
在神经元细胞体以及轴突和树突膜上存在一种β淀粉样前体蛋白(β-amyloid precursor protein,β-APP),是一种受体样结构的膜整合糖蛋白,具有维持和保护轴突结构的重要作用。病理状况下β-APP的分解过程发生异常时(图4-1-4),生成β淀粉样蛋白(amyloid betaprotein,Aβ)在轴索内积聚,使细胞骨架受到损害,而影响突触传递功能,最终可引起神经元变性、死亡,突触丢失等。
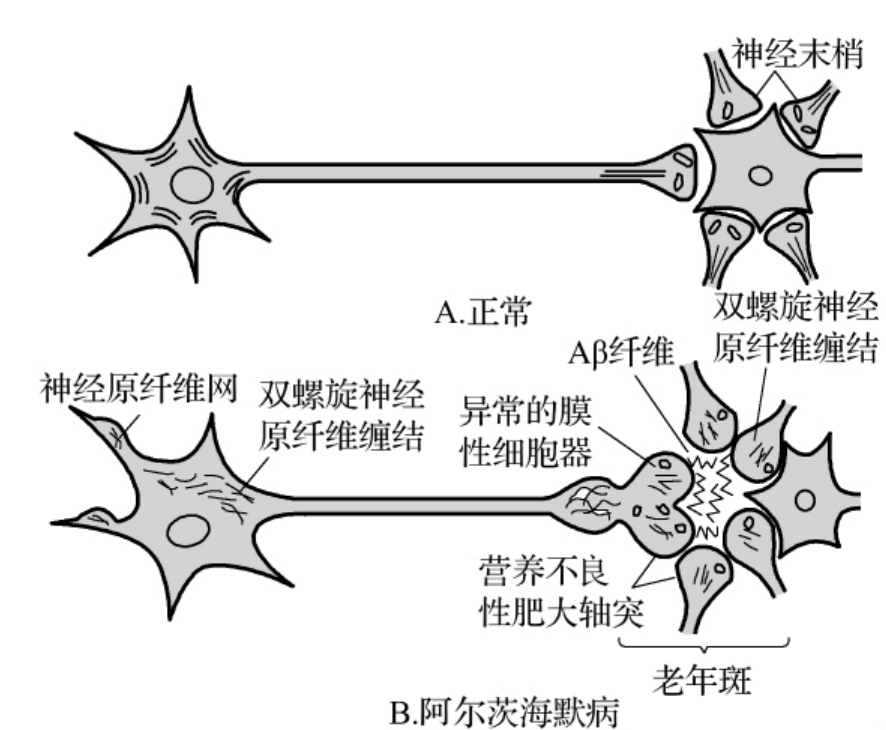
图4-1-4 阿尔茨海默病时神经原纤维缠结和老年斑
2.树突 树突的主要功能是接受信息的传入,并以衰减性的去极化和超极化电位的方式传至胞体,一般不产生动作电位。但近年来研究发现,某些神经元的树突上也可记录到动作电位。
神经元可发出数个树突,多时可达20个。每条树突粗而短,呈树状反复分支,越分越细,最后形成树突终末支。树突表面的终末支上还发出很多细小突起,称为树突棘,棘长短不一,其形状通常为细小的棘样、圆珠状或小片状。树突棘的数量及分布因神经元的不同而不同,如大脑皮质的锥体细胞有数千个至数万个树突棘,小脑的Purkinje细胞树突棘可多达十几万个,树突棘具有对传入神经元的刺激起调整作用。树突的分支及大量的树突棘可形成更多的突触连接,使树突接受刺激后易发生空间总和而快速传入信息。树突棘具有可塑性,它可随神经元的机能状态而变化,如在去神经纤维时,棘可减少甚至消失,而在学习过程中则可能发生新的树突棘以适应突触回路的变化。在哺乳类动物神经元的树突棘附近发现有Ca2+池形成,可能与学习和记忆过程中突触传递效应增强有关。
树突内的胞质基本上与核周质的结构相同,质内存在有多种细胞器,有尼氏体、线粒体、高尔基复合体、滑面内质网、神经细丝和微管等。粗树突内的主要特征是具有丰富的MAP-2A和MAP-2B微管细胞骨架成分,并呈规则地纵向排列,这一特征是用荧光抗体法鉴别树突和轴突的方法之一。
二、神经胶质细胞的特征与功能
(一)神经胶质细胞的特征
神经胶质细胞广泛分布于神经元胞体、突起以及毛细血管的周围,神经元由神经胶质细胞(glia cells)包围。其数量为神经元的10~50倍。中枢神经系统中主要有星形胶质细胞、少突胶质细胞和小胶质细胞三类,在周围神经系统中有形成髓鞘的施旺细胞和脊神经节内的卫星细胞(图4-1-5)。(https://www.daowen.com)
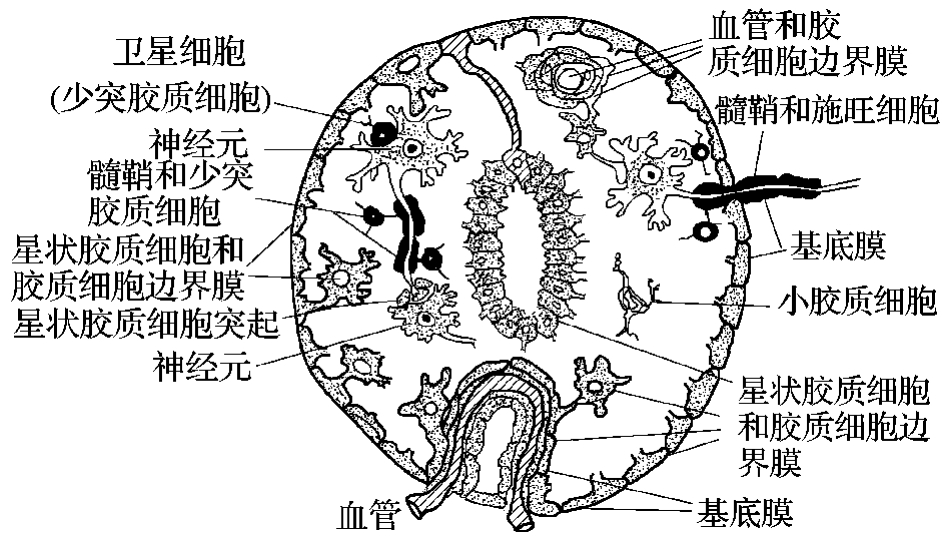
图4-1-5 各种胶质细胞填充神经元之间的空隙
胶质细胞体积小,突起多而不规则,无树突和轴突之分。其细胞膜与神经元膜一样,含有离子通道、神经递质受体、离子泵以及氨基酸转运体等。细胞之间不形成化学性突触,但普遍存在于低电阻、允许离子和小分子直接通过的缝隙连接。胶质细胞的膜电位也随膜外的K+浓度改变而变化,由于静息电位比神经元的更低,且膜上缺少Na+通道,不能产生动作电位。此外,胶质细胞终身具有分裂增殖的能力。
(二)胶质细胞的功能
胶质细胞的传统观念一直认为对神经细胞仅起支持、营养、绝缘、保护和修复功能。近几年的研究发现,胶质细胞对正常脑发育、生长、迁移、受损后的再生机制以及突触可塑性、突触传递及其信息整合等方面也发挥着重要作用。由于对星形胶质细胞研究较深入,重点介绍星形胶质细胞在神经系统复杂多样的重要作用。
1.星形胶质细胞功能 星形胶质细胞可分为纤维性星形胶质细胞(fibrous astrocyte)和原浆性星形胶质细胞(protoplasmic astrocyte)两种。纤维性星形胶质细胞多分布在白质,细胞呈星形,突起细长,分支较少,胞质内含大量胶质丝,该类细胞用免疫细胞化学染色技术能特异性地显示。原浆性星形胶质细胞多分布在灰质,细胞的突起较短粗,分支较多,胞质内胶质丝较少。
(1)支持、隔离和绝缘作用 神经元及其突起以外的空隙主要由星形胶质细胞的突起伸展充填。它们与神经元紧密相邻,并以其长突起在脑和脊髓内交织成网,充填在神经细胞的胞体及其突起之间,连接而构成支架,起支持和分隔神经元的作用。星形胶质细胞突起的末端常膨大形成终足,可覆盖到神经元的每一神经末梢,以阻挡不同来源的传入纤维活动的干扰。以前认为,神经髓鞘可防止神经冲动在轴突上传导时的电流扩散,使电信号在各神经纤维上的传导互不干扰;现在认为髓鞘的主要作用可能在于提高传导速度,而绝缘作用则可能是次要的。
(2)维持离子平衡 星形胶质细胞上的K+泵可将细胞外的K+泵入细胞内,并通过缝隙连接将K+扩散至其他胶质细胞,以维持神经元周围环境K+含量的稳定性。星形胶质细胞含有碳酸酐酶及H+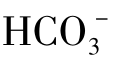 转运体,通过K+-Na+交换和
转运体,通过K+-Na+交换和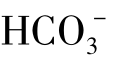 -Cl-交换方式,调节神经组织内的离子与pH值相对稳定,有助于神经元电活动的正常进行。若胶质细胞受损时,K+泵活动减弱,将导致细胞外液中K+浓度升高,可引起神经元的兴奋性升高而发生癫痫样放电。
-Cl-交换方式,调节神经组织内的离子与pH值相对稳定,有助于神经元电活动的正常进行。若胶质细胞受损时,K+泵活动减弱,将导致细胞外液中K+浓度升高,可引起神经元的兴奋性升高而发生癫痫样放电。
(3)参与神经递质的代谢 星形胶质细胞能摄取由神经元释放的谷氨酸(Glu)和γ-氨基丁酸(GABA)。在神经元内的Glu经脱羧酶作用下转变为GABA后由神经末梢释放入突触间隙,间隙中GABA一部分被星形胶质细胞再摄回,经酶的催化作用脱氨基转移至α-酮戊二酸形成Glu。Glu在谷氨酰胺酶的作用下加氨形成谷氨酰胺(Gln)转运到神经元内,从而消除氨基酸类递质对神经元的持续作用,同时也为神经元合成Glu和GABA递质提供前体和原料。星形胶质细胞合成Glu的过程,降低了脑氨,对保证脑的正常生存环境具有重要意义。
(4)合成活性物质 星形胶质细胞能合成和分泌20余种神经活性物质。如神经营养因子,包括神经生长因子(nerve growth factor,NGF)、睫状神经营养因子(ciliary neurotrophic factor,CNTF)和胶质源性神经营养因子(glial cell line-drived neurotrophic factor,GDNF)等。还能分泌血管紧张素原、前列腺素及几种白细胞介素(interleukin,IL),如IL21、IL23、IL26等。它们对维持神经元的存活和促进神经突起生长、发育、再生和分化均有重要作用。
一些类固醇前体能在脑内转化为具有生物活性的神经活性类固醇。Ismail等研究报道脑内雄激素及孕酮合成的主要部位在星形胶质细胞与少突胶质细胞。芳香化酶在脑发育过程中主要表达于干细胞或神经前体细胞[4],脑损伤后其表达有明显增高。脑内的雌激素是由雄激素在芳香化酶催化作用下转化而来,雌激素在中枢神经系统发育时可促进突触和髓鞘的形成、调节突触可塑性的作用,因而可预防或减缓老年性痴呆的发病。已有研究显示雌激素的作用是以载脂蛋白E(ApoE)依赖性的,在ApoE基因缺陷鼠,雌激素作用显著降低,而ApoE在中枢神经系统内主要由星形胶质细胞合成,现已证实其变异是导致阿尔茨海默病发生的一个高危因子。
(5)星形胶质细胞表面的受体 在中枢神经系统内,神经元与胶质细胞间存在着密切的双向相互调节途径。在星形胶质细胞膜上具有多种电压门控通道和神经递质的受体如谷氨酸、肾上腺素、多巴胺、5-HT、γ-氨基丁酸、乙酰胆碱、P物质、生长抑素、胰岛素等受体。这些受体能与神经元释放的相应递质结合,引起星形胶质细胞的Ca2+内流而发生去极化,被激活的星形胶质细胞可释放谷氨酸、ATP等递质,这些递质反过来可影响神经细胞的递质合成、改变离子浓度和促进突触形成等多种方式调节突触传递。
(6)诱导血—脑屏障的形成 星形胶质细胞的终足几乎包被脑毛细血管外面70%~80%的面积,它形成一层胶质界膜,是诱导微血管内皮细胞间紧密连接和维持血—脑屏障重要的结构基础。星形胶质细胞还能释放多种化学物质,调节内皮细胞的通透性。在分子水平上研究发现屏障相关蛋白的表达与星形胶质细胞源性因子存在密切相关。星形胶质细胞之间存有15~20 nm的间隙,内含组织液,互相沟通,是脑内的毛细血管与细胞外液及神经元之间进行物质交换的场所。
(7)引导神经元发生迁移作用 星形胶质细胞具有引导神经元迁移到目的地的桥梁作用,引导神经元迁移的胶质细胞在大脑皮质称为放射胶质细胞,在小脑称为Bergmann胶质细胞。在人的大脑和小脑皮层发育时期,这些细胞呈放射状排列,神经元得以沿着此桥架由发源地爬行迁移到达最终预定区域,提示星形胶质细胞参与了神经组织构筑的塑造;并影响神经元轴突的移动,促进神经元与其他细胞建立突触连接。研究表明中枢神经系统中的星形胶质细胞通过释放一种免疫系统分子(白血病抑制因子)来促进髓鞘的形成,这将可能为治疗脱髓鞘疾病提供新的方法[5]。
中枢神经系统变性和损伤时,星形胶质细胞增生、肥大,胞体及其突起可包围损伤和变性的神经结构,充填缺损的空隙,形成胶质瘢痕(glial scar)。过去,人们认为胶质瘢痕阻碍轴突再生,妨碍少突胶质细胞形成髓鞘和包裹轴突。现在认为,至少在损伤的早期阶段,反应的星形胶质细胞具有修复功能,星形胶质细胞可合成和分泌NGF等多种神经营养因子,支持神经细胞的存活和轴突的生长。
在神经移植过程中,在移植部位有纤维性星形胶质细胞增生,伴有各种形态和来源不同的巨噬细胞,其中有一部分来自局部的小胶质细胞。它们都参与神经营养反应,促进移植物存活和损伤细胞的再生。
(8)参与脑的免疫应答反应 传统观念认为,脑是与免疫系统作用“隔绝”的组织器官,因为脑内没有淋巴系统,仅存有血—脑屏障,可将免疫细胞和免疫物质拒之门外。但现在研究发现,脑内的星形胶质细胞具有抗原提呈细胞(antigen presenting cell,APC)作用,APC可将外来抗原介绍给特定的内源性分子——主要组织相容性复合体(MHC),并与外来抗原结合再激活T淋巴细胞,产生应答反应,排斥或破坏入侵的外来物质。
(9)参与突触信号传递和处理 近年来研究发现星形胶质细胞和突触之间以多种方式相互作用,参与了突触信号传递和处理。星形胶质细胞释放的ATP可发生突触抑制作用,在海马,突触前结构释放的谷氨酸可作用于星形胶质细胞的谷氨酸受体引起星形胶质细胞释放ATP[6]。
2.少突胶质细胞的功能
(1)少突胶质细胞的特征与分布 少突胶质细胞在银染色标本中,突起较少,胞体较星形胶质细胞略小,常呈串珠状。电镜下,细胞核中以异染色质为主;胞质中有丰富游离核糖体,粗面内质网和线粒体,Golgi复合体发达,有大量的微管。在中枢内的位置和分布:①束间少突胶质细胞分布在神经纤维周围;②神经细胞周围少突胶质细胞分布在灰质区的神经胞体附近;③血管周围少突胶质细胞主要分布在脑血管周围。
(2)少突胶质细胞的主要功能 ①一个少突胶质细胞发出多个板状突起包卷数条以至数十条轴突,形成有髓神经纤维。少突胶质细胞的突起接近神经元的轴突时,它的突起末端扩展成扁平薄膜,反复包卷神经元的轴突形成髓鞘。由于少突胶质细胞构成髓鞘,因此可利用髓鞘的某些物质,如髓鞘碱性蛋白(myelin basic,MBP)、髓鞘半乳糖脑苷脂(galactocerebroside,GC)、髓鞘相关糖蛋白(myelin associated glycoprotein,MAG)标记少突胶质细胞。②近年的研究表明,少突胶质细胞具有抑制神经生长的作用。因含有一些抑制因子,如NI-35、NI-250和髓磷脂连结糖蛋白(myelin-associated glycoprotein,MAG)等,能抑制再生神经元突起的生长。
3.小胶质细胞 小胶质细胞(microglia,MG)是胶质细胞中最小且数量较少的一种。电镜下细胞核以异染色质为主,核小,扁或三角形,染色深;胞质少且有较多溶酶体;其突起细长有分支,表面有许多小棘突。
中枢神经系统发育完成后,小胶质细胞处于静止状态;中枢神经系统受到损伤时,小胶质细胞被激活,可转变为具有吞噬能力的小胶质细胞,吞噬细胞碎片及退化变性的髓鞘。在血循环中的单核细胞亦侵入损伤区,转变为巨噬细胞,参与吞噬活动。
近年来发现,小胶质细胞是中枢神经系统的免疫细胞。在脑缺血时,损伤的神经元释放的细胞因子可促进吞噬细胞的生成,其释放的神经毒素能杀伤神经元,而吞噬细胞释放的细胞因子能刺激细胞修复过程,如生长转化因子1(TGF-l)对脑血管具有保护作用。
大多数学者认为淀粉样β蛋白(Aβ)沉积激活小胶质细胞引起的炎症反应和神经毒性作用是AD的核心病理机制。脑老化中星形胶质细胞不同程度的肥大,而部分小胶质细胞由静止型转为活化型。
三、神经营养因子
神经纤维对其所支配的组织能发挥两个方面的作用:一是通过神经冲动抵达末梢时释放神经递质,作用于突触后膜,调节所支配组织的功能活动,这一作用称为功能性作用;另一方面神经还经常释放一些营养性因子,借助于轴浆运输由胞体流向末梢,持续地调整被支配组织的内在代谢活动,影响其持久性的结构、生化和生理的变化,这一作用与神经冲动无关,称为营养性作用。这种营养性作用在正常情况下不易觉察,但神经损伤后便能明显地表现出来。如切断运动神经后,由于骨骼肌失去神经的营养作用,肌肉逐渐萎缩。用局部麻醉药能阻断神经冲动的传导,并不能使所支配的肌肉发生代谢改变,表明神经的营养性作用与神经冲动无关。
神经营养因子(neurotrophin factor,NTF)也可来源于神经所支配的组织(如肌肉)和星形胶质细胞,它们在神经末梢经由受体介导入胞,再经逆向轴浆运输抵达胞体,促进胞体生成有关的蛋白质,从而发挥其支持神经元生长、发育和功能完整性的作用。
(一)神经营养因子的生物学作用
20世纪80年代末期以来,随着生物技术的发展,已发现并分离到多种NTF,主要有神经生长因子(nerve growth factor,NGF)、脑源神经营养因子(brain-derived neurotrophic factor,BDNF)、神经营养因子3(NT-3)、神经营养因子4/5(NT-4/5)和神经营养因子6(NT-6)等。
NGF是最早发现的神经营养因子,广泛存在于人和多种动物体内。神经营养因子的主要生物学作用如下。
1.对神经系统作用
(1)神经元发育阶段 促进神经元的突起充分发育和突触形成,神经元特异递质合成酶的表达,以及膜离子通道和膜电位的出现。NGF可影响神经元的形态和轴突的数目增加;它还可促进交感神经元内的去甲肾上腺素酶系发育;若将NGF的抗体注入发育期间的动物,可使几乎所有的交感神经节受损;而将抗体注入母鼠则可导致胎鼠背根节感觉神经系统缺失。NTF是诱导神经纤维迁移到目的地的重要因素之一,它可通过靶区NTFs水平来控制NTF效应神经元的自然减数,从而控制神经元存活数量。剔除NTF-3基因可引起皮肤触—压觉感受器明显缺失;BDNF缺乏的小鼠,其周围感觉神经元数量减少,前庭神经节严重变性。
(2)神经元成熟阶段 一些外周和中枢的神经元仍需要一定水平的NTF维持其正常功能,NTF对损伤神经元具有保护和修复作用。大量资料显示,AD患者学习记忆与认知功能障碍累及了多种神经递质系统,其中以基底前脑的神经元投射到海马和大脑皮质的胆碱能系统受累最明显[7]。而实验中证实了向侧脑室灌注NGF能够防止AD模型鼠的胆碱能神经元逆行性溃变,能够明显提高AD鼠的空间学习记忆能力[8]。实验表明,NGF能提高基底前脑和纹状体胆碱能神经元的cAMP水平,增强胆碱乙酰转移酶的活性,阻止基底前脑神经元的死亡。因此NGF已被广泛地应用于AD、帕金森病、亨廷顿病、脊髓损伤和外周神经病变的治疗。
2.对其他组织的作用 NTF是多功能生长因子,可影响免疫、造血、内分泌和生殖等系统的功能。NGF促进肥大细胞增殖和生长,刺激淋巴细胞增殖。
(二)神经营养因子的受体
已发现神经末梢上有NTF受体,它是一类跨膜糖蛋白,以二聚体的形式存在,胞内部分具有酪氨酸激酶元件,NTF受体包括TrkA、TrkB和TrkC三种。TrkA受体对NGF的亲和力较高,TrkB受体对BD~NTF-4/5的亲和力较高,而TrkC受体则主要与NTF-3结合。当它们特异性结合后,可磷酸化受体的底物,后者能结合和激活磷脂酶C和磷脂酰肌醇激酶等信号转导系统,引起细胞内的多种生物反应。
(三)第二类神经生长因子
第二类神经系统的生长因子是细胞因子家族,它是一种存在细胞外液中的特异蛋白质,也能促进神经元的增殖、分化和存活。该家族成员包括睫状神经营养因子(ciliary neurotrophic factor,CNTF)、白血病抑制因子(leukemia inhibitory factor,LIF)、胰岛素样生长因子I(insulin likegrowth factor-I,IGF-I)、转化生长因子(transforming growth factor,TGF)、表皮生长(epidermal growth factor,EGF)、胶质细胞源神经营养因子(glial cell line-derived neurotrophic factor,GDNF)、成纤维细胞生长因子(fibroblast growth factor,FGF)和血小板源生长因子(platelet-derived growth factor,PDGF)等。
第二类神经生长因子的生物学作用是:①由施旺细胞和星形胶质细胞产生的CNTF,作用广泛,被称为多功能因子,它对于治疗人类运动神经元变性疾病有一定价值。在体外实验中,CNTF能作为运动神经元的存活因子发挥作用,它对外周及中枢多种靶神经元有促进存活和分化作用。外周神经切断后,CNTF表达上调,促使损伤后运动和感觉神经元的存活和轴突的再生;防止神经轴突离断所引起的运动神经元退变;还能改善运动神经元退变小鼠的行为并延长其生命。CNTF有保护基底前脑胆碱能神经元和黑质多巴胺能神经元的作用。CNTF对少突胶质细胞有促进存活及成熟作用,并保护其免受TNF介导的损伤。CNTF对免疫系统、造血系统和肝功能有影响;还对去神经的骨骼肌有营养作用。②GDNF在离体实验中,能维持中脑多巴胺能神经元的生存,诱导损伤的多巴胺(DA)能神经元长出新的突起。在帕金森病(PD)动物模型中,能保护DA能神经元的活性,可提高DA能神经元的存活率和神经末梢的密度,改善PD动物的行为。③EGF在体外培养中支持胚鼠脑皮质下神经元活存及突起生长。实验证明EGF在脑内有表达,其受体存在于神经组织,尤其存在于黑质中。
(周玉琴 张孟业)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





