第三章 外科常见全身并存病的围手术期处理
第一节 高血压病人的围手术期处理
动脉压随年龄的增长而升高。对于高血压的诊断标准,可根据世界卫生组织、国际高血压学会1999年的建议进行判断:①最佳血压:收缩压(SBP)<16.0kPa(120mg),舒张压:(DBP)<10.7kPa(80mm Hg)。②正常血压:SBP<17.3kPa(130mm Hg)且DBP<11.3k Pa(85mm Hg)。正常血压高值:SBP17.3~18.5kPa(130~139mm Hg)或DBP11.3~11.9kPa(85~89mm Hg)。③高血压:Ⅰ级,SBP 18.7~21.2k Pa(140~159mm Hg)或DBP12.0~13.9k Pa(90~99mm Hg);Ⅱ级,SBP21.3~23.9k Pa(160~179mm Hg)或DBP13.3~14.5kPa(100~109mm Hg);Ⅲ级,SBP ≥24.0kPa(180mm Hg)或DBP≥14.7k Pa(110mm Hg)。SBP与DBP属于不同度时,以高值为准。
以往有高血压病史,未经治疗而目前血压已正常者,不列为高血压;正在作降压药物治疗,目前虽血压正常,仍属高血压。
一、高血压病人围手术期的危险性
高血压病的早期,其病理特征为周身细、小动脉痉挛,日久管壁缺氧,呈透明样变性。小动脉压力持续增高时,内膜纤维组织和弹力纤维增生,管腔变窄,缺血加重,各脏器因供血不足而发生继发性病理改变,其中以心、脑、肾的病理损害最为突出。
高血压病人围手术期的危险性,取决于下列因素:①血压增高的程度与持续时间。②高血压以外的“危险因素”,如年龄,男性>55岁,女性>65岁;吸烟;总胆固醇>6.5mmol/L;并存糖尿病;有高血压家族史。③靶器官损害:如左室大,蛋白尿/血肌酐轻度升高,视网膜动脉变细等。④已存并发症:如脑梗死、脑出血、心肌梗死、心衰等。
(一)高血压对手术病人的主要病理生理的影响
1.可诱发心肌缺血,甚至心肌梗死 血压升高,虽可提高冠状动脉的灌注压,改善心肌供氧,但由于血压升高,心脏为克服外周血管阻力,心肌收缩力增强,心肌耗氧量增加,使心肌缺血(心绞痛)和心肌梗死的危险性增加。据报道,有心肌梗死病史者,如果术前存在高血压,术中及术后发生心肌梗死的概率为无高血压病人的2倍,或其中的23%的病人将发生心肌再梗死。
2.血压易于剧烈波动 高血压病人,由于压力感受器反射(baroreceptor reflex)敏感性下降,以及由于细、小动脉硬化,动脉壁弹性下降,血压自身调节能力变差,在围手术期血压易于剧烈波动。例如:①术前精神紧张、全麻气管内插管操作、麻醉过浅或作用不全、体腔内手术探查、术后疼痛刺激、低氧血症、高碳酸血症以及缩血管药物的应用等,均可使血压突然升高。②椎管内麻醉由于广泛血管扩张,全麻加深或全麻药与降压药物的协同作用,以及麻醉状态或/和存在血容量不足状态下的体位变动等易导致血压突然下降。过低血压对病人安全的威胁不亚于甚至超过高血压。
3.血管破裂、出血发生率增高 血压突然升高,可导致脑血管破裂、主动脉瘤破裂出血等并发症。SBP>24k Pa(180mm Hg)者,脑血管破裂出血的发生率较血压正常者高3.4倍。
4.重要器官血流灌注调节能力下降 除上述高血压对心肌的血流灌注与心肌耗氧的影响外,较为重要的是对脑、肾血流灌注的影响。高血压病人常存在脑及肾脏的中、小动脉硬化,导致这些器官血流灌注调节能力变差,术中、术后发生低血压时,易引起这些器官缺血。严重的肾脏缺血,可产生肾功能衰竭。
(二)高血压病人围手术期危险性的判断
Ⅰ、Ⅱ级高血压并存2个“危险因素”,属中度危险;Ⅰ、Ⅱ级高血压并存3个以上“危险因素”或存在靶器官损害,以及Ⅲ级高血压,属高度危险;Ⅰ、Ⅱ级高血压已存并发症,Ⅲ级高血压并存一个以上“危险因素”,靶器官损害或(和)并发症者,均属极度危险。基此,高血压的治疗不仅在于降压,更重要的是保护脏器,防止心、脑、肾病理损害的进展。
二、高血压病人的围手术期处理
(一)术前准备
术前准备的主要措施是:①应用抗高血压药物,使血压降至允许施行麻醉、手术的目标值;②处理危险因素,如治疗并存的高脂血症与糖尿病;③维护已存的靶器官损伤,包括改善心脏及肾脏功能等;④正在应用利尿剂者,要注意矫正水与电解质失衡。
表3-1 抗高血压药物分类表
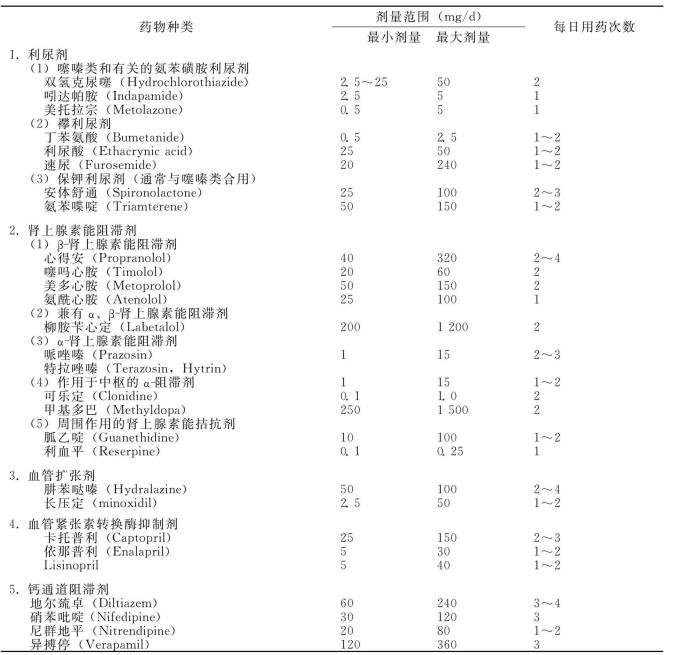
(引自谭新洪,黄震东.现代内科治疗学.广东科技出版社,1997,402~403)
1.抗高血压药物的应用 根据作用方式,抗高血压药物可分成5大类:利尿剂,肾上腺素能阻滞剂,血管扩张剂,血管紧张素转换酶抑制剂(angiotension-converting enzyme inhibitor,ACET)以及钙通道阻滞剂(见表3-1)。
重点介绍如下:
(1)利尿剂:包括噻嗪类利尿剂、襻利尿剂及保钾利尿剂。利尿剂的降压机制是通过抑制肾小管对钠离子和水再吸收,导致体内钠、水负平衡,使血容量减少,心排出量下降,血压下降。
噻嗪类属中效降压利尿剂,为首选,突出的代谢副作用是排钾,要注意钾的补充,以防低钾血症。襻利尿为强利尿剂,适用于中效利尿剂无效或伴肾功能不全的病人。保钾利尿剂为弱降压利尿剂,单独应用效果不佳,常与噻嗪类利尿剂合用,可减轻钾代谢紊乱。
(2)β-肾上腺素阻滞剂:是广泛用于治疗高血压的安全、有效的药物,其降压作用与阻滞β1-受体密切相关。降压的作用机制是:①心脏β1-受体被阻滞后,心率下降,心脏收缩力受抑制,心排出量降低;②抑制肾素分泌;③降低外周交感神经活性,使血管扩张。
从降压效果来看,各种β阻滞剂大致相同。在选择应用时应注意下列问题:①心动过缓、Ⅰ°以上房室传导阻滞、病态窦房结综合征病人禁用;②伴有慢性阻塞性肺病及糖尿病的高血压病人,应选用心脏选择性β-阻滞剂(如美多心安、氨酰心安)。然而,心脏选择性也是相对的,随着药物剂量增加,选择性就减弱,有严重哮喘和支气管痉挛的慢性阻塞性肺病者,即使是心脏选择性β-阻滞剂也是禁忌的。
(3)作用于中枢的α-阻滞剂:可乐定作用于延脑血管运动中枢α2-受体,抑制交感神经冲动。可乐定停药后6~8h极易发生反跳性高血压(rebound hypertension)。
(4)周围作用的肾上腺素能拮抗剂:如胍乙定(Guanethidine)、利血平(reserpine)及降压灵等。以往认为,长期服用后,由于交感神经末梢介质(去甲肾上腺素)贮存耗竭,麻醉和手术一旦产生低血压,可能难以纠正,因而主张术前1周停药。现在认为,术中血压波动主要取决于高血压的病理程度,与是否停药关系不大,再则,术前1周停药,如果术中血压过度升高,其危害性更大。
(5)血管扩张剂:肼苯哒嗪及长压定,直接作用于血管平滑肌引起血管舒张。因此类药副作用较多,一般不单独用于治疗高血压,仅在利尿剂、β-肾上腺素阻滞剂无效时加用此类药。
(6)血管紧张素转换酶抑制剂(ACEI):其作用是抑制血管紧张素I转变成具有强加压作用的血管紧张素Ⅱ,降低周围血管阻力,血压下降。ACEI副反应较少,最常见的副反应是刺激性干咳及高血钾。利尿剂能显著增强ACEI的降压作用。
(7)钙通道阻滞剂:是新型降压药,其作用机制主要是通过Ca2+内流和细胞内移动的阻滞而影响心肌及平滑肌细胞收缩,使心肌收缩性降低,外周血管扩张,阻力下降。常用的钙通道阻滞剂有心痛定(Nifedinin,硝苯吡啶)、异搏停(Verapamil)及地尔硫卓(Diltiazem)等,钙通道阻滞剂主要的副作用是面红、头痛和水肿。心痛定一次口服或舌下含服后10~15min血压下降,可引起反射性心动过速,异搏定及地尔硫卓可引起心动过缓及减慢房室传导。
2.抗高血压药物的应用方法 可参照1988年美国高血压委员会提出个体化阶梯治疗方案,其方案见图3-1。
据此方案,先选用第一阶梯药物(或称第1类药,即利尿剂,或β-阻滞剂,或钙阻滞剂,或ACEI抑制剂)。如血压未能满意控制,则加大第1类药物剂量(或改用该类另一种药),并加不同种的第2类药。如血压仍未能控制,则加不同种的第3类药,或换用第2类中的另一种药。依次类推,直至血压控制至允许施行麻醉手术的目标值。
3.降压的目标值 不能一概而论,取决于原有高血压的严重程度。一般认为,降压的目标值以18.7/12.0k Pa(140/90mm Hg)最为理想。临床实践中因各种原因,常遇术前降压未达预期目标值的病例,可按下述原则处理:
(1)择期手术,血压>24.0/14.7k Pa(180/110mm Hg)者,推迟手术。
(2)择期手术,血压18.7~21.3/12.0~14.7kPa(140~160/90~110mm Hg)者,应区别两种情况:①无症状,无靶器官损害者,并非择期手术的禁忌证。但仍有25%的这类病人术后因高血压导致心肌缺血、心肌梗死及心律失常发生,甚至有发生心源性死亡的危险。因此,应注意处理术后高血压及预防心脑并发症。②有症状及有靶器官损害的客观证据者,必须继续降压治疗,并使心、肾损害得到改善后方可手术。

图3-1 高血压的个体化阶梯治疗
(引自the“1988 Report of the Joint National Committee on Detection,Evaluation,and Treatment of I High Blood pressure.”Archives of Internal Medicinc,1988,148:1023~1038)
(3)单纯收缩压升高:以往认为,择期手术多不考虑收缩压水平,现已证实,围手术期心肌缺血的发生率与收缩压升高程度呈正相关。因此,对于60岁以上的老年病人,当收缩压≥21.3kPa (160mm Hg)者,应将收缩压控制在21.3kPa以下。
(4)急诊手术:可选用作用快、持续时间短的降压药,如硝普钠(Sodium nitroprusside),50~100mg加入葡萄糖液500m L,静脉滴入。如有条件最好用输液泵精确调整滴速:开始应为0.3μg/(kg·min),5min后增至1μg/(kg·min),以后据血压测定调整速率。避光,不能加入其他药物。
(二)麻醉及术中处理
硬膜外麻醉的主要危险是血压骤降,如处理不及时,甚至可导致心脏骤停,故必须精心管理,采用少量分次用药,逐渐诱导,及时观察、预防及处理低血压。全身麻醉血压波动较缓和,骤降概率相对较少,但麻醉中诱发血压波动环节多,调控难度大,术中应对病人进行全面监测(包括心率、血压、ECG、CVP、SaO2等),及时处理导致血压波动的原因。
手术操作要求轻柔,减少出血,防止血容量不足,避免手术操作本身导致血压剧升或骤降。
血压一旦发生剧升、骤降,其处理原则是尽早、小步、微调。
(三)术后处理
术后高血压更为多见,是术后发生心肌梗死的促发因素。术后高血压多因疼痛、寒战、意识恢复反应、气管留滞插管刺激、缺氧、高碳酸血症、液体超载、膀胱过度膨胀等引起,应给予及时处理。
术后如血压仍高,可恢复降压药物治疗。鉴于大手术后对应用降压药可能发生非特异性降压效应,此效应在术后2~4周才逐渐恢复,故在此期间,用药剂量应适当减少,或据血压测定进行调整。
第二节 心肌缺血病人的围手术期处理
尽管主动脉瓣狭窄、冠状动静脉瘘等心脏病亦可产生心肌缺血,但临床上最常见的病因是冠心病。
冠心病是由于冠状动脉粥样硬化使其管腔狭窄或阻塞,导致心肌缺血、缺氧。本节以冠心病为代表,讨论心肌缺血病人的围手术期处理。
一、影响心肌缺血的血液动力学因素
心肌耗氧量增加或/和冠状动脉供血、供氧量减少,均会使心肌耗氧量与供氧量之差增大,导致心肌缺血、缺氧。
引起心肌缺血、缺氧,主要与下列因素有关。
(一)血压
心肌收缩需要耗氧。血压升高时,为克服外周血管阻力,心肌收缩力增强,耗氧量增加。因此,凡是引起血压增高的因素,如气管插管,手术与疼痛刺激,以及应用缩血管药物等,都可诱发心肌缺血。
然而,有临床资料表明,单纯的血压升高并不一定都引起心肌缺血,甚至冠状动脉狭窄已达70%也是如此。因为血压升高固使心肌耗氧增加,但却能提高冠状动脉的灌注压,改善心肌供氧。
(二)心率
心脏单位时间收缩次数越多,心肌耗氧量愈大。其次,心室壁内膜下的心肌仅在心室舒张期才有血流灌注,心率增快,舒张期时值则相应缩短,心室内膜下心肌的血流灌注就减少。因些,心肌缺血的发生率与心动速率呈正相关。
(三)心率与收缩压的乘积(RPP)
基于心肌耗氧量与血压及心率呈正相关,心率(次/min)与收缩压(mm Hg)的乘积(rate pressure product,RPP)可作为反映心肌耗氧量的间接指标。RPP值愈大,表明心肌耗氧量越大,RPP值通常要求不超过12 000。然而,有研究表明,对于冠心病人,即使RPP值<12 000,亦能诱发心绞痛发作。
用RPP值判断诱发心肌缺血的可能性,应排除低血压对该值的影响。例如某病人收缩压为120mm Hg,心率为60次/min,如果此病人麻醉后收缩压降至60mm Hg,心率增至120次/min,这两种情况RPP值均为7 200。然而在后一情况,由于心率增快,心肌耗氧增加,而血压降低,使冠状动脉灌注量减少,则极易导致心肌缺血。因此,只有当收缩压大于或等于该病人原来平时的收缩压,用RPP值来判断心肌缺血的可能性才有价值。
(四)低血压
冠状动脉灌注需要具有一定的冠状动脉灌注压。冠状动脉灌注压与平均动脉压密切相关。即冠状动脉灌注压(Coronary perfusion pressure,CPP)是平均动脉压(Mean arterial blood pressure,MABP)与冠状窦压(Coronary sinus pressure,CSP)之差。
CPP=MABP-CSP
鉴于CSP很低,因此CPP实际上几乎等于MABP。
当冠心病病人的MABP降低,可诱发心肌缺血。但血压降至何种程度才诱发心肌缺血,主要取决于已存冠状动脉的狭窄程度。如果冠状动脉狭窄严重,MABP较正常下降5%~10%即可诱发心肌缺血,如果冠状动脉狭窄不太严重,MABP较正常下降50% ECG才能显示心肌缺血表现。
低血压与心率过速同时存在,是最易诱发心肌缺血的因素。
(五)中心静脉压
中心静脉压是反映心脏前负荷的指标,亦即心脏做功的指标。冠心病病人中心静脉压升高,可诱发心肌缺血。
(六)贫血
贫血使血液运输氧能力降低,对心肌供氧不利。
二、麻醉与手术对心脏的影响
(一)手术对心脏的影响
手术引起的创伤及疼痛,可导致交感神经兴奋性增高,血压升高,心率加速,心功能加强,心肌耗氧增加。术中出血及血容量丧失,如得不到及时补充,亦可致血压下降甚至休克,使冠状动脉灌注不足。此外,低氧血症、高碳酸血症,也是心肌缺血缺氧的原因。
(二)麻醉对心脏的影响
局麻对心脏及血液动力学基本无影响。椎管内麻醉(硬膜外或蛛网膜下腔麻醉)对心脏及血液动力学的影响决定于麻醉平面的高度,高位硬膜外麻醉,血管扩张范围广泛,可致血压迅速下降,如未及时处理,将导致冠状动脉灌注不足甚至心力衰竭。气管内麻醉,作气管插管时,由于迷走神经反射,可发生窦性心动过缓,房室交界区异位搏动甚至心脏骤停。全麻所应用的多数麻醉剂,对呼吸循环均有抑制作用。吸入麻醉时如供氧不足,呼吸道不通畅或过度抑制,都可引起缺氧和二氧化碳贮积,诱发心肌缺血。
三、术前对冠心病病人手术耐受性的判断
冠心病病人对手术的耐受性取决于心功能状态,全身状况及手术类型。术前应根据病史、体征及有关特殊检查(ECG及负荷ECG试验,超声心动图等)综合判断。
(一)心脏代偿功能与手术耐受力
总的说来,心脏代偿功能“良好”或“较差”者(相当于心脏功能0~Ⅱ级),一般都能较好地耐受手术,手术死亡率较低;而代偿功能削弱或严重损害者(心功能Ⅲ~Ⅳ级)手术死亡率高,必须作好术前准备,改善心功能方能手术。见表3-2。
表3-2 心脏代偿功能与手术耐受力的关系

注:*屏气试验:为测定心功能的简易方法,可让病人深吸气后屏气,计算能耐受的时间,应与临床表现对照参考。
(二)心脏危险因素记分法
1977年Goldman等前瞻性地对40岁以上1 001例非心脏外科手术病人,采用多元分析方法建立了心脏危险因素记分法。该记分法对于手术前估计发生心脏并发症的危险性,迄今仍有重要的指导意义(见表3-3、表3-4)。
表3-3 心脏危险因素记分
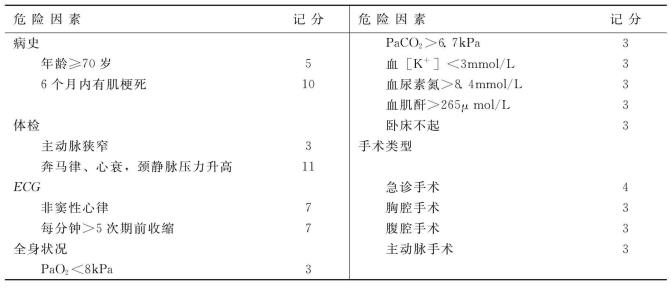
危险因素记分的积分越多,发生心脏并发症的危险性越大。积分>26分者,心脏病并发症的死亡率达56%,故积分>26分者不应施行任何择期手术。
表3-4 危险因素积分与围手术期严重心脏并发症发生率的关系

采用心脏危险因素记分法判断非心脏外科手术病人发生严重心脏并发症的危险性,不但考虑到了心脏本身的状态,还考虑到了全身状况和手术类型。此外,在心脏危险因素记分中,有相当一部分是可以通过适当处理来降低评分,从而降低了心脏病人手术的危险性,对于防治心脏并发症有指导意义。
四、冠心病病人的围手术期处理原则
(一)术前评估与准备
1.隐匿型冠心病 指病人无症状,仅有心肌缺血的心电图表现者。手术危险性较小,术前不需作特殊处理。然而,由于麻醉与手术引起的应激,无症状的心肌缺血可以进展为心绞痛甚至心肌梗死。因此,麻醉及手术中,应作好心电图及血液动力学监测,避免前述引起心肌耗氧量增加及冠状动脉灌注减少的因素,预防心肌缺血的发生。
2.稳定型心绞痛 是指由于体力劳动或其他因素(如情绪激动)导致心肌耗氧增加而诱发心绞痛者,其病理基础是冠状动脉狭窄,冠状动脉血流量不能适应心脏做功强度的增加而相应增加。
稳定型心绞痛虽不是麻醉与手术的禁忌证,但应充分作好术前准备,防止心肌进一步缺血。
(1)借助踏车试验判断其对手术的耐受能力 术前踏车试验,以测定出现心绞痛或心电图出现心肌缺血性改变的RPP值,可根据此RPP值的大小判断心绞痛的轻重程度。例如,一病人踏车试验10min,当心率达150次/min,收缩压为170mmHg时出现心绞痛,其时的RPP值为22 500,而另一病人踏车试验3min,当心率达100次/min收缩压为135mmHg时出现心绞痛,其时的RPP值为13 500。显然前一病人冠状动脉狭窄程度较轻,麻醉与手术危险性较小。术中及术后可据此RPP值控制心率及血压变化,预防心肌缺血的发生。
(2)抗心绞痛药物
1)硝酸酯制剂:其作用为扩张周围血管,减少血液回流,从而减少心肌耗氧;扩张冠状动脉。
硝酸甘油:舌下含片0.3~0.6mg;口服缓释剂,2.5mg,1日2次;1%~2%硝酸甘油软膏,涂于皮肤;硝酸甘油贴膜外贴于皮肤。
消心痛:口服5~20mg,每4~6h1次。
2)β-受体阻滞剂:其抗心绞痛的作用主要是通过降低心率及减弱心肌收缩强度,以减少心肌耗氧量,如心得安、心得平等。
抗心绞痛药物应常规应用直至手术日晨,以免因突然停药而导致心肌供氧与耗氧失衡。此外,手术前晚及手术日晨,应用镇静剂消除焦虑。
3.不稳定型心绞痛 其心绞痛症状加重,引起发作的刺激阈值降低,发作持续时间延长,间隔变短,或在静息状态和清醒时有心绞痛发作,是病情严重的表现。不稳定心绞痛可以是心肌梗死的前兆,故又称梗死前心绞痛或中间综合征。不稳定型心绞痛出现3个月内,约有30%病人发生心肌梗死。
不稳定型心绞痛手术危险性大,只有急诊手术才不得已施行。一般手术应推迟进行,进行内科治疗,待心绞痛稳定后再手术。
4.有心肌梗死史者 有心肌梗死史者,约有6%病人术后发生再梗死,再梗死一旦发生,死亡率达50%以上。手术期距心肌梗死时间愈近,再梗死发生率愈高,心肌梗死后3个月内手术者,再梗死率约30%,3~6个月者约20%,6个月者下降至10%以下。因此,择期手术应推迟至心肌梗死6个月后施行。
(二)术后处理
冠心病病人手术后心脏情况并不能改善,且由于手术创伤的打击还可能加重。因此,重点仍是防治心肌缺血,警惕急性心肌梗死的发生。术后心肌梗死,常发生于术后1周,尤其是3d内。多常表现为血压突然下降,心衰,心律失常或心脏骤停。可靠的诊断依据是心电图改变。因手术所造成肌肉组织损伤亦可释出肌酸激酶(creatine kinase,CK)和乳酸脱氢酶(Lactase dehydrogenase,LDH),故这些血清酶学检查对心肌梗死诊断价值不大,心型同功酶(如心型肌酸磷酸激酶,即CK-MB)测定对诊断有帮助。
术后处理的要点仍是防止心肌供氧与需氧之间的失衡,包括镇痛、吸氧、矫正水与电解质失衡,保持血液动力学稳定以及β-受体阻滞剂的应用等。
第三节 慢性肺部疾病病人的围手术期处理
一、呼吸生理简要及肺功能测定
呼吸系统的主要功能是体内、外之间的气体交换。呼吸生理的全过程包括以下各环节(图3-2):

图3-2 呼吸生理全过程
肺泡与外界之间的气体交换,称为“肺通气”;肺泡与肺循环毛细血管之间的气体(O2及CO2)交换,称为“肺换气”,肺换气需通过肺泡-肺毛细血管壁(即“呼吸膜”)屏障。肺脏借其通气功能和换气功能,为组织代谢提供O2,并排出体内代谢产物CO2。
(一)涉及“肺通气功能”的若干指标
1.肺活量(vital capacity,VC) 是指深吸气后,缓慢呼出的最大气体容量。肺活量的变化能反映肺组织病理和生理变化,成年男性平均值为3 500m L,女性为2 500m L。
用VC值判断肺功能的缺点是不能反映肺组织的弹性及呼吸道的通畅程度,因为测量VC时不受时间限制,只反映呼出的最大总气量,慢性阻塞性肺部疾病病人(如阻塞性肺气肿),其VC量与健康人差不多。但VC仍是反映限制性肺部疾病、肺通气功能有价值的指标。
2.用力肺活量(forced vital capacity,FVC) 是指在最大吸气后,尽最大努力快速呼出的气体容量。正常人FVC与VC接近。但在严重慢性阻塞性肺病时,因肺内气体不能顺利排出,FVC明显小于VC。故FVC测定对慢性阻塞性肺病病人更具有诊断价值。
3.功能残气量(functional residual capacity,FRC) 是指平静呼气之末肺内所剩下的气体量。它约占肺总容量(TLC)的40%,成年男性平均为2.4L,女性为1.8L。功能性残气量的存在,使在呼吸运动的间歇期肺泡气与肺毛细血管内血液气体仍能进行交换。在FRC位(即平静呼气末期位)时,胸壁的弹性回缩(增加肺容量)和肺的弹性回缩(减少肺容量)取得平衡,二者相等,但方向相反。肺气肿时,肺弹性回缩减少,FRC增加;相反,肺水肿、间质纤维化和其他限制性肺部疾病造成肺硬度增加,FRC下降。
4.肺总容量(total lung capacity,TLC) 是深吸气后肺内所含气体的容量,即肺活量与残气量之和。成人男性平均5 000m L,女性3 500m L。肺组织广泛性病变、纤维化、胸腔积液、气胸等肺总容量减少。
5.第1秒钟用力呼气量(fored expiratory volume in one second,FEV1) 是测量FVC过程中测定第1秒钟的呼气量,亦是用于测量气道阻力的方法。正常人FEV 1值>70%的肺活量(该值常用占肺活量的百分比表示,即FEV 1% VC)。
6.最大通气量(maximal voluntary ventilation,MVV) 是指每分钟尽力(主动用力,尽可能深,尽可能快)的最大呼出或吸入的气体容量。MVV受呼吸肌收缩力、气道阻力、胸壁和肺的顺应性、病人测试时合作程度及全身一般状况等因素影响,是测试肺通气功能的综合指标。在15s内进行快而深的呼吸,将此期间呼出的气量乘4,所得通气总量即为最大通气量。正常为100~200L/min。
最大通气量减去安静时的通气量,其差值与最大通气量的百分比,称为“通气贮备百分比”,正常人的通气贮备百分比在93%以上,若低于70%,表明肺通气功能不良。
![]()
7.肺泡通气量(V A) 是指每分钟进入肺泡气体的气量,是与血液中进行气体交换的有效部分,故又称“有效通气量”。
(二)影响“肺换气功能”的主要因素及其判断指标
1.影响“肺换气功能”的主要因素
(1)肺泡与肺动脉血O2、CO2的分压差:“呼吸膜”是半透膜,其两侧(即肺泡与肺毛细血管内的肺动脉血)的气体交换取决于该气体的分压差。肺泡中O2分压为100mm Hg,肺动脉血中O2分压为40mm Hg,故肺泡中的O2向肺动脉血中扩散;肺泡中CO2分压为40mm Hg,肺动脉血中CO2分压为46mm Hg,故肺动脉血中CO2向肺泡中扩散。
维持病人通气功能,增加吸入气体的O2分压(如给病人吸入O2),能提高肺泡内气体的氧分压,有利于O2向肺毛细血管弥散。
(2)呼吸膜的生理功能:因某种(或某些)疾病,肺泡膜的面积减少(如肺不张,肺纤维化),或呼吸膜增厚(如肺间质水肿),气体弥散阻力增高,可引起低氧血症和高碳酸血症。
(3)肺泡通气/肺泡血流比值(V/Q):肺泡与血液进行气体交换,不但要有足够的肺泡通气量,还要有相应的肺泡血流量。肺泡通气量不足或肺泡血流量减少均使肺换气功能降低。
正常肺泡通气量每分钟为4.2L,肺泡血流量每分钟为5L,V/Q比值为4.2L/5L=0.84,此时肺泡与肺泡血流之间的气体能进行充分交换。
若肺泡通气量减少,而肺泡血流量不变时,V/Q<0.84,肺泡血流氧合不全导致PaO2↓、PaCO2↑。若肺泡完全萎缩或充满液体,所通过肺泡的血流完全不能氧合,形成动-静脉短路。
若肺泡血流灌注减少,而肺泡通气良好,肺泡无效通气增加,V/Q>0.84,亦导致PaO2↓、PaCO2↑。
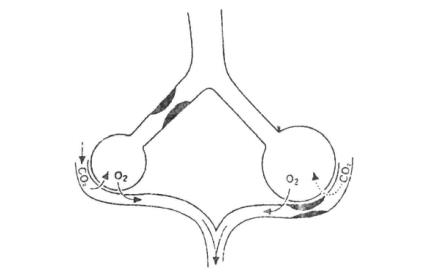
图3-3 右侧肺泡通气下降(如分泌物,支气管痉挛)肺动脉血氧合不完全,V/Q<0.84,导致PaO2↓、PaCO2↑;左侧肺泡通气良好,但肺泡血流灌注差,肺泡无效通气增加,V/Q>0.84,亦导致PaO2↓、PaCO2↑
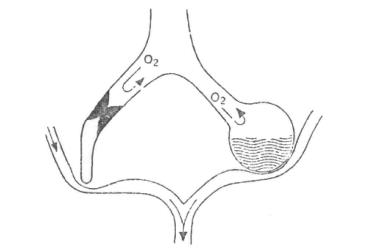
图3-4 肺泡完全萎缩(右)或充满液体(左),但血液仍能通过无通气区域,形成动-静脉短路,导致低氧血症
2.“肺换气功能”的判断指标 PaO2、PaCO2与肺换气功能关系密切,是判断肺换气功能的重要指标。此外,血氧饱合度(SaO2)测定亦有一定价值。
(1)动脉血氧分压(PaO2):表示动脉血中物理溶解的O2分子所产生的张力和压力。健康人在海平面大气压下呼吸时正常值为10.7~13.3k Pa(80~100mm Hg)。其值与年龄呈负相关,与年龄的关系按下列公式计算:PaO2=102-0.33×年龄。(例如65岁的健康人,PaO2值应为102-0.33×65 =80.6mm Hg)。但即使年龄再大,正常人也不应低于70mm Hg。
(2)动脉血二氧化碳分压(PaCO2):表示动脉血中溶解的CO2产生的张力和压力。是反映通气功能的一个极敏感指标,正常值4.67~6.0kPa(35~45mm Hg)。PaCO2>45mm Hg,表示通气不足,可形成呼吸性酸中毒。
(3)氧饱和度(SaO2):是指单位血液中Hb实际结合O2量与应当结合O2量之比。例如100m L动脉血含Hb 14g,实际测得O2含量为18m L,鉴于每克Hb最多能结合1.34m LO2,则其SaO2为18/14×1.34≈96%。正常为95%~97.5%。该指标虽亦反映肺的氧合情况,但不及PaO2敏感。SaO2主要决定于PaO2,但二者并不呈直线关系,而呈“S”形曲线,它一般反映血液携带O2的状况,故SaO2乃为浓度之比,而并不表示绝对O2含量的多少。
二、慢性肺部疾病病人术前肺功能判断
(一)慢性肺部疾病的类型
可将慢性肺部疾病分为两类:①慢性阻塞性肺部疾病(chronic obstructive pulmonary disease,COPD),最为常见,如慢性支气管炎、哮喘所引起的阻塞性肺气肿及支气管扩张等,其特点是由于气道狭窄或阻塞造成呼气流速降低,肺通气功能测定FVC、FEV 1、FEV 1% VC及MVV均明显下降;②限制性肺部疾病(restrictive lung disease,RLD),是指肺扩张受限的肺部疾病,如肺纤维化,肺不张、液胸、气胸、严重脊柱或胸廓畸形均属之,其特点是肺容量低于正常值,肺功能测定VC、MVV减少,而呼气流速测定可在正常范围。
有时同一病人兼有两类不同的疾病。
(二)术前肺功能测试的指征
大多数拟行腹部手术的病人,术前并不需作肺功能测定,术后也不致发生肺功能严重受损,即使发生某些肺部并发症,通过处理与治疗,也能得到控制。然而,下列情况可能预示肺功能存在受损,拟作腹部中、大手术者,需作肺功能测定:①年龄≥40岁,且具有慢性咳嗽、咯痰或轻度体力活动后出现呼吸困难者。②年龄≥65岁者。③长期吸烟且有呼吸道症状者。④过度肥胖者。⑤已明确患有慢性肺部疾病者。至于静息状态已有呼吸困难者,说明呼吸功能已处于衰竭状态,难以承受手术刺激。
(三)肺通气与换气功能受损程度的判断
1.肺通气功能受损的“高危值”(表3-5)
表3-5 肺通气功能受损的高危值

2.肺换气功能受损程度的判断(表3-6)
表3-6 动脉血气分析与肺换气功能的关系

肺通气功能的“高危值”和小于“高危值”,以及动脉血气分析显示轻度不全以上者,预示肺功能已遭受较明显损害,除非急诊手术,术前均需一段时间处理与治疗,使肺功能得以改善才能施行手术,否则术后肺部及全身并发症难以避免。
三、麻醉及手术对肺及肺功能的影响(一)肺通气功能下降
麻醉及手术可使肺通气功能下降,其主要原因是:①膈肌抬高:术中及术后的平卧位或侧卧位,使膈肌较直立位上升4cm,导致胸腔内压增高,进而导致TLC、FRC、MVV及V A的下降。②呼吸肌收缩力减弱:全麻及高位硬膜外麻醉所导致的膈肌和/或肋间肌松弛,使胸腔容量减少,FRC仅为生理状态的75%~90%。当FRC值小于闭合容量,则导致肺膨胀不全。③膈肌活动度减弱:腹部手术后,由于手术操作及切口疼痛,反射性地使膈肌活动幅度减弱,呼吸变浅变快,呼吸道解剖死腔增大,肺泡通气量减少。例如,呼吸频率10次/min,肺泡通气量为4 000m L/min,而呼吸频率增至30次/min,肺泡通气量则降至1 500m L/min。④呼吸对PaO2、PaCO2改变的反应性下降:生理状态,当PaO2<8kPa(60mm Hg)时,呼吸则加深加快,以增加肺通气量,提高PaO2;PaCO2增高时亦然。但在全麻、镇静及镇痛剂应用、深睡、并存碱中毒及老年病人,这种反应性下降,肺通气量及低氧血症不能及时改善。
有学者临床研究显示,腹部手术后潮气量下降20%,肺活量减少25%~50%,功能性残气量减少20%。上腹部手术、老年人下降更为显著。
(二)对肺换气功能的影响
除肺通气功能下降对换气功能的不利影响外,如果在围手术期,存在血容量不足,使肺泡血流灌注不足,V/Q>0.84,或输液超载,导致肺间质水肿,呼吸膜厚度增加,均对肺换气功能造成不利影响。
(三)肺部并发症发生率高
肺不张、肺炎、吸入性肺炎及呼吸功能衰竭等是气管内麻醉和胸腔手术最常见的术后并发症。其原因是:①气管内麻醉及复苏期,呼吸受抑制,肺通气量减少,气管纤毛运动功能降低;②由于切口疼痛和镇痛药物的应用,以及呼吸肌收缩力减弱,使呼吸反射下降,呼吸道分泌物不能有效地排出;③术中及术后较长期平卧位或侧卧位。(https://www.daowen.com)
此外,尚有其他因素促使术后肺部并发症的发生。①长期吸烟:吸烟者,术后肺部并发症发生率增加5倍。②年龄:老年人肺组织与功能发生退行性变;慢性肺部疾病发生率高;咳嗽反射减弱。③过度肥胖:胸壁顺应性降低;代谢高,呼吸功能负担重;为克服胸壁重量,呼吸运动机械负荷增加。
(四)低氧血症
严重的肺功能受损,均可导致低氧血症。
在已存在慢性肺部疾病的病人,肺功能贮备能力差,麻醉及胸、腹部手术对其影响更为显著。
四、围手术期处理要点
(一)术前处理
术前处理的目的是治疗已存的慢性肺部疾病,改善肺功能,增强对麻醉与手术的耐受能力,减少术后并发症。
(1)加强营养,适当的体力活动,练习有效咳嗽及深呼吸,以增强肺功能。
(2)停止吸烟:择期手术前,停止吸烟2周以上,以恢复气管黏膜纤毛运动,减少呼吸道分泌物,消除黏膜肿胀,改善通气功能。
(3)应用抗生素:呼吸道感染症状明显、痰量多及有脓性痰者,根据痰培养和药敏结果,术前5 ~7d给予敏感抗生素控制感染,同时给气道雾化吸入,1日3次,具有使黏稠痰液变稀薄、促进呼吸道黏膜充血肿胀好转的功效。
(4)应用支气管扩张剂:利于改善支气管痉挛因素所引起的阻塞性肺功能不足(如哮喘、慢性支气管炎),如给予口服、肌注或静脉滴注氨茶碱,吸入舒喘宁,经常发作的哮喘病人,给予肾上腺皮质激素。
(5)严格的口、鼻腔卫生处理,每日刷牙2次。
(二)术中及术后处理
(1)选用对呼吸功能影响较小麻醉方法:尽可能不采用气管内麻醉,全麻时维持足够的肺通气量;全麻复苏期吸净呼吸道的分泌物,防止和及时处理误吸。
(2)及时矫正血容量不足,以保证肺泡血流灌注;同时防止输液过多及晶体液成分过多引起液体超载及肺水肿。
(3)全麻病人清醒后及硬膜外麻醉6h后,如无其他禁忌证,及时置病人于半卧位。
(4)全麻手术病人,术后第一天常规拍打病人背部,鼓励、指导和协助病人深呼吸及咯痰,是预防治疗肺不张、坠积性肺炎的有效方法。
(5)一旦具有停止胃肠减压的指征,及时拔除鼻胃管,以免影响深呼吸及咯痰。
(6)鼻导管气管内吸痰:适用于年老、痰多、肺不张而无力咳嗽的病人。方法是将14~18号无菌橡皮导管,自鼻孔插入咽部,病人头稍后仰,此时要病人用力快速深吸气,与深吸气的同时,将导管快速插入。病人出现连续剧烈哑声咳嗽表明导管已插入气管,此时将导管末端连接吸引器,反复上下移动并左右旋转导管,吸出气管内稠厚的分泌物。每次吸痰数秒钟,间歇进行,以免过度刺激造成缺氧。
(7)气管切开的应用:气管切开可减少呼吸道解剖死腔(可从150m L减少至50m L),增加有效的气体交换量。气管切开后,呼吸道内积存的分泌物容易吸除,还可经气管套管滴入药物(如抗生素,α-糜蛋白酶)和施行雾化吸入及吸氧。当存在术后肺部并发症且出现呼吸功能不全,在吸O2后病人SaO2仍小于84%,PaCO2不能降至6.6k Pa(50mm Hg)以下时,应及时施行气管切开。
(8)吸氧:氧吸入,可提高吸入气体的氧分压(PaO2),提高肺泡与毛细胞血管之间的氧分压差,改善低氧血症。在COPD病人,只要气道未完全阻塞,增加吸入氧分压(PiO2)即可纠正低氧血症,因为在低氧肺泡还存在一个很高的弥散梯度。PiO2从24%增加到28%即可较满意地纠正由于V/Q失调(V/Q>0.84)所致的低氧血症。
(9)呼吸机辅助呼吸:全麻复苏期或者术后出现下列情况者,应考虑带气管导管或气管切开回ICU病房并给呼吸机辅助呼吸:①严重通气不足,如COPD病人并发急性呼吸衰竭、中枢性呼吸衰竭及呼吸肌麻痹等。②严重换气障碍合并通气障碍。③胸部及心脏手术等并发急性呼吸衰竭时。
(10)合理选用抗生素:鉴于慢性肺部疾病病人的免疫功能低下,且术前多已用过抗生素,术后应选用广谱及敏感的抗生素。
第四节 糖尿病病人的围手术期处理
一、概述
糖尿病(Diabetes mellitus,DM)是因胰岛素分泌绝对或相对不足或靶细胞对胰岛素敏感降低,临床上以高血糖为特征的综合征,严重者导致糖尿病酮症酸中毒(Diabetic ketoacidosis,DKA)或非酮症高血糖-高渗性昏迷(Nonketogenic hyperglycemia-hyperosmotic coma,NKHHC)。其晚期并发症包括糖尿病肾病、神经病变、高血压、周围动脉病变、视网膜及白内障。
糖尿病分型:按照美国糖尿病协会(ADA),1996年的规范,糖尿病分下列4型,表3-7。
1型约占糖尿病总数的10%~15%,见于儿童及30岁以前的成年人,病人不肥胖,是与遗传有关的自身免疫性疾病。1型的易感性受到遗传因素影响,病人有特殊的HLA表型。导致β细胞自身免疫损害的特异性抗原虽尚不完全清楚,但80%的1型病人体内可检出胰岛细胞抗体(ICA)或/和胰岛细胞表面抗体(ICSA)以及致敏T淋巴细胞,病理组织学的特征是胰岛炎。由于自身免疫导致的胰岛炎性损害,体内胰岛素绝对缺乏,需长期依赖胰岛素治疗。1型易发生DKA。
2型占糖尿病总数的85%以上,见于30岁以后的成年人,病人多肥胖,其发病机理是靶细胞对胰岛素不敏感或β细胞对因胰岛素阻抗所导致的高血糖不能有效地代偿性分泌增加,其结局是胰岛素相对不足。肥胖及2型家族史是其发病的危险因素。此型不伴DKA倾向,但易发生NKHHC,重要的慢性并发症是动脉粥样硬化冠心病。
表3-7 糖尿病分型(1996,ADA)

当二次以上空腹血浆葡萄糖(FPG)值≥7.8mmol/L(140mg/d L),可诊断为糖尿病。如果FPG<7.8mmol/L,但口服葡萄糖耐量试验(OGTT)在葡萄糖负荷后2h FPG值为7.8~11.1mmol/L者,为糖耐量异常(Impaired glucose tolerance,IGT)。
我国自然人群糖尿病的患病率为0.6%~1.0%,40岁以上者达3%~4%。约1/3的糖尿病手术病人是在术前初次被发现,因此术前应常规测血糖、尿糖,以防漏诊。
糖尿病病人较非糖尿病病人手术危险性明显增加,如围手术期处理不当,其死亡率可增高2倍之多。
二、糖尿病病人手术的危险性
1.手术可使血糖进一步升高 非糖尿病病人,手术所产生的神经内分泌反应,即可导致应激性高血糖(Stress hyperglycemia)和胰岛素阻抗(Insulin resistance),使血糖升高。而对糖尿病病人来说,由于本已存在胰岛分泌绝对或相对不足和靶细胞对胰岛素敏感性降低,手术刺激导致的升糖反应更为显著。
当血糖>10mmol/L时,尿糖则可为阳性;当血糖升至15~20mmol/L,则产生明显的渗透性利尿;当血糖>33mmol/L,血浆渗透压>320mmol/L时,则产生非酮症高血糖-高渗性昏迷。此外,病情重者,还可发生酮中毒及酸中毒等严重并发症(表3-8)。
表3-8 不同血糖浓度的临床表现

2.易发生心血管及肾脏并发症 糖尿病病人易导致心血管及肾脏功能损害,其损害的发生率及程度与糖尿病的严重程度、病程呈正相关。大体地说,其心血管、肾脏的功能相当于其实际年龄,加上患糖尿病年限之和的普通人的功能。病程超过10年者,冠心病、高血压等动脉粥样硬化并发症的发生率为同龄非糖尿病者的11倍。糖尿病发生20年后,约50%有糖尿病、肾病的临床表现。因此,糖尿病病人术前应作好心血管及肾脏功能检测,预防心、肾并发症的发生。
3.血管舒缩调节功能差 这与糖尿病所并发的植物神经病变有关,由于血管舒缩神经调节功能障碍,对血容量丧失或麻醉等引起的血管扩张的代偿能力差,术中易发生低血压及休克。
4.易发生感染并发症 糖尿病病人,感染性并发症发生率高,如切口感染、腹腔脓肿、肺部感染、泌尿系感染乃至全身性感染等。这是由于:①高血糖利于细菌生长。②由于白细胞糖代谢紊乱,致其趋化功能、吞噬及杀菌能力降低。③糖尿病病人体内蛋白合成减少,分解加速,使免疫球蛋白、补体等生成减少。
5.组织愈合能力差 此与糖尿病病人物质代谢紊乱有关。组织愈合能力差,不仅表现为手术切口愈合不良或延迟,更重要的是涉及体腔内手术脏器吻合(或缝合)后由于愈合不良而发生相关并发症,如消化道吻合口瘘,支气管残端瘘等。
三、围手术期血糖的控制
在围手术期,最理想的是将血糖控制在6.1~10mmol/L;血糖4.5~14.0mmol/L是围手术期“可允许范围”;而3.0~20.0mmol/L是围手术期“最大允许范围”,低于或高于此值均具有危险性。
1.术前 择期手术,术前应将血糖控制在6.1~10mmol/L,尿糖(-)~(+),无酮症及酸中毒。
(1)术前数日,停用口服降糖药及中效(或长效)胰岛素,改用正规胰岛素(Regular insulin,RI):口服降糖药、中效或长效胰岛素的半寿期及作用时间见表3-9。究竟术前几天停药,取决于具体药物的半寿期及作用时间,如氯磺丙脲、NPH、PZI均应在术前5d停药,停药2~3d后改用RI。
表3-9 口服降糖药及中(或长)效胰岛素的半寿期与作用时间

(2)根据血糖浓度及4次/d尿糖测定(餐前及睡前),皮下注射正规胰岛素(RI);尿糖(-)~(+)不用RI,(+)~(++)者4U,(++)~(+++)者8U,(+++)~(++++)者12U,定期复查血糖,据血糖值调整胰岛素用量。
2.术中 手术当天清晨(6Am)测定空腹血糖,继以缓慢静脉滴注5%葡萄糖溶液,以防术前禁饮食过久引起的低血糖。根据6Am空腹血糖值,将相应剂量之RI加入5%葡萄糖500m L中(即配制RI-5%葡萄糖溶液),见表3-10。于手术开始时以80~90m L/h速率静脉滴注,每2h监测血糖1次,并据监测血糖值调整RI-5%葡萄糖液滴注速率或调整RI的剂量,使血糖控制在“理想范围”或“允许范围”。
表3-10 静脉滴注RI控制血糖的方案

3.术后 每6h监测血糖1次,据测定值酌情继续滴注RI-5%葡萄糖溶液,使血糖控制在6.1~14mmol/L之间。其持续时间决定于手术类型及所引起应激状态的时间长短,腹腔大手术约需持续3 ~4d。待病情稳定,胃肠功能恢复,可改用皮下注射胰岛素或口服降糖药。
需急诊手术的糖尿病人,据血糖值按表3-9所示方案滴注RI-5%葡萄糖溶液,使血糖降至术前要求的“理想范围”或“允许范围”。
四、围手术期糖尿病危象的处理
糖尿病危象(Diabetic crisis)是糖尿病常见的急性严重代谢并发症,主要有:①糖尿病酮症酸中毒;②非酮症高血糖-高渗性昏迷;③低血糖昏迷等,围手术期皆可能发生,需紧急处理。
(一)糖尿病酮症酸中毒(DKA)
是1型糖尿病病人体内胰岛素绝对或相对严重缺乏所引起的常见代谢紊乱并发症。围手术期引起DKA常见的原因为:①胰岛素减量过快或突然停止。②手术创伤术后感染的应激反应,胰岛素相对不足。
体内胰岛素绝对或相对严重不足,导致一系列病理生理改变:①高血糖症:当血糖>15~20mmol/L,则引起渗透性利尿,过多的尿量使水、K+、Na+丢失,血容量下降,血液浓缩。②高酮血症及酮尿:由于脂肪分解加速,大量脂肪酸经肝脏β氧化产生乙酰乙酸和β-羟丁酸,后者经脱羟生成丙酮(三者总称为酮体),酮体产生量超过肝外组织的氧化限度,则出现高酮血症及酮尿。③代谢性酸中毒:乙酰乙酸和β-羟丁酸是强有机酸,诱发代谢性酸中毒,由于呼吸性代偿,呼吸深而快,大量酮体从肺呼出,呼气呈酮味。④中枢神经功能障碍:意识迟钝、嗜睡以致昏迷,系由于脑缺氧、失水及酮中毒等多因素引起。
1.诊断要点
(1)有上述某种或数种诱因。
(2)临床表现:恶心、呕吐、腹痛;多尿、脱水及血压下降乃至周围循环衰竭。呼吸深快,呼气酮味。意识障碍。
(3)实验室检查特征:血糖多为16.7~33.3mmol/L(300~600mg/d L),有时可更高;血酮体增高,严重者>4.8mmol/L(50mg/d L)。尿糖、尿酮强阳性;血pH值<7.3,重者可<7.1,[HCO3-]<15mmol/L;血Na+、Cl-降低,初期血K+正常或偏低,尿量减少后可偏高。血尿素氮升高。
2.治疗 治疗原则是:①快速扩容,稳定循环,保持足够尿量。②静脉给予足够剂量正规胰岛素(GI),纠正高血糖和高血酮症。③纠正电解质紊乱和酸中毒。④消除应激,控制感染。
(1)快速扩容:治疗开始2h内快速输注0.9%生理盐水1 000~2 000m L,如尿量>40m L/h,输液速率减慢,第1个24h输液总量可达4 000~8 000m L。及时查血糖,当血糖降至13.9mmol/L (250mg/d L)以下时,可换用5%葡萄糖盐水。老年人及心脏功能不全者,适当减慢输液速度,以防超载。
(2)正规胰岛素的应用:目前主张速效正规胰岛素小剂量疗法。可将正规胰岛素16~24单位加入500m L生理盐水,以125m L/h速率滴入,4h左右滴完,复查血糖,如血糖下降不明显,则加大胰岛素剂量或加快速率。当血糖降至11mmol/L以下,改用皮下注射。
(3)纠正电解质紊乱和酸中毒:其原则与基础外科相同。
(4)其他:控制感染,防治脑水肿等。
(二)非酮症高血糖-高渗性昏迷(NKHHC)
NKHHC是2型糖尿病的并发症,其临床特点为严重高血糖症,但不伴酮症酸中毒,高血钠,
血浆渗透压升高,极度脱水,肾前性氮质血症,意识障碍,甚至昏迷,有时伴癫痫发作。病死率达50%左右。
NKHHC的病因多为术前糖尿病被漏诊,或虽未被漏诊,但因某些诱因使糖尿病发展、恶化、
血糖迅速升高,而又未能作出及早处理。其诱因主要包括手术刺激及术后感染并发症造成的应激,补液不足或液体丢失(如利尿剂应用)造成血液浓缩,皮质激素应用,不恰当的肠外营养葡萄糖输入过多等。
上述诱因使血糖进一步升高。高血糖的渗透性利尿作用,造成大量失水、血容量下降以及继以细
胞内脱水;渗透性利尿使失水多于失盐,血液浓缩,导致高血钠及高血浆渗透压;因NKHHC病人血浆胰岛素水平的低下不如KDA者明显,尚能抑制脂肪的动员和分解,故不出现或仅有轻度酮症;脑细胞内脱水及大脑供血不足是导致意识障碍、昏迷的原因。总之,NKHHC的病理生理改变可归纳为“三高二低”,即高血糖、高血浆渗透压、高血钠以及低血容量和细胞内脱水。
NKHHC病人血糖多数>33mmol/L,尿糖强阳性;血浆渗透压增加,>320MOSM/L有诊断价值,多数>350MOSM/L,血浆渗透压可按公式计算:血浆渗透压=2×(Na++K+)mmol/L+血糖mmol/L+尿素氮mmol/L,正常值为280~300MOSM/L;血清钠增高,常>150mmol/L;血酮体不高,尿酮阴性或弱阳性;血pH值及[HCO3-]正常或轻度下降。
主要治疗方法(例如正规胰岛素的应用)与DKA相同,但应注意以下两点:①24h补液量按病人体重10%~15%计算,先快后慢;②一般情况下以补生理盐水为主,但如血糖>33mmol/L,血钠>150mmol/L则先给予0.45%氯化钠静脉输注,当血浆渗透压降至330MOSM/L时改用0.9%生理盐水。
(三)低血糖昏迷(hypoglycemia coma)
在围手术期要警惕低血糖发生。其原因主要是未停用口服降糖药及中效(或长效)胰岛素又过早应用了RI,禁饮食过久,RI用量过大。重度低血糖可造成脑及其他重要器官功能障碍,血糖<1.7mmol/L,则导致昏迷,故低血糖同样具有危险性。凡术中用RI控制血糖者,如全麻后未如期苏醒或苏醒后又陷入意识障碍者,应立即暂停注RI,急查血糖,根据血糖结果再决定是否继续滴注RI。
第五节 肝功能障碍病人的围手术期处理
伴有肝硬变、肝功能损害而需接受外科手术治疗的病人,由于肝脏的合成、解毒和代谢功能减弱,大大增加了手术的危险性。麻醉与手术必然要增加肝脏的负担,由于肝脏本已处于功能不全状态,如果手术的指征和时机选择不当,将导致肝功能进一步恶化,严重者发生术后肝功能衰竭,甚至死亡。本节介绍术前肝脏贮备功能的判断及肝功能障碍病人的围手术期处理。
一、术前肝脏贮备功能的判断
(一)肝脏贮备功能判断的传统标准
多年来临床一直沿用判断门脉高压症病人接受手术治疗危险的Child肝功能分级法(1964年)及其所派生出来的Pugh肝功能分级法和1983年我国所制订的肝功能分级法(表3-11)。
表3-11 Child分级法

Pugh则以“凝血酶原时间延长的秒数”取代了上表中的“营养状况”指标。并用5项指标总分来综合评定肝功能(见表3-12),较Child法更合理。
表3-12 Pugh肝功能分级法

1983年我国召开了门脉高压症专题讨论会,制定了我国统一的肝功能分级标准(见表3-13)。
表3-13 1983年武汉会议肝功能分级

上述肝功能分级,临床实践证明,其主要问题是对肝功能的实际状况估计偏高,不能准确预计增加肝功能负荷后实际的贮备能力。例如,按Child分级,A级病人作一般术前准备即可手术,B级应作好充分术前准备,改善肝功能及全身一般状况才能手术,C级为手术禁忌证。然而实际情况是,术前A级者,仅有50%病人术后肝功能保持良好,41%出现肝功能损害,而有9%者发生了肝功能衰竭。因此,传统的判断标准需赖其他检查方法补充与修订。
(二)判断肝脏贮备功能的新近方法
(1)靛青绿15min潴留率(Indocyanine-gree retain in 15minute ICGR15):由日本学者冈本英三(1987年)倡用。ICGR15<30%可行肝叶切除,30%~40%仅可行肝动脉结扎或肝段切除,>40%者不能耐受手术,其他腹腔手术可参照此标准判断。
(2)口服葡萄糖耐量试验(Oral glucose tolerance test,OGTT):OGTT血糖曲线反映肝细胞线粒体代谢状态和糖原合成能力。正常血糖曲线为抛物线型(P型),可以耐受肝切除术,如为直线(L型)则不能耐受任何手术。国内研究将P型进一步分为两个亚型:P1型指糖负荷后120min血糖值降至≤7.3mmol/L,预示肝贮备功能良好,可耐受任何手术。如血糖徘徊在7.3mmol/L以上,为P2型,预示肝贮备功能不足,不能耐受手术。
(3)胰高血糖素负荷试验(Glucagon load test,GLT):GLT是通过胰高血糖素与肝细胞受体结合激活腺苷酸环化酶,将ATP转化为C-AMP。GLT血浆中C-AMP浓度的高峰值与基础值之比(P/B)是检测肝细胞数量和ATP合成功能的敏感指标。P/B>20、10~20、<10可预测三个不同程度的贮备功能。
(4)预测肝切除术后肝衰可能性的多元回归方程式:Okamoto等选择17项肝功能指标对肝切除病人分析,发现年龄、ICGR 15、ICGR max(靛青绿最大清除率)和肝实质切除率(parenchymal hepatic reseeivon rate,PHRR)为判断肝贮备功能的敏感指标,并推导出一个预测肝切除术后出现肝衰可能性的多元回归方程式,即:
y=-110+0.94×PHRR+1.36×ICGR 15+1.17×年龄+5.94×ICGR max
![]()
该研究发现:y>50者术后均发生肝衰,因而提出凡y>50者,只能作局部性切除或肝动脉结扎术;y<50者术后均存活,而提出凡<50者可选择行肝叶切除术。
二、围手术期的处理原则
急性肝炎、活动性慢性肝炎是择期手术的禁忌证。慢性肝病(肝硬变、非活动性慢性肝炎)者,应据肝功损害及肝贮备功能状况选择手术时机:Child、Pugh A级和国内分级Ⅰ级者可施行腹部手术;B级和Ⅱ级者经积极术前准备肝功改善后,可施行一般腹部手术,但大型腹部手术仍应慎重;需施行肝叶切除者(如肝癌并存肝硬变),应考虑到肝实质切除率、术中肝门阻断等对肝贮备功能的额外不利影响,还需据其他方法(如Okamoto的多元回归方程式)综合判断肝贮备功能,确定肝叶切除的耐受能力和手术时机。
肝功能障碍病人的围手术期处理基本原则是:
(一)营养支持
肝功能障碍病人多存在程度不等的营养不良。合理的营养支持对促进肝细胞结构的恢复与再生,维护与改善肝功能以及改善全身营养状况,增进对手术的耐受能力均具重要意义。
胃肠消化、吸收功能尚好者,调整饮食结构即可,即给予高蛋白、高维生素、低脂及适量糖类的饮食。
食欲及消化吸收功能较差者,传统膳食进食不足,应辅以肠内营养支持——口服肠内营养制剂,如能全素、安素、百普素、爱伦多等。
消化、吸收功能障碍者,应给予部分肠外营养支持(详见本书第四章第九节)。
(二)提高血浆白蛋白水平
肝功能障碍病人血浆白蛋白水平降低,是由于肝脏合成蛋白的能力受损所致。因此,提高血浆白蛋白的根本措施仍在于合理的营养支持,促进肝细胞结构与功能的恢复。
只有在合理营养支持、提供足够的能量与营养基质的基础上,输注外源性白蛋白才能起到实际作用,否则所输注的白蛋白及其他的血液制品均将会被机体充当能量消耗。间断输注白蛋白的肠外营养支持,称之为“白蛋白强化的(肠外)营养支持”。
(三)改善凝血机制
有6种凝血因子在肝脏合成,即因子Ⅰ(纤维蛋白原)、Ⅱ(凝血酶原)及因子Ⅴ、Ⅶ、Ⅸ、Ⅹ,严重肝功能障碍时,它们呈集体性减少。在这6种因子中,有4种因子,即因子Ⅱ、Ⅶ、Ⅸ、Ⅹ等需要维生素K作为它们的合成原料,这4种因子称“维生素K依赖因子”。
伴有消化、吸收功能障碍的病人,存在程度不等的维生素K缺乏症,静脉补充维生素K是必要的。新鲜全血及新鲜血浆,保留了所有凝血因子的活性,新鲜冷冻血浆(Fresh frozm plasma,FFP)除保留了“维生素K依赖因子”的活性外,还保留了因子Ⅴ、Ⅷ的活性,浓缩凝血酶原复合物是含因子Ⅱ、Ⅶ、Ⅸ、Ⅹ的血液制品,它们均可用于矫正肝病病人凝血机制障碍。并存脾功能亢进其血小板计数<50×109~100×109/L者,手术前1~2d应输注新鲜全血或血小板。
(四)腹水的控制
通过“白蛋白强化的营养支持”提高血浆白蛋白水平,以提高血浆胶体渗透压;限制水与钠的摄入(或输入);合理地应用利尿剂。单独应用排钾性利尿剂(如双氢克尿噻)时要注意补钾。
(五)维护肝脏的血流灌注
术中及术后保持相对稳定血容量,避免与预防低血压及腹腔内脏血管收缩对肝脏血流灌注的不利影响。
采用第一肝门阻断切肝术时,常温下第一肝门阻断时间不要超过20min,如需阻断更长时间才能完成肝切除操作时,可采用间歇阻断,中间开放肝血流5min,拟行规则性半肝切除时,可先解剖第一肝门,分别游离、切断、结扎所属3个管道,再按解剖平面切肝。肝叶段切除,可采用单侧肝血流阻断术。
第六节 长期应用激素病人的围手术期处理
糖皮质类固醇激素(简称激素)具有抑制炎症、抗过敏等多种药理作用,目前广泛用于临床。1952年Fraser报告长期应用激素病人术后发生不可逆休克死亡,尸检发现肾上腺皮质萎缩、急性充血、出血。1961年Sampson、Winstone等证实,对这类病人手术时补充激素可避免肾上腺皮质危象的发生。目前,其围手术期处理已为临床医师重视。
一、长期应用激素对机体的影响
正常成人每日分泌皮质醇(Cortisol,hydrocortisone)20mg。当手术、创伤、感染等导致应激时,皮质醇分泌随之增加,其增加量与应激的程度呈正相关。如疝修补、阑尾切除等小手术,皮质醇分泌增至50~60mg/d,持续1d左右,而腹部大手术,则增至75~250mg/d,持续2~4d。
术前长期应用激素治疗的病人,体内激素水平因外源性激素的供给而增加,进而反馈地抑制了下丘脑的促皮质释放激素(corticotropin-releasing hormone,CRH)和垂体前叶的促肾上腺皮质激素(Adrenocorticotropic hormone,ACTH)的释放,即抑制了丘脑-垂体-肾上腺轴(hypothalamic-pituitary-adrenal axis,H-P-A),使肾上腺皮质失去正常分泌功能,甚至导致萎缩。
受抑制的程度与激素使用的量和持续时间有关,剂量越大,持续时间越长,距本次手术时间越近,肾上腺皮质应激能力受损越大。当给予外源性激素大于皮质醇20mg或其他肾上腺皮质类固醇药物的相当剂量(表3-14)超过1个月,体内糖皮质激素的合成与分泌就受到明显抑制,如在此时施行手术,又缺乏外源性激素补充时,其分泌量就不能满足机体应激的需要,则可发生急性肾上腺皮质衰竭。
表3-14 肾上腺皮质类固醇药物临床效应及等价剂量

二、围手术期补充激素的判断
适应证尚缺乏统一标准,综合国内外学者意见,适应证为:
(1)目前正在进行激素治疗者。
(2)术前9个月连续应用大于生理量激素超过1个月或激素总量相当于氢化考的松1.0g以上的皮质类固醇者:这一指征的制定是基于Byyny的研究,即超生理量外源性激素的应用超过1个月者,停药后,其垂体-肾上腺皮质的功能需9个月才能恢复正常。
(3)血清皮质醇值测定:正常值为50~250mg/L。在正常值者不能排除潜在的肾上腺皮质功能不全,凡有长期应用皮质激素史者,即使其值在正常范围,仍需作进一步检查。
(4)ACTH刺激试验:这是一客观判断肾上腺皮质功能安全而简便的方法,现多采用人工合成的ACTH异构体——Cosyntropin,静脉滴注或肌注25U,在注射前及注射后60min分别测定血浆皮质醇浓度,注射后较注射前皮质醇浓度升高值≥7μg%,或其值为注射前的2倍或其浓度≥18μg%者,均表示皮质功能正常。否则,应在围手术期补充激素。
(5)胰岛素低血糖试验:其原理是注射胰岛素后,血糖降低,导致ACTH分泌增加,进而刺激肾上腺分泌皮质醇增多。具体判断是:静脉滴注胰岛素0.15μ/kg体重,90min后血糖<40mg%而血浆皮质醇较注射前升高值>5μg%者为反应正常。反应不正常者应在围手术期补充激素。鉴于此试验可能招致严重低血糖,一般不用或严密观察下慎用。
三、围手术期补充激素的方案
围手术期激素补充量与持续的时间取决于术前已产生的H-P-A的抑制程度及本次疾病与手术将造成应激状态的严重程度。没有一个固定的方案适用于所有病人,下列方案可供临床选用,见表3-15、表3-16、表3-17、表3-18。
表3-15 择期手术小剂量给药法

注:此法适用于多数手术病人。
表3-16 择期手术大剂量给药法
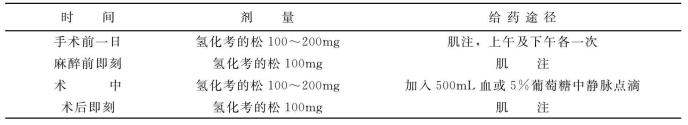
表3-17 急症手术病人给药法

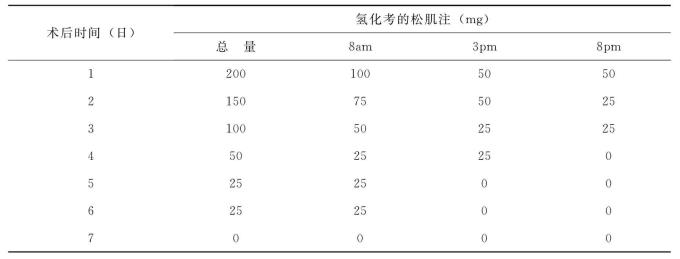
表3-18 对应用激素的病人术后激素给药法
(周亚魁)
参 考 文 献
1 周亚魁.普通外科常见全身并存病的围手术期处理./夏穗生主编.疑难普外科学.武汉:湖北科学技术出版社,2001:111~133
2 张秉钧.高血压病人外科手术时的几种问题.中国实用外科杂志,2000,20(4):196~197
3 郑斯聚.心肌缺血病人的围手术期处理.中国实用外科杂志,2000,20(4):197~199
4 徐葆元.糖尿病的病理生理.中华实用外科杂志,1999,19(3):132~333
5 黄洁夫.外科病人合并肝功能障碍的处理.中华实用外科杂志,1996,16(2):718~720
6 黑飞龙.糖尿病的围手术期处理(文献综述).国外医学外科分册,2000,27(2):71~75
7 Peters J,Tarnow J.The patient with cardiovascular diseases under going noncardiac surgery.In:Prys-Roberts C,Brown BR Jr(eds).International Practice of Anaesthesia.Oxford:Butterworth-Heinemann,1996,1(48):1~18
8 Fleisher LA,Barash PG.Preoperative cardiac evaluation for noncardiac surgery:a functional approach.Anesth Analg,1992,74(4):586
9 Tubau JF,Szlachcic J Meer L,et al.Left ventricular hypertrophy increases the risk of postoperative myocardial ischemia.Circulation,1990,82(suppl 4):163
10 Stone JG,Foex P,Sear JW,et al.Risks of myocardial ischemia during anaesthesia in treated and unteated hypertensive patients.Br J Anaeth,1988,61(2):675
11 Huber KC,Evans MA,Bresnahan JF,et al.Outcome Of noncardiac operation in patients with severe coronary arteral disease successfully treated preoperatively with angioplasty.Mayo Clin proc,1992,67(1):15
12 Mehta RH,Bossone E,Eagle KA.Perioperative cardiac risk assessment for noncardiac surgery.Cardiologia,1999,44(5):409
13 Eldridge AJ,Sear JW.Perioperative management of diabetic patients.Anaesthesia,1996,51 (1):45
14 Babineau JJ,Bothe AJ.General surgery considerations in the diabetic patients.Infect Dis Clin North Am,1995,9(1):183
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






