为了理解钢铁的氢脆,需要对金属中的氢固溶性质有所了解。首先考虑热平衡金属中的氢浓度。如前所述H2分子首先在金属表面物理吸附,解离成两个氢原子并稳定地化学吸附在金属表面,然后通过热活性化过程进入金属格点中。这个过程是可逆的,其反应可以用如(17-1)式表示:
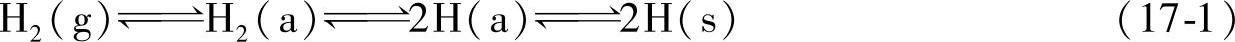
这里g、a、s分别表示气体氢、吸附氢以及固溶氢。
压力对于固相和液相平衡的影响极小,而对于含气相的反应来说则是重要因素。例如,在一定温度下,气体在金属中的最大溶解度将随气体的压力升高而显著增大,所以压力的变化使气体-金属二元相图形状发生重大变化。热平衡状态下氢气的压力P与氢在金属中的最大溶解度S([H]/[M])的关系服从Sieverts定律(指双原子气体):
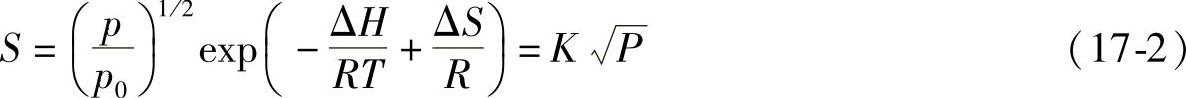
式中,K为常数,取决于温度和晶体结构。
当压力一定时,温度对溶解度的影响如下式所定:
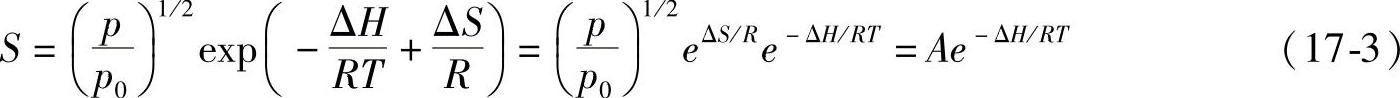
式中,A为常数;R为气体常数;T为温度。
因为△H和△R值可以从表17-1中获得[1],由此可以计算出在室温附近0.1MPa氢气压力下的平衡氢固溶浓度为S≈5×10-8,非常微量。
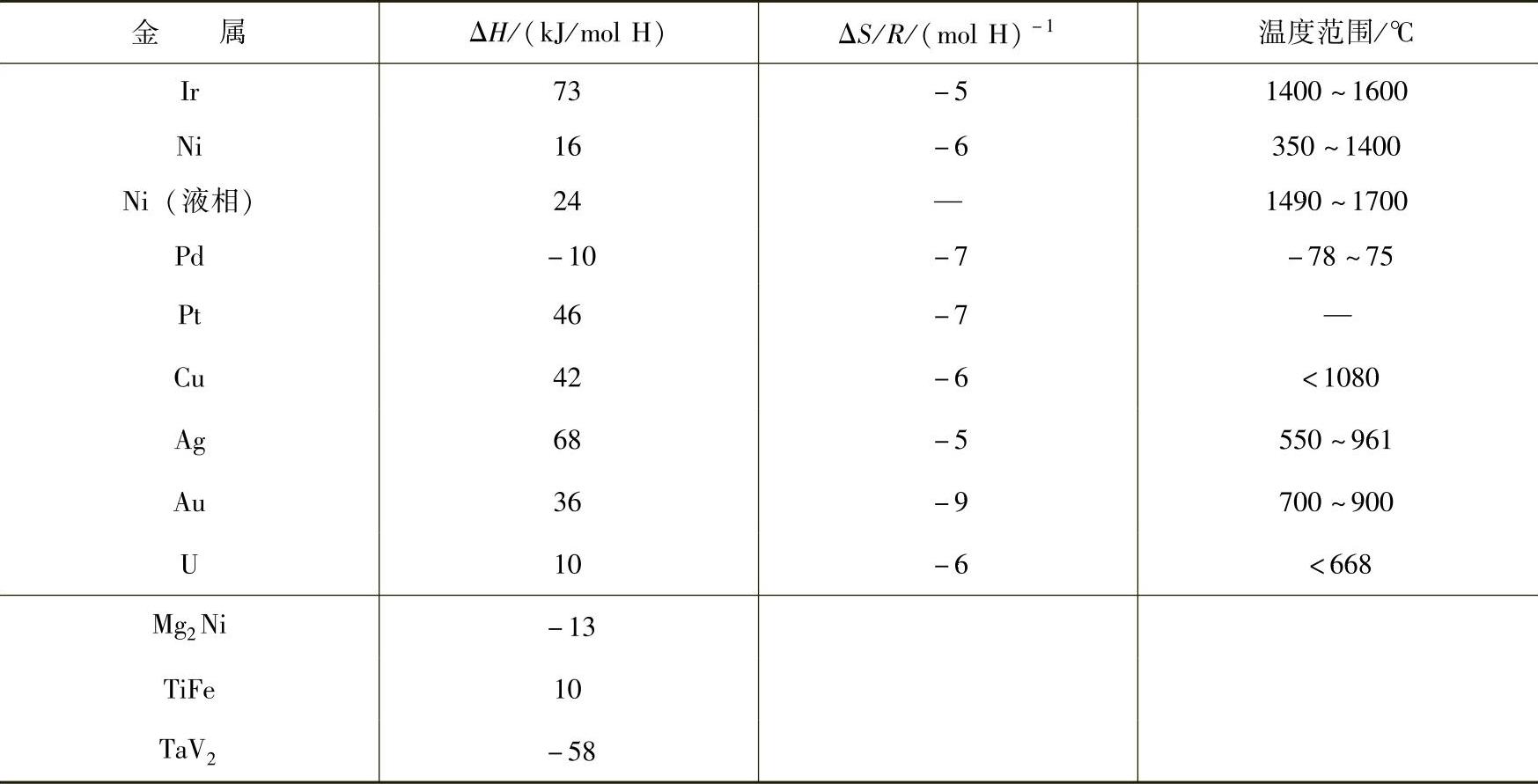
表17-1 氢在金属中的固溶热和固溶焓
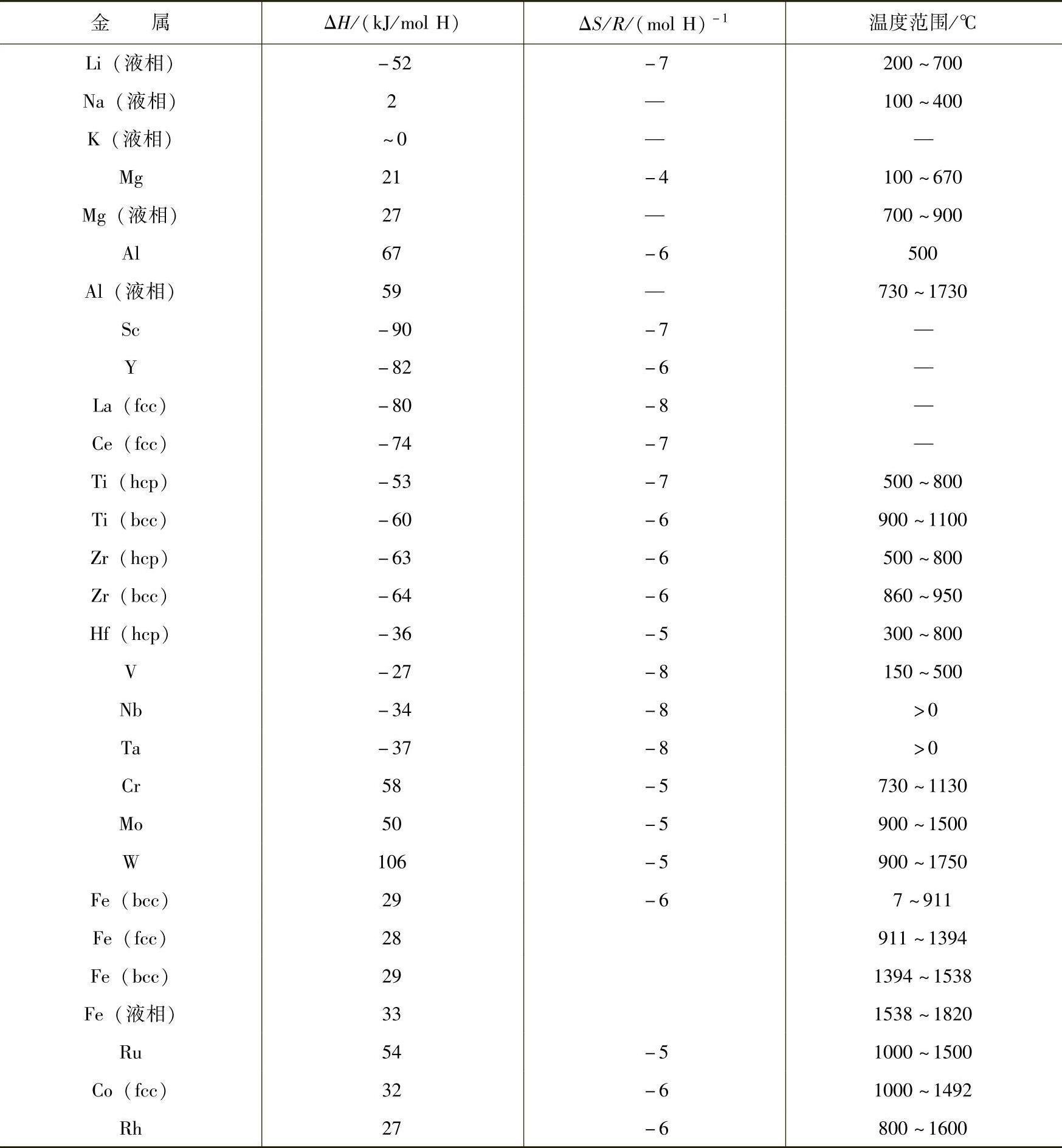
(续)
与气体状态加氢不同,在电镀或酸洗过程中会直接产生活性的氢原子,其中一部分以氢气的形式逸出,另一部分直接进入样品内部。由于不需要氢分子解离过程,而且活性的氢原子浓度远大于气体状态氢分子吸附和解离成原子的浓度,所以充氢速率要快很多。在一些氢气加热加压难以充氢的情况下,在电解或酸洗过程中却很容易充氢,这也是为什么研究氢脆行为时充氢往往都是通过电解方法的原因。
图17-1是不同金属中固溶氢与压力的关系[2]。图17-2所示为氢的固容量与温度的变化关系,从图中可知金属发生相变时,氢的溶解度将发生显著的变化。氢在液体金属中的溶解度要比固体中的溶解度大很多。如果溶有大量氢的金属液体进行结晶,将有大量氢气被析出,析出的氢气将成为气泡逃逸出金属或被保留在金属内部成为气泡。
 (https://www.daowen.com)
(https://www.daowen.com)
图17-1 压力对H2在固态金属中最大溶解度的影响
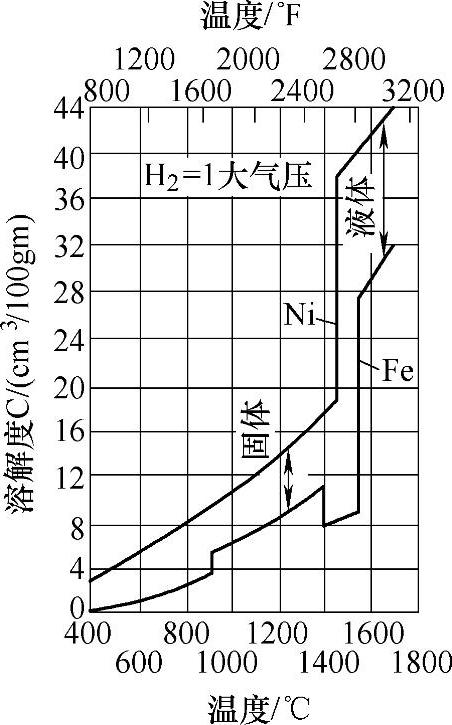
图17-2 温度对H2在固态与液态Ni和Fe中的溶解度的影响
图17-3是1个大气压氢气下的纯铁的氢固溶浓度随温度的变化。一般认为α-Fe中固溶的氢原子占据bcc晶格中四面体间隙中(T site),从而引起周围的铁点阵变形和体积膨胀。体积膨胀为2.0×10-6m3/mol氢或3.3×10-6nm3/氢原子,大体与其他金属中的氢固溶引起的膨胀相当。
如果晶体受外力或内应力的作用,应力场将与固溶氢原子引起的局部应变发生弹性相互作用,从而产生势场分布变化,形成对氢原子有势场梯度的环境,从而引起氢原子在晶体中的重新分布。由此,氢会在空位、位错、界面、析出物等地方偏析,其浓度往往比平衡时的浓度大很多。位错附近富集的固溶氢原子会对位错-位错之间以及位错与其他类型固溶杂质原子(C、N等)产生屏蔽作用,这也是一种解释铁的强度因氢的固溶而下降的原因,但这一点还没有得到实验的支持。
氢与位错的相互作用在塑性变形过程中尤为突出。图17-4是不同纯度的铁在充氢前后的应力-应变曲线[3]。从1%应变处看,高纯度的充氢样品(A、B)比没有充氢的样品(A′、B′)形变应力减小很多,这也被称为是氢固溶软化。而纯度低的充氢的样品(D)比没有充氢的样品(D)的强度提高,成为氢固溶硬化。图17-5是高纯度Fe吸放氢前后样品在不同温度下的应力-应变曲线。200K以上温度显示氢固溶软化,190K以下显示氢固溶硬化和脆化[3]。
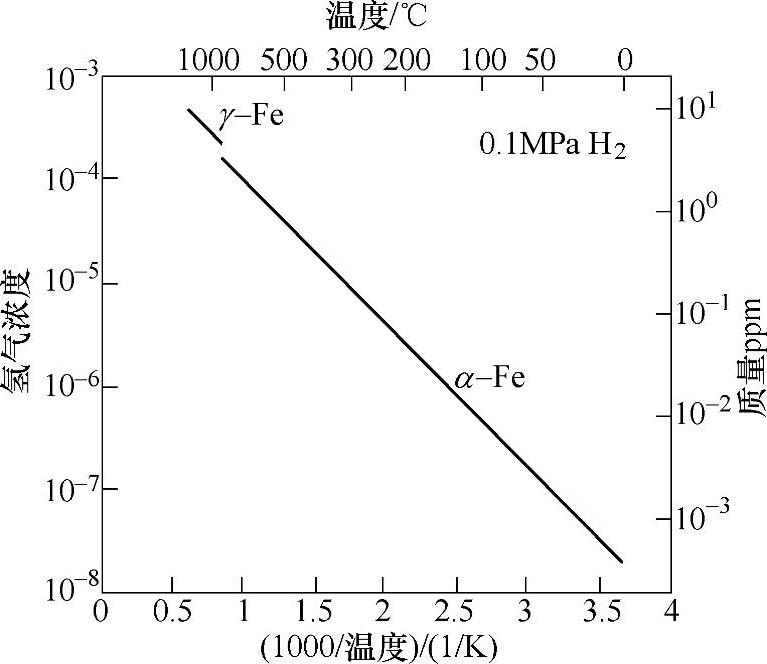
图17-3 一个大气压下纯铁的氢固溶浓度的温度变化

图17-4 不同纯度Fe在200K温度下的拉伸性质以及充氢的影响
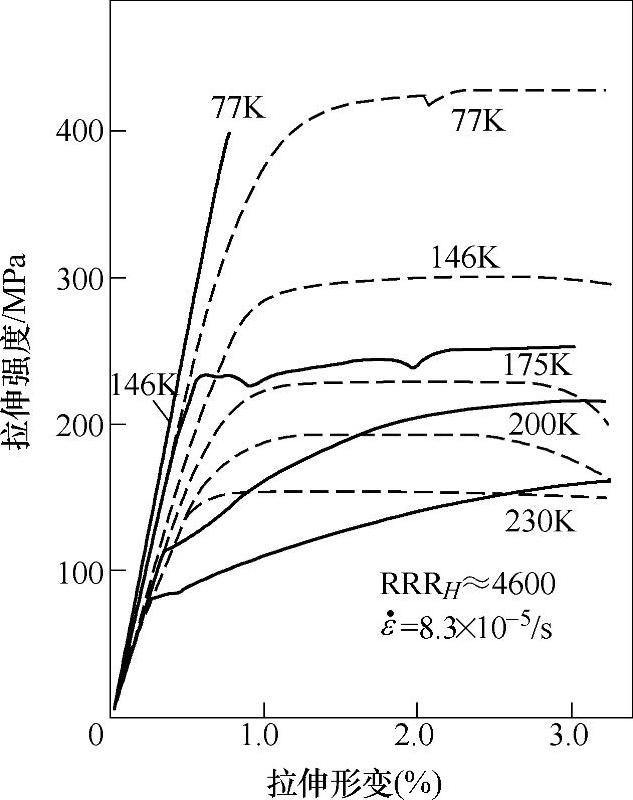
图17-5 高纯度Fe的应力-应变曲线以及氢气吸收和温度的影响
图17-6是不锈钢在氩气环境和氢气环境下拉伸断裂断口比较[4]。氩气气氛下样品有明显的变形引起的缩颈现象,而氢气环境下是脆性断裂。

图17-6 SUS316不锈钢在70MPa的氩气以及氢气环境下拉伸断裂样品照片
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






