各种金属Al氢化物的晶体结构参数已归纳于表9-3中。
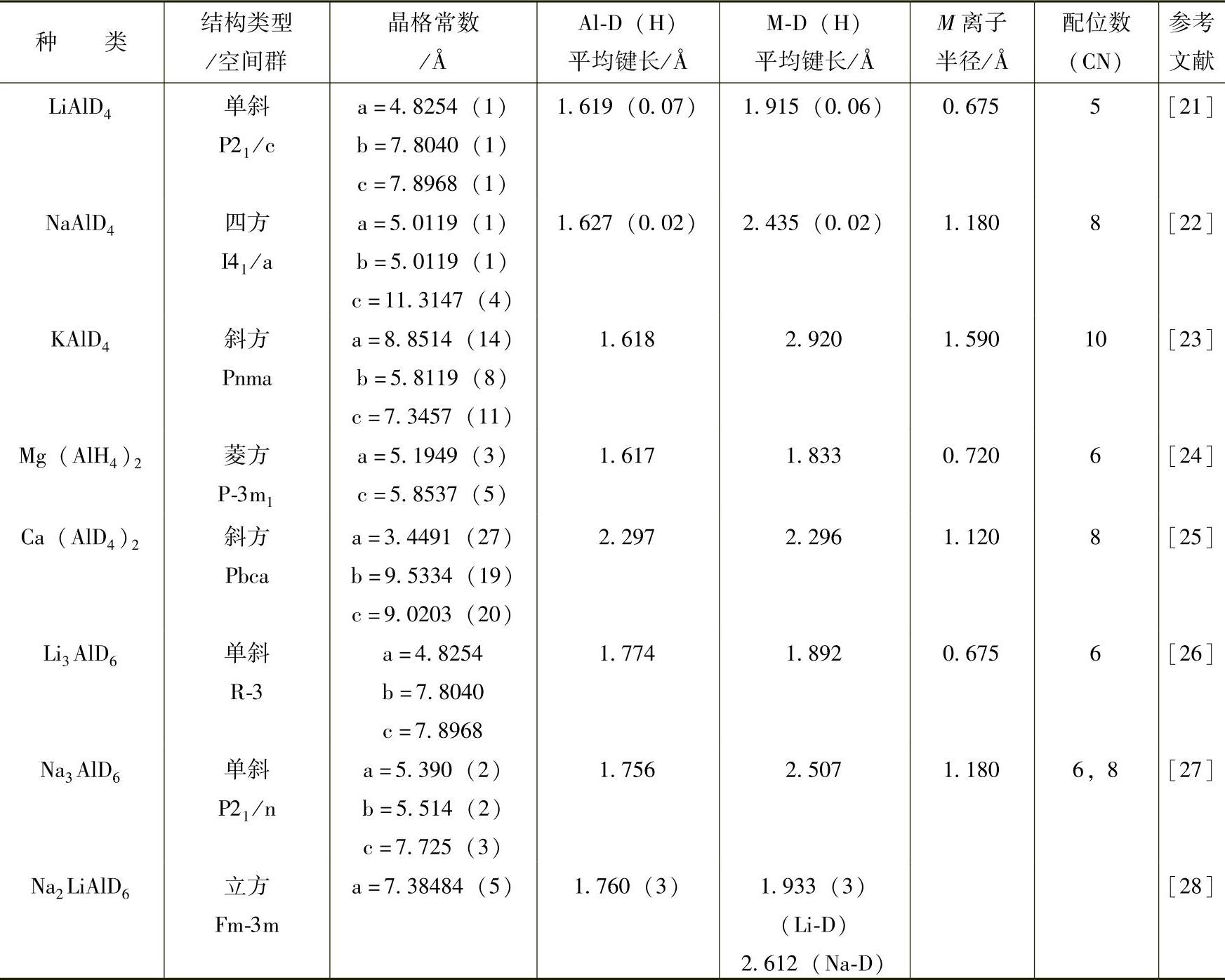
表9-3 常温下,配位Al氢化物MAlH4(或MAlD4)和M3AlH6(或M3AlD6)(M为金属原子)的晶体结构参数
碱金属Al氢化物的晶体结构示意图如图9-4所示,相关结构参数见表9-3。LiAlD4属于单斜晶系,空间群为P21/c[21]。Li+由周围由5个孤立的[AlD4]-四面体围绕,以三角双锥形式配位,如图9-4所示。
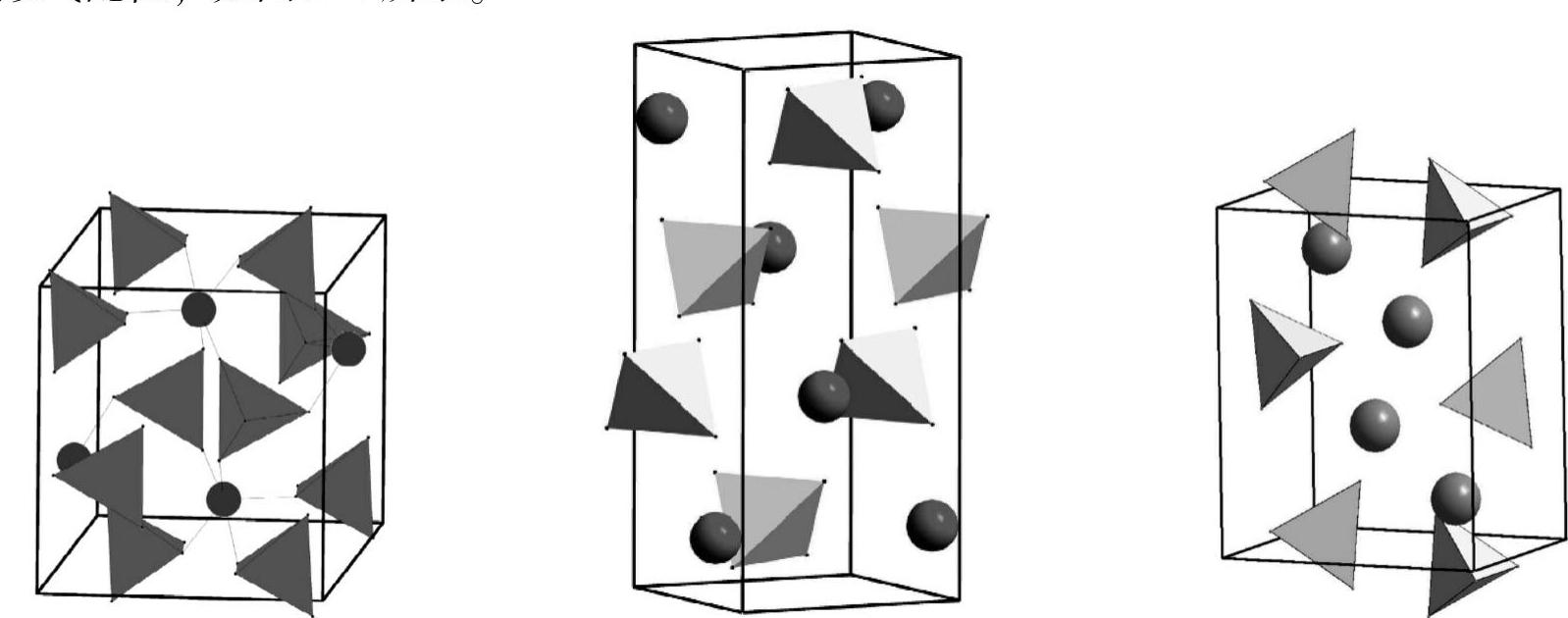
图9-4 MAlD4(M从左往右分别为Li、Na、K)的晶体结构[21-23]
注:四面体表示[AlH4]-,圆球表示M+。
NaAlD4的空间群为I41/a,具有体心四方结构[22]。每个Na+周围由最近邻的8个孤立[AlH4]-围绕,形成一个扭曲的反四方棱柱的空间构型。
KAlD4具有BaSO4型结构,空间群为Pnma[23],每个K+由邻近的7个[AlD4]-四面体围绕,并与这7个[AlD4]-四面体的10个D原子成键。
随着碱金属阳离子半径的增大(如Li+<Na+<K+),其配位数逐渐增加,导致LiAlD4、NaAlD4和KAlD4具有不同的晶体结构[24]。另外,LiAlD4、NaAlD4和KAlD4在结构上还存在诸多的相似之处;如,晶胞中都包含近似理想结构的[AlD4]-正四面体,[AlD4]-四面体的大小接近。
Mg(AlH4)2具有P-3m1空间群,由层状排列的[AlH4]-四面体构成,每个[AlH4]-离子周围由相邻的6个Mg2+围绕,形成一个扭曲的八面体[24],如图9-5所示。另一方面,Mg2+的配位数为6,与相邻的6个氢原子组成一个MgH6八面体。
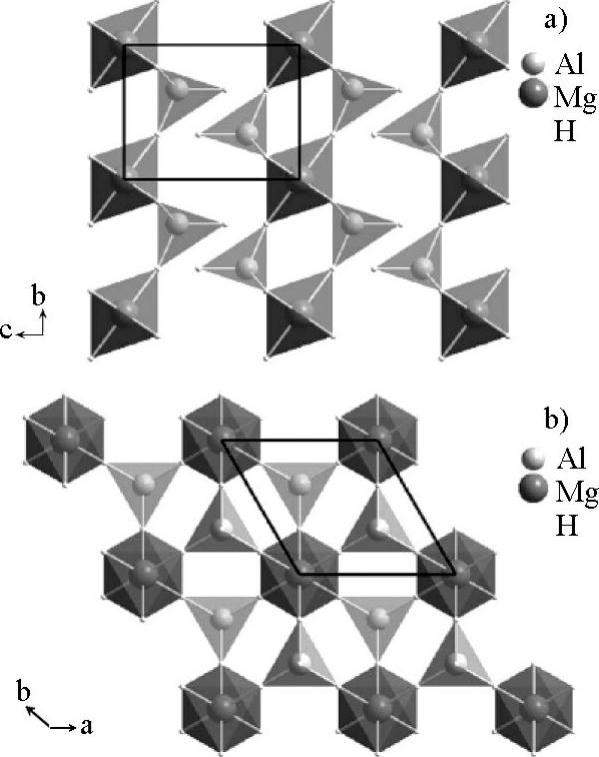
图9-5 Mg(AlH4)2的晶体结构[24]
a)沿着a轴方向的结构视图 b)沿着c轴方向的结构视图(https://www.daowen.com)
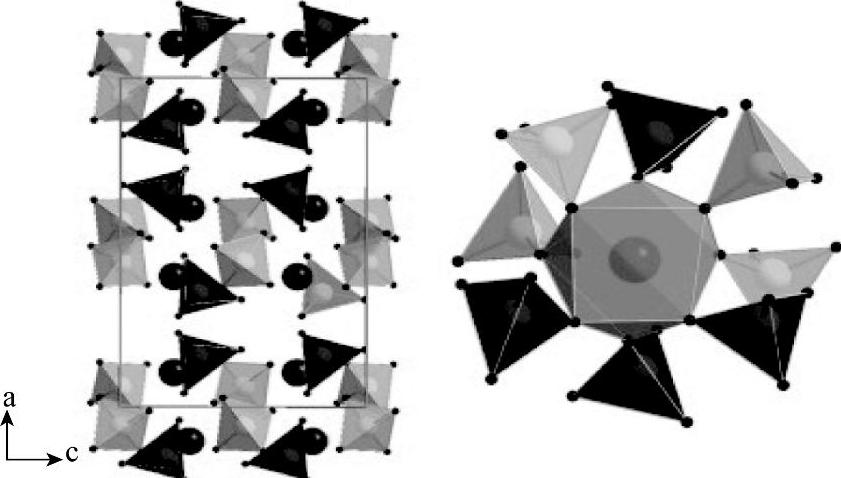
图9-6 左图为Ca(AlD4)2的晶体结构(沿b轴方向视图)[25];右图为Ca与8个[AlH4]-四面体形成的正方反棱柱型配位体
注:Ca(AlD4)2晶胞中有两种类型[AlD4]-四面体,分别为Al1D4(黑色四面体)和Al2D4(灰色四面体);圆球代表Ca原子。
Ca(AlD4)2属于斜方晶系,具有Ca(BF4)2型结构(见图9-6中左图),空间群为Pbca[25]。Ca(AlD4)2晶胞中,每个Ca2+周围由相邻的8个D原子环绕,形成一个正方反棱柱体(见图9-6右图),[AlH4]-四面体位于棱柱体的顶点。这种配位方式与NaAlD4相似[22],其原因是Ca2+(1.120Å)和Na+(1.180Å)的离子半径相近,配位数相同,均为8。
Na3AlH6属单斜晶系,空间群为P21/n[26]。晶胞是由孤立的[AlH6]3-八面体单元构成的一个扭曲fcc结构,Na+占据四面体和八面体间隙位置。
Li3AlD6的空间群为R-3,晶胞由孤立的[AlD6]3-八面体构成,[AlD6]3-之间由六配位的Li+连接,每个Li+与相邻的4个[AlD6]3-八面体中的6个H原子成(6个H对应2个八面体中的两个顶点和另外两个八面体的两条棱边)[27]。值得注意的是,如图9-7所示,Li3AlD6中Li+的配位数为6,而在Na3AlD6中,Na离子同时具有6配位和8配位[26],这种差别是由Li+和Na+的离子半径不同所造成。
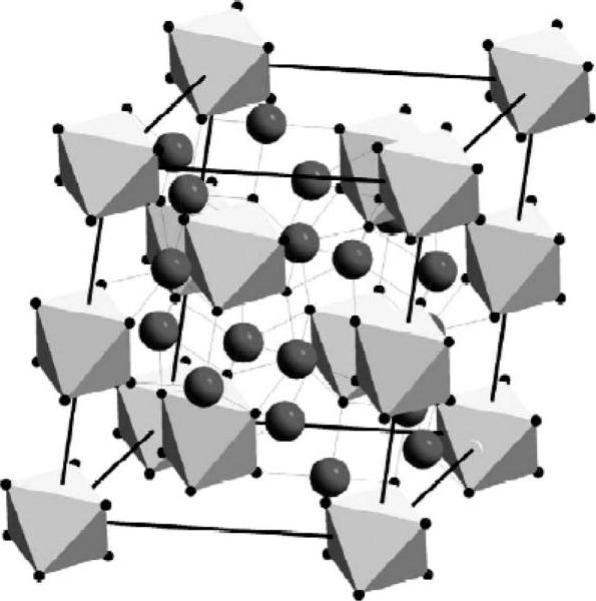
图9-7 Li3AlD6的晶体结构[27]
注:图中八面体表示[AlD6]3-,圆球表示Li+。
Na2LiAlD6具有立方钙钛矿结构(见图9-8),是由[AlD6]3-八面体单元组成变形fcc结构,Li+和Na+分别位于八面体间隙和四面体间隙位置;空间群为Fm-3m。虽然K+、Na+、Li+之间的离子半径不同,但K2NaAlD6具有与Na2LiAlD6相似的晶体结构[29],K+占据fcc晶胞的八面体间隙位置;而K2LiAlH6则不同[30],它具有六方菱形结构,空间群为R-3M。

图9-8 Na2LiAlD6的晶体结构[28]
注:图中黑色的八面体表示[AlD6]3-,浅色的八面体为LiD6,圆球表示Na+。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







