自1974年美国布鲁克海文国立研究所的Reilly和Wiswall发表了TiFe的储氢性质研究以来,Ti基AB型储氢合金受到了人们的重视[204]。TiFe合金储氢量较大,理论上室温下可吸收1.86wt%的氢气,大于传统的LaNi5等稀土系储氢材料的储氢量,且可以循环吸放氢,氢气平衡压在室温下约为0.3MPa,适于工业应用。此外,TiFe合金还具有资源丰富价格便宜的特点,而受到工业上的青睐,目前TiFe合金已经在一定程度上应用在了工业领域。但是TiFe合金也具有活化困难、抗杂质气体中毒能力差等问题。
Ti和Fe具有两种稳定的金属间化合物TiFe和TiFe2,其中只有TiFe可以在室温下可逆地吸放氢。TiFe与氢气反应可以生成正方晶系的TiFeH1.04和立方晶系的TiFeH1.95。反应焓ΔH分别为-28kJ/mol和-31.4kJ/mol。TiFe合金的PCT曲线有两个平台,分别对应形成两种氢化物的相变反应。其中平衡压较低的一个平台代表TiFe合金吸氢转变为TiFeH1.04,平衡压较高的一个平台代表TiFeH1.04吸氢转变为TiFeH1.95。而当温度升高时,平衡压较高的平台逐渐变窄,当温度超过338K时,该平台逐渐消失,即此温度以上TiFeH1.04相与TiFeH1.95相不共存。此外,TiFe合金PCT曲线的滞后比较大。TiFe合金的化学计量比对其储氢性质有较大的影响,Ti/Fe原子比为1∶1形成TiFe合金最适合储氢。若Ti原子过量,则会在TiFe合金中形成室温下稳定的氢化钛相,影响其室温储氢性质。若Fe原子过量,则会在TiFe合金中形成不吸氢的TiFe2相,减少体系的储氢量。
TiFe合金具有活化困难的缺点,需要在673K以上、5MPa氢气的条件下反复几十次吸放氢循环才能完全被活化。且合金对杂质气体非常敏感,氢气中氧的含量达到0.01%时,或CO含量达到0.03%时,合金再经过几次循环以后就会因为中毒而活性大大下降[205,206]。
TiFe合金的储氢性能的改善,一是通过添加其他金属成分[207-214],如Cr、Mn、Ni、Co、Cu、V、Nb、Al、Be、Mo等取代部分Fe元素或Ti元素,形成三元或多元合金,一是对TiFe合金进行表面处理[215],或采用机械合金化的方法合成材料。一般认为,通过添加过渡金属成分而在TiFe合金表面形成少量的第二相合金,对改善合金的活化性能起到主要作用。同时,取代金属可以降低TiFe合金吸放氢的平衡压力,减少吸放氢压力的滞后现象,并有稳定β相氢化物的作用,其稳定顺序为Cr>Mn>Ni>Co>Fe[207]。而在TiFe合金中添加Mm等稀土元素成分,弥散在合金中细小的Mm颗粒在室温下很容易吸氢发生体积膨胀,是TiFe合金产生大量的微裂纹,增加了氢气进入合金的通道,可以提高体系的活化性能[216,217]。几种Ti-Fe基储氢合金的性能如表8-12所示。(https://www.daowen.com)
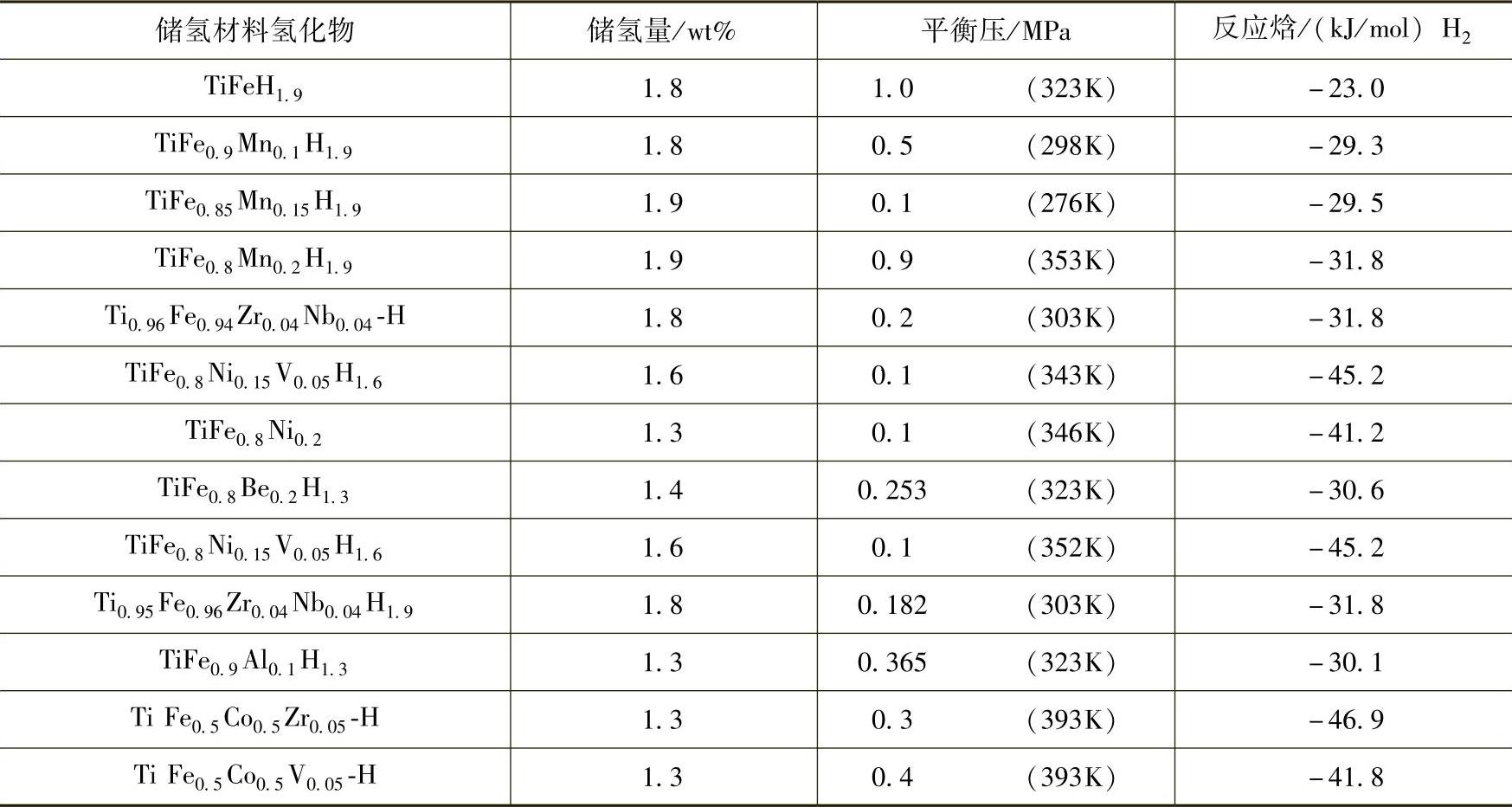
表8-12 几种Ti-Fe基储氢合金的性能
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






