储氢合金研究历史上,Libowitz等人于1958年首次报道了金属合金氢化物ZrNiH3[1]。20世纪60~70年代,美国布鲁克海文国家实验室以及荷兰的飞利浦公司相继开发出了La-Ni5-H、TiFe-H、ZrMn2-H、Mg2Ni-H金属合金-氢化物体系。自此以后,储氢合金的研究进入了全面发展的局面,世界上各个国家的众多研究机构开发出了多种类型的储氢合金体系。
简单来说,储氢合金AmBn由两大类元素组成,A元素一般容易与氢反应生成稳定的氢化物,并放出一定的热量。这些元素主要为ⅠA-ⅤB族金属,如Li、Na、Ca、Mg、Ti、V、Zr以及稀土元素等。B元素一般不与氢反应,但它与A形成合金后,能够催化氢的吸收和放出。这些元素主要是ⅢA金属和ⅥB-Ⅷ族过渡金属元素,如Cr、Mn、Ni、Co、Fe等。
表8-2列出了传统的几大类储氢合金。第一代储氢合金是以LaNi5为代表的AB5型稀土类合金。它是1969年荷兰飞利浦实验室[2]在研究永磁材料SmCo5时发现的,LaNi5的吸氢量为1.4wt%,室温下吸放氢容易,吸放氢平衡压差小,初期活化容易,抗毒化性能好。为了降低成本,一般使用稀土元素的混合物Mm(主要为La、Ce、Pr、Nb)来取代La,制得MmNi5。后来又使用Ca,Mn,Fe,Cu,Al等金属部分置换Mm或Ni,形成稀土类储氢合金。这类合金的致命缺点便是价格成本较高。
第二代储氢合金为AB型的FeTi和AB2型的ZrM2和TiM2等,FeTi储氢量为1.8wt%,具有储氢量大,热力学性能良好及原材料便宜等优点,但初期活化困难,需要在高温和高真空条件下进行预处理并经多次吸放氢循环后才能够正常地吸放氢,而且抗毒化能力差,容易被氢气中微量的O2、H2O、CO2等毒化。AB2型合金同样需要严格的活化过程。
第三代Mg2Ni储氢合金则具有资源丰富、重量轻、价格便宜、相对吸氢量大(3.6wt%)的特点,具有诱人的应用前景,但是其吸放氢温度高,活化困难,动力学性能差等因素制约了其实用化。
研究较多的储氢合金还包括钒基等体心立方(bcc)结构固溶体储氢合金[3]等。V可以在常温常压下吸收和放出氢。与氢反应主要有两种氢化物,即VH以及VH2。但是VH的放氢平台比较低,导致一般吸放氢过程中,真正可以有效使用的吸放氢量较低。此类材料的缺点是需要经过严格的活化过程,而且动力学性能一般。(https://www.daowen.com)
其他储氢合金类型还包括AB3(如GdFe3,NdCo3)、A2B7、A6B23、A2B17(如La2 Mg17)、A3B、A17B12(如Mg17Al12)等[4]。
表8-2 主要传统储氢合金种类[5]
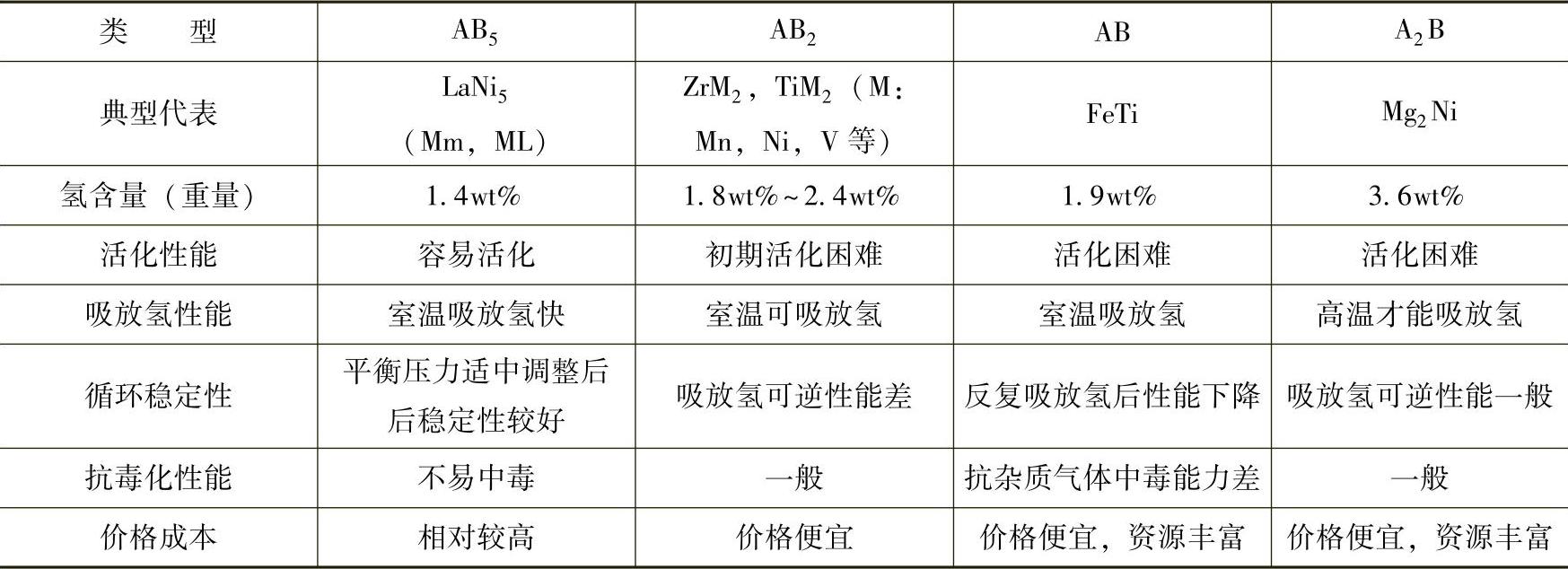
传统的储氢合金都有一个致命的缺陷,便是其有限的吸氢量。从表8-2中可以看出,这几大类传统储氢合金中,具有最大吸氢量的便是Mg2Ni,但也只有3.6wt%,这与美国能源部所制定的2015年氢燃料汽车5.5wt%的体系重量要求还有很大的距离。最近,储氢材料发展出了NaAlH4、LiAlH4、LiBH4、LixN-H等吸氢化合物体系,从传统储氢合金到这几类储氢化合物体系,一个明显的提高便是其理论吸氢量。但是,这几种储氢体系离真正的实用化则还有很远的距离,它们在吸放氢所需的条件以及循环反复性等困难使得其应用还需要进行更多的研究改进过程。
储氢合金目前一个重要的应用方向便是作为镍-金属氢化物(Ni-MH)电池的负极材料。在20世纪的70年代,科学家们便发现LaNi5和TiNi系的储氢合金具有电池负极储氢能力。最初的镍氢电池的大规模开发是在80年代以后,1984年荷兰飞利浦公司、日本松下公司和国内外许多科研院所大力开展实用化储氢合金电极材料的研究。1990年,镍氢电池首先由日本开始商业化,以后的数年内席卷全球,成为了可以替代镍镉电池的新型电池。它与镍镉电池相比具有更高的能量密度,为镍镉电池的1.5~2倍。它的循环寿命也比镍镉电池长。它与镍镉电池的本质区别只是在于负极材料的不同。这种电池的电压和镍镉电池完全相同,为1.2V,因此它可以直接应用在使用镍镉电池的器件上。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





