
与抑制作用相反,一些酶促反应必须有其他适当物质存在时才能表现出酶的催化活性或提高其催化活力。这些能够提高酶活力、加速酶促反应进行的物质均称为激活剂或活化剂(activator)。酶的激活与酶原的激活不同,酶激活是使已具有活性的酶的活力增高,使活力由低变高;酶原激活是使本来无活性的酶原变成有活性的酶。
有些酶的激活剂是金属离子,如酵母磷酸葡萄糖激酶催化活力需要Mg2+激活,Mg2+和Zn2+对酵母磷酸葡萄糖变位酶具有激活作用,精氨酸酶需要Mn2+,羧肽酶需要Zn2+,解脂耶氏酵母(Yarrowia lipolytica)脂肪酶Lip2需要Ca2+。酶促反应过程中缺少这些离子时其反应速率缓慢,增加离子的浓度时反应速率加快,但是当这些离子超过一定的限度时反应速率反而开始下降。如酵母磷酸葡萄糖变位酶在无Mg2+存在的催化反应中其活力只有最高点的15%左右,Mg2+浓度在3mmol/L时酶活力最高。一般认为金属离子的激活作用是由于金属离子与酶结合,此结合物又与底物结合成三位一体的“酶—金属—底物”复合物,金属离子在其中起到了搭桥的作用,其存在更有利于底物同酶的催化区和底物结合区相结合,从而提高了酶的催化速率。
无机阴离子对酶的激活作用在实践中也较为常见。例如唾液淀粉酶的催化作用需要Cl-参与,Cl-、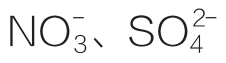 等为枯草芽孢杆菌淀粉酶的激活剂。无机阴离子的激活作用机制目前还不是特别清楚,推测可能是阴离子在这些反应过程中作为酶的必需因子,对酶的热稳定性起到保护作用。另外,一些小分子有机化合物如半胱氨酸、巯基乙醇、谷胱甘肽、维生素C等也可能是某些酶的激活剂;一些特殊的酶还需要其他蛋白质的存在来激活。(www.daowen.com)
等为枯草芽孢杆菌淀粉酶的激活剂。无机阴离子的激活作用机制目前还不是特别清楚,推测可能是阴离子在这些反应过程中作为酶的必需因子,对酶的热稳定性起到保护作用。另外,一些小分子有机化合物如半胱氨酸、巯基乙醇、谷胱甘肽、维生素C等也可能是某些酶的激活剂;一些特殊的酶还需要其他蛋白质的存在来激活。(www.daowen.com)
激活剂的作用是相对的,一种酶的激活剂对另一种酶来说可能没有作用,也可能是一种抑制剂。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






