【实验目的】
(1)掌握谷丙转氨酶作用原理,酶活力的定义和测定方法。
(2)熟悉转氨酶在代谢过程中的重要作用及其在临床诊断中的意义。
(3)了解肝脏疾病的相关标志物和人类疾病的酶学标志物。
【实验原理】
转氨基作用是指α-氨基酸的氨基转移到α-酮酸的酮基上,使原来的α-酮酸生成相应的α-氨基酸,而原来的α-氨基酸则转变为α-酮酸。反应可逆,实际反应方向取决于反应体系中4种反应物质的相对浓度。催化转氨基反应的酶称为转氨酶。转氨酶的种类很多,其中丙氨酸氨基转移酶(Alanine aminortransferase,ALT,又称谷丙转氨酶,Glutamic pyruvic transaminase,GPT)与医学关系密切。
ALT广泛存在于机体心、脑、肝、肾、横纹肌等各组织中,但含量不等。正常人血清中此酶活性很低。肝细胞中此酶活性极高,心肌细胞中此酶活性也很高。肝脏疾病(尤其是急性病毒性肝炎、急性肝细胞坏死等)或心肌梗死时,细胞膜通透性增高或细胞破坏,ALT释放入血,导致血中ALT活性显著升高。此外,阻塞性黄疸、胆管炎症、多发性肌炎时血清ALT活性也会有所增高。因此测定血清ALT活性对于某些疾病的诊断具有重要的参考价值。
血清中的丙氨酸氨基转移酶,在37 °C、pH 7.4的条件下,可催化基质液(底物)中的丙氨酸与α-酮戊二酸生成谷氨酸和丙酮酸:
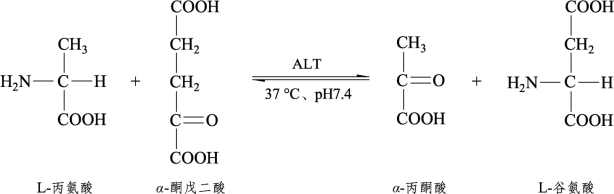
生成的丙酮酸可与起终止和显色作用的2,4-二硝基苯肼发生反应,生成丙酮酸-2,4-二硝基苯腙,进而在碱性环境中生成红棕色的苯腙硝醌化合物,其颜色深浅在一定范围内与丙酮酸的生成量,即与ALT活性的高低成正比关系。据此与同样处理的丙酮酸标准液相比较,便可算出或通过标准曲线查出血清中ALT的活性。
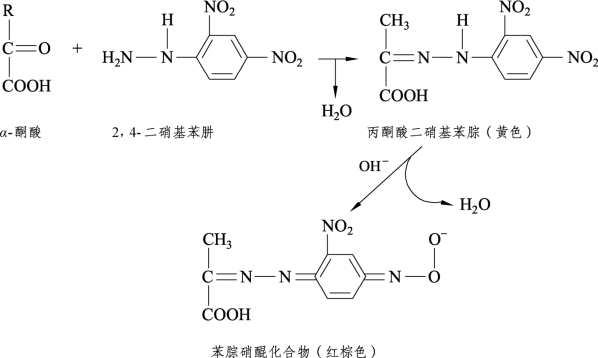
尽管基质液中余下的α-酮戊二酸同样可生成红棕色苯腙硝醌化合物而影响测定结果,但因其量不多,加之对505 nm的吸光度远不如丙酮酸生成的苯腙硝醌化合物强,尤其用标准曲线做测定时,所用的酶活性单位通过卡门氏分光光度速率法矫正,摒弃了赖氏法一些固有弊端,结果比其他比色法准确。国家卫健委临检中心建议国内无条件使用连续监测法的单位使用赖氏法。
【实验试剂与器材】
1. 实验试剂
(1)0.1 mol/L磷酸缓冲液(pH 7.4):① 0.1 mol/L磷酸氢二钠溶液:称取Na2HPO4 14.22 g或Na2HPO4·2H2O 17.8 g溶解于蒸馏水中,并稀释至1 000 mL,4 °C保存。② 0.1 mol/L磷酸二氢钾溶液:称取KH2PO4 13.61 g溶解于蒸馏水中,并稀释至1000 mL,4 °C保存。
取溶液①420 mL和溶液②80 mL混匀,即为0.1 mol/L pH 7.4的磷酸盐缓冲液。加氯仿数滴,4°C保存。
(2)2 mmol/L丙酮酸标准液:准确称取丙酮酸钠22 mg,溶于0.1 mol/L磷酸缓冲液(pH 7.4),定容至100 mL。丙酮酸钠不稳定,其纯度对于标准曲线有明显影响。如果丙酮酸钠颜色变黄或潮解,则不可用。此溶液应临用前新鲜配制,不能存放。
(3)基质液:精确称取α-酮戊二酸29.2 mg,D(L)-丙氨酸1.79 g,先溶于0.1 mol/L磷酸缓冲液(pH 7.4)50 mL中,用1 mol/L NaOH溶液调pH至7.4,再加此磷酸缓冲液至100 mL,4 °C保存,可加数滴氯仿以防腐。
(4)2,4-二硝基苯肼溶液:称取2,4-二硝基苯肼19.8 mg,溶于1 mol /L盐酸100 mL中,置于棕色瓶中保存,若用冰箱保存可稳定2个月。若有结晶析出,应重新配制。
(5)0.4 mol/L NaOH溶液。
2. 实验器材
恒温水浴锅、分光光度计、试管、移液管。
【实验步骤】
1. 标准曲线的绘制
取5支试管,编号后按表5-1加入相应试剂,并进行相应操作。
表5-1 标准曲线的制作(https://www.daowen.com)

混匀,室温放置10 min,于30 min内比色。采用波长505 nm,以蒸馏水调零,读取各管吸光度值。将各管吸光度值减去“1”号管吸光度,差值即为各标准管吸光度值。
以吸光度为纵坐标,对应的酶卡门氏活性单位为横坐标,绘制标准曲线。
2. 标本的测定
在测定前取适量的底物溶液和待测血清,37 °C水浴预温5 min后使用。取试管2支,按表5-2所列步骤操作。
表5-2 血清丙氨酸氨基转移酶活性的测定

混匀,室温放置10 min,在波长505 nm处以蒸馏水调零,读取各管吸光度值。测定管吸光度值减去对照管吸光度值,差值即为标本的吸光度值。在标准曲线上查得该值对应的ALT的卡门氏单位。
【参考值】
5~25卡门氏单位。1 mL血清能使A值下降0.001的转氨酶活性为1个卡门氏单位。
【注意事项】
(1)常温下标本不宜久置,采血4 h内应进行测定。
(2)严重脂血、黄疸、溶血和糖尿病酮症酸中毒病人血清标本可增加测定的吸光度,测定这类标本应做血清标本对照管。
(3)当标本的酶活力超过150卡门氏单位时,应将血清用0.145 mol/L氯化钠液稀释重做,其结果乘以稀释倍数。
(4)α-酮戊二酸、2,4 -二硝基苯肼是直接显色物,NaOH的浓度与显色深浅有关,因此它们的浓度必须很准确。
(5)丙酮酸标准液的浓度要求十分精确。由于丙酮酸开封后易变质为多聚丙酮酸,影响丙酮酸标准液的有效浓度而不易察觉,因此建议使用质量可靠的市售丙酮酸标准液。
(6)加入2,4-二硝基苯肼溶液后应充分混匀,使反应完全。
(7)保温温度、作用时间、加入试剂的方式方法、速度和时间间隔都应准确掌握。建议将试管架置37°C水浴中操作。从第一管加液混匀后开始计时,以一定时间间隔、加液方式和混匀方式依次向各管加入基质液;当第一管保温达到30 min时,即刻以加基质液相同的时间间隔和加液、混匀方式,依次又向各管加入2,4-二硝基苯肼,如是操作,直到做完本实验。
(8)每批试剂的空白管吸光度上下波动不应超过0.015 A,若有超出,应仔细检查试剂与仪器方面的问题。
【讨论与思考】
(1)测定血清中的谷丙转氨酶活性有何临床意义?
(2)为什么在制作标准曲线时要加入基质液?加入基质液的体积不同,对反应有无影响?
(3)在样品的采集时,为什么要避免溶血?溶血对谷丙转氨酶活性的测定有什么影响?
(4)测定血清谷丙转氨酶活性的过程中有哪些注意事项?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







