27,000,000,000,000,000,000个空气分子挤在1立方厘米的空间里,是不是特别的拥挤呢?其实一点儿也不拥挤,实际上,氧或氮的每个分子的直径大约是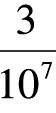 毫米,即是3×10-7毫米,我们不难计算出每个的体积为(
毫米,即是3×10-7毫米,我们不难计算出每个的体积为(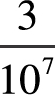 毫米)3=
毫米)3=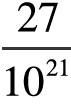 立方毫米。
立方毫米。
27×1018个分子总共的体积为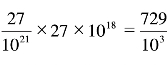 立方毫米。大约为1立方毫米,所以这些数量巨大的分子的总体积其实只占1立方厘米的千分之一。因此可见,这个1立方厘米的空间内并不拥挤,反而是很宽敞的,分子们可以在里面任意活动。物理学家们也曾告诉过我们,微小的分子们并不是静止不动的,而是一刻不停地运动着。
立方毫米。大约为1立方毫米,所以这些数量巨大的分子的总体积其实只占1立方厘米的千分之一。因此可见,这个1立方厘米的空间内并不拥挤,反而是很宽敞的,分子们可以在里面任意活动。物理学家们也曾告诉过我们,微小的分子们并不是静止不动的,而是一刻不停地运动着。
很多气体,比如氧、二氧化碳、氢、氮等在工业上都有很重要的用途,如果要储存大量的气体就需要体积巨大的容器,但是有时候并没有这样大的空间位置,这时工程师们就想到了好办法,将它们压缩之后保存。比如说,如果我们要储存1吨(1000千克)重的纯氮,在正常情况下需要占据800立方米的体积,也就是说,我们需要有8×10×10立方米大小的容器。而要存储1吨的纯氢,需要的容器体积更大,为10000立方米。
现实生活中,我们可不会这样存储气体,工程师们对它们进行了压缩,使这些分子之间的空距变小。但这并不是一件容易的事情,我们对气体施加了多大的力,气体就会施加同样大小的力在容器的内壁上。因此,这对容器的坚固性的要求很高,而且还要保证制成的容器不和储存的气体起化学反应而腐蚀容器。
现在,我们的工程师们已经可以将氢气压缩到原来体积的![]() 。在正常气压下体积为10000立方米的1吨重的纯氢,经过压缩之后,可以储存在大约9立方米体积的钢罐里,这个大小的对比可以看图60。
。在正常气压下体积为10000立方米的1吨重的纯氢,经过压缩之后,可以储存在大约9立方米体积的钢罐里,这个大小的对比可以看图60。
那么需要多大的压力才能使钢罐里的氢气缩小到原来的![]() 呢?物理知识告诉我们,气体体积要缩小多少倍,压力就要增加到多少倍。所以你会认为,这个问题的答案是1163倍。(https://www.daowen.com)
呢?物理知识告诉我们,气体体积要缩小多少倍,压力就要增加到多少倍。所以你会认为,这个问题的答案是1163倍。(https://www.daowen.com)
但事实并不是这样。钢罐中的氢气受到的压力为5000个大气压力,这就是说,压力不是要增加到1163倍而是要增加到5000倍。这是因为,你所知道的物理知识并不适用于压力很大的情况。
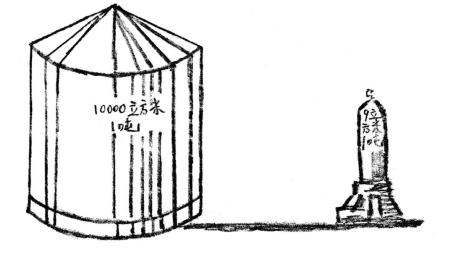
图60 一吨的氢气在大气压力下的体积(左),在5000气压下所占的体积(右)
例如,1吨重的氮气在正常大气压力下的体积为800立方米,气压增加为1000大气压时,体积缩小到1.7立方米,而继续增加气压,到5000个大气压时,氮气的体积并没有发生五倍的变化,仅缩小到了1.1立方米。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






