如图7-2所示,在高温环境下,TAN为10 mmol/L的ATS和NATS反应器内,乙酸均被快速转化为甲烷,未出现显著的迟滞。TAN为500 mmol/L时,ATS_N7反应器的产甲烷过程为:产甲烷迟滞期—缓慢产甲烷期—活跃产甲烷期—稳定期,其比产甲烷速率![]() 随时间的变化为“单峰”模式;而NATS_N7反应器的产甲烷过程则具有明显差异,可描述为:缓慢产甲烷期—前活跃产甲烷期—中间抑制期—后活跃产甲烷期—稳定期,其
随时间的变化为“单峰”模式;而NATS_N7反应器的产甲烷过程则具有明显差异,可描述为:缓慢产甲烷期—前活跃产甲烷期—中间抑制期—后活跃产甲烷期—稳定期,其![]() 随时间的变化呈现出“双峰”模式。
随时间的变化呈现出“双峰”模式。
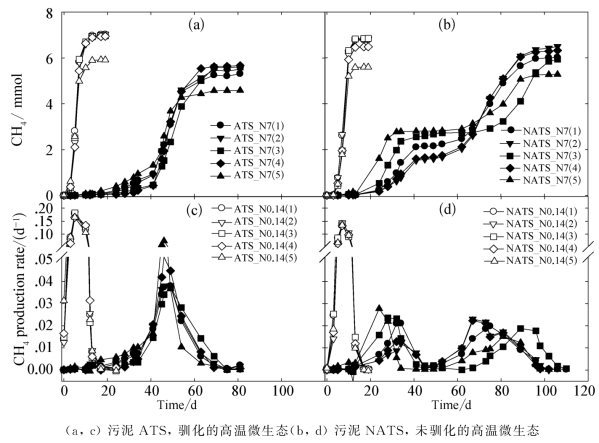
图7-2 各高温反应器的累计产甲烷量和比产甲烷速率
注:反应器编号含义:(1,2)采用未标记的CH3COOH作为底物;(3)和(4)分别采用[2-13C]CH3COOH和[1,2-13C]CH3COOH作为底物;(5)采用50%的[13C]NaHCO3作为缓冲体系。
氨胁迫下,NATS_N7反应器中,![]() 在两个活跃产甲烷期的峰值分别为0.021~0.028 d-1和0.015~0.023 d-1,均小于ATS_N7反应器的0.037~0.074 d-1。无氨胁迫时,NATS_N0.14和ATS_N0.14反应器中,
在两个活跃产甲烷期的峰值分别为0.021~0.028 d-1和0.015~0.023 d-1,均小于ATS_N7反应器的0.037~0.074 d-1。无氨胁迫时,NATS_N0.14和ATS_N0.14反应器中,![]() 的最大值则分别为0.132~0.144 d-1和0.164~0.182 d-1。可见,氨对产甲烷微生态的胁迫使其活力迅速降低。
的最大值则分别为0.132~0.144 d-1和0.164~0.182 d-1。可见,氨对产甲烷微生态的胁迫使其活力迅速降低。
TAN为500 mmol/L时,5个平行反应器中,活跃产甲烷期的出现呈现出一定的时间差异性,表明各反应器内的甲烷化功能微生物在不同时间先后被激活。这种差异在NATS_N7中表现得尤为显著。
在中温反应器内,乙酸的甲烷化化过程与高温下相似。TAN为357 mmol/L时,AMS_N5和NAMS_N5反应器中,![]() 随时间的变化分别呈现“单峰”和“双峰”模式(图7-3)。AMS_N5的产甲烷过程为:缓慢产甲烷期—迟滞期—活跃产甲烷期—稳定期,
随时间的变化分别呈现“单峰”和“双峰”模式(图7-3)。AMS_N5的产甲烷过程为:缓慢产甲烷期—迟滞期—活跃产甲烷期—稳定期,![]() 最大值为0.030~0.058 d-1;而NAMS_N5反应器则在起始阶段即进入前活跃产甲烷期,
最大值为0.030~0.058 d-1;而NAMS_N5反应器则在起始阶段即进入前活跃产甲烷期,![]() 最大值为0.033~0.045 d-1。
最大值为0.033~0.045 d-1。
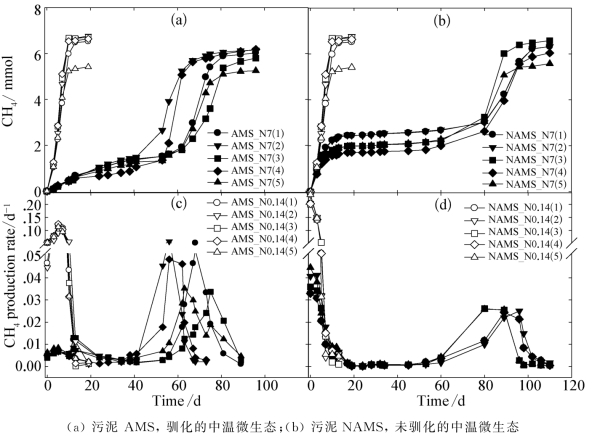
图7-3 各中温反应器的累计产甲烷量和比产甲烷速率(www.daowen.com)
注:反应器编号含义:(1,2)采用未标记的CH3COOH作为底物;(3)和(4)分别采用[2-13C]CH3COOH和[1,2-13C]CH3COOH作为底物;(5)采用50%的[13C]NaHCO3作为缓冲体系。
TAN为10 mmol/L时,NAMS反应器中,![]() 的最大值为0.201~0.239 d-1,高于AMS反应器的0.091~0.125 d-1。
的最大值为0.201~0.239 d-1,高于AMS反应器的0.091~0.125 d-1。
与高温微生态相比,在起始阶段,中温微生态具有更强的产甲烷活力,这种差异可能是由氨浓度、温度和微生物种群结构等的不同所导致。
比较驯化和未驯化微生态的产甲烷过程,可见,临界氨浓度下的预培养过程削弱了ATS和AMS中产甲烷菌的活力。将驯化后的ATS和AMS置入低浓度氨中,产甲烷菌的活力可迅速恢复;而若将其再次暴露于高浓度氨中,其活力则继续降低,经过一段时间(≤40 d)的驯化后,甲烷化活力又可重新恢复。
而未经驯化的NATS和NAMS暴露于高浓度氨中时,在起始阶段呈现了较高的产甲烷活力;但随着暴露时间的延长,其产甲烷活力逐渐消失;在经历了较长的迟滞期(10~40 d)后,其产甲烷活力再次恢复。
可见,驯化过程削弱了微生态的代谢活力,但也加速了胁迫状态下代谢功能的恢复进程。
图7-4显示了高温和中温反应器内乙酸浓度的变化。各反应器中,乙酸的降解与甲烷的产生过程一一对应。但是,对处于胁迫状态的ATS_N7和AMS_N5反应器而言,活跃产甲烷期到来之前,乙酸的消耗速率略大于甲烷的产生速率。在NATS_N7和NAMS_N5反应器的后活跃产甲烷期也存在类似的现象。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






