图6-2显示了未标记实验中,δ13CH4、δ13CO2和αc随时间的变化。
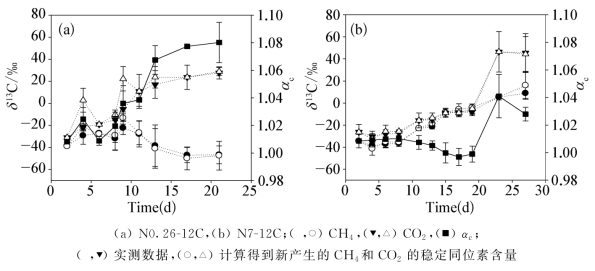
图6-2 未标记各反应器的δ13CH4,δ13CO2和αc
注:图中数据点为3平行实验的平均值,误差线表示标准偏差。
TAN 500 mmol/L反应器中,当乙酸浓度高于50 mmol/L时,气相的δ13CH4和δ13CO2值分别为-41.4‰~-34.5‰和-32.7‰~-26.4‰,此时的αc值为1.008~1.010。之后,随着乙酸浓度的降低,δ13CH4和δ13CO2值逐渐提高到0‰左右,αc值则逐渐降低到1.000左右。当乙酸浓度低于1 mmol/L时,δ13CO2值迅速增加,使得αc值提高到1.028~1.041。而δ13CH4值在反应末期的增加,可能与残留乙酸中13C的富集效应相关。(https://www.daowen.com)
TAN 19 mmol/L反应器中,当乙酸浓度高于3 mmol/L时,αc值波动于1.008~1.025之间。随着乙酸浓度继续降低,δ13CH4和δ13CO2值分别降低和升高,使得αc值增加到1.077~1.080,并未发生底物中13C富集导致δ13CH4增加的现象。在未添加乙酸的空白实验中,污泥内源呼吸产生少量的CH4和CO2,其αc值在不同氨浓度下均为1.019~1.030。
由此可见,在底物充足时,甲烷通过乙酸发酵型途径生成,TAN浓度对代谢途径无显著影响。随着乙酸浓度持续降低,并成为限制因素时,TAN 19 mmol/L下,主导代谢途径转向氢营养型;而在TAN 500 mmol/L下,氢营养型途径的贡献亦可能有所增加。这与产甲烷底物、乙酸和H2/CO2浓度的变化密切相关。
本实验未引入无机碳源,厌氧产气中的碳大部分来源于添加的乙酸。由于产甲烷反应中存在的同位素分馏效应(乙酸发酵型的分馏因子为1.007~1.027;氢营养型的分馏因子为1.045~1.080),13C在残留乙酸中逐渐富集。因此,气相中δ13CO2值的增加可能是由甲烷化过程中乙酸内13C的富集导致,也可能是CO2还原产甲烷反应中较高的分馏效应造成。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






