厌氧降解过程中甲烷生成途径的变化也可通过δ13CH4的变化进行表征。δ13CH4的值取决于底物(乙酸和CO2)的碳同位素比值和产甲烷反应的同位素分馏系数,计算公式(参考本书2.5.3.1章节)如下:
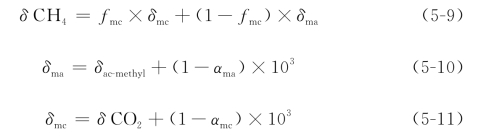
式中,δma为由乙酸甲基生成的CH4的稳定碳同位素丰度;δmc为CO2还原生成的CH4的稳定碳同位素丰度;δCH4为实际生成的CH4的稳定碳同位素丰度;δac-methyl为基质乙酸中甲基的稳定碳同位素丰度;δCO2为基质CO2中的碳同位素丰度;αma为乙酸型产甲烷途径的稳定碳同位素分馏效应因子;αmc为氢营养型产甲烷途径的稳定碳同位素分馏效应因子;fmc为氢营养型甲烷化途径对总产甲烷量的贡献。
根据以上公式计算两种产甲烷途径的比例,需要确定δac-methyl、δCO2、αma和αmc的值。由于实验仪器和测试方法的限制,本研究中未直接测试这些参数。但是,可以根据文献值和其他假设获得这些参数的大致取值,据此估算甲烷的生成途径。
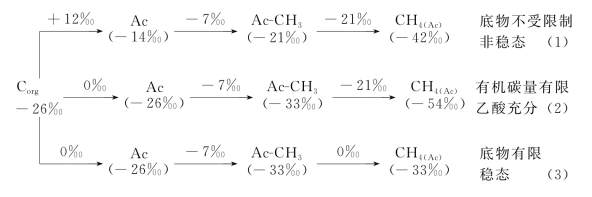
根据式(2-10),δma的取值由δac-methyl和αma决定。对乙酸整体稳定碳同位素比值的测试结果显示,δac值约为(-24.4±0.2)‰。如图5-6所示,δac-methyl的值通常比δac低7‰[144],因此δac-methyl值约为-31‰。在乙酸供给充分时,根据对纯培养产甲烷菌的研究结果,αma值的范围为1.007~1.027(附表A-1),此时,δma值的范围应为-38‰~-58‰。
 (https://www.daowen.com)
(https://www.daowen.com)
图5-6 有机物通过乙酸发酵型途径产甲烷的碳同位素分馏效应模型[139]
随着乙酸逐渐被降解,底物中的13C逐渐富集,产甲烷过程的同位素分馏效应逐渐降低。假设乙酸全部转化为甲烷,则累积CH4的δma值应为-31‰。故培养末期乙酸浓度降到极低水平时,δma值应≥-31‰。
相应的,δmc的取值决定于CO2中的13C同位素比值(δCO2)和氢营养型途径的稳定碳同位素分馏效应因子(αmc)。当乙酸浓度高于其限制浓度时,本研究中测得CO2的13C同位素比值为-20‰~-3‰。已有的对纯培养产甲烷菌的研究结果表明,αmc值的范围为1.045~1.080(附表A-1)。因此,CO2还原生成的CH4的13C同位素比值范围为-48‰~-100‰。
根据实测δCH4的变化可以看到,随着氨浓度的提高,氢营养型产甲烷途径的比重逐渐增加。由于本实验中乙酸为唯一的有机碳源,故氢营养型甲烷化反应的底物(H2/CO2)应主要来自乙酸氧化反应。产物中稳定碳同位素比值的变化,反映的是共生乙酸氧化和氢营养型甲烷化联合途径对乙酸降解过程的贡献。
低氨浓度(10 mmol/L TAN)下,中温和高温培养中,甲烷主要通过乙酸发酵型途径产生。较高氨浓度(高温214~357 mmol/L TAN;中温214 mmol/L TAN)下,乙酸发酵仍然为主导途径,但甲烷化反应逐渐受到抑制,表现为迟滞期的延长和产甲烷速率的降低;同时,δ13CH4值的降低和αmc的升高,表明乙酸氧化细菌和氢营养型产甲烷菌逐渐参与到乙酸向甲烷的转化中。氨浓度进一步升高(高温500 mmol/L TAN;中温357 mmol/L TAN)后,微生态开始变得不稳定,生境中各生态因子极小的差异都可能导致微生物菌群结构和功能向着两个方向发展,即:甲烷化过程可能在初期通过乙酸发酵型途径进行,而后逐渐向氢营养型途径转化;也可能在经历较长的迟滞期后,甲烷化过程通过氢营养型途径启动。在高氨浓度(高温643 mmol/L TAN;中温500~643 mmol/L TAN)下,乙酸发酵型甲烷化途径完全被抑制,在经历了长时间的迟滞期以后,共生乙酸氧化和氢营养型甲烷化串联反应开始活跃进行。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






