1.pH
最适宜pH范围pH是影响厌氧甲烷化过程的重要生态因子。参与厌氧消化过程的每种微生物可在一定的pH范围内活动,但它们的最适pH是不同的。产酸细菌能适应的pH范围较宽,一些产酸菌可以在pH为5.5~8.5的范围内生长良好,有些甚至可以在pH低于5.0的环境中生长,其最适宜的pH在6.5~7.5之间[16,32,33]。产甲烷菌的最适pH随甲烷菌种类的不同而有所差异,但大部分种群的生长最佳pH范围大致在6.8~7.5之间[7,81]。产甲烷菌对生长环境内pH变化的适应性较差,当pH过高(>8.0)或过低(<6.0)时,其代谢过程和生长繁殖就会受到抑制,导致反应器内有机酸积累、酸碱平衡失调,甚至运行失败[7,8]。
抑制机理pH过高或过低都会从生物化学和生物能量学的角度不同程度地损害细胞。为正常的生存和生长,微生物需要维持一定的细胞内pH。当生长环境的pH超出其可承受范围时,可通过细胞膜磷脂双分子层内的主动调节(如质子的被动运输)使细胞内维持适宜的pH水平,但这样的调节行为使得细胞维持生存的能量增加[82-84]。为在pH胁迫环境中生存,产甲烷菌需要通过质子泵维持适宜的内部pH,其消耗的能量由质子泵的工作速率以及泵出单位质子所需的能量决定,随着细胞内外pH差值的增加而增加。因而,微生物维持生存所需的能量随着环境pH与其最适宜pH的差距呈线性增加[85,86]。
微生物细胞对底物的吸收也受介质pH的影响。pH可极大程度地影响甲烷化底物,包括乙酸、CO2的存在状态。离子化的甲烷化底物很难扩散透过细胞膜,需要消耗更多能量进行被动运输或增加细胞膜的通透性以增强对底物的吸收,但这又会增加“pH渗漏效应”,需要质子泵增加工作速率进行补偿。因此,乙酸和碳酸在碱性环境下的强解离效应,限制了产甲烷菌在高pH环境下的生存[85]。
pH与VFAs、![]() 的相互作用,影响着游离有机酸和游离氨分子的浓度。以乙酸为例,pH过高时乙酸多以离子态存在,限制了产甲烷菌对底物的吸收;但pH过低时,游离乙酸分子的浓度大大增加,高浓度的游离乙酸透过细胞膜,进入细胞内部。如图1-2所示,细胞内为近中性环境,游离酸解离,增加了胞内的H+浓度,由此成为细胞膜上的质子原动力的解偶联剂而损害微生物[87-89]。碱性环境下大量存在的游离氨则可使蛋白质变性,易于透过细胞膜,剥夺细胞质中的H+以维持电离平衡。细胞为了维持质子浓度,以损失体内K+为代价,由外向内运输H+[90]。质子的不平衡或K+的损失降低了微生物活力,阻碍了细胞生长[26,91]。也有人认为,游离氨通过直接作用于产甲烷反应的酶系统而对其造成损害[92]。另外,氨向细胞内的渗透和解离增加了细胞维持生存所需的能量,则是从生物能量学观点提出的一种解释[85,93]。
的相互作用,影响着游离有机酸和游离氨分子的浓度。以乙酸为例,pH过高时乙酸多以离子态存在,限制了产甲烷菌对底物的吸收;但pH过低时,游离乙酸分子的浓度大大增加,高浓度的游离乙酸透过细胞膜,进入细胞内部。如图1-2所示,细胞内为近中性环境,游离酸解离,增加了胞内的H+浓度,由此成为细胞膜上的质子原动力的解偶联剂而损害微生物[87-89]。碱性环境下大量存在的游离氨则可使蛋白质变性,易于透过细胞膜,剥夺细胞质中的H+以维持电离平衡。细胞为了维持质子浓度,以损失体内K+为代价,由外向内运输H+[90]。质子的不平衡或K+的损失降低了微生物活力,阻碍了细胞生长[26,91]。也有人认为,游离氨通过直接作用于产甲烷反应的酶系统而对其造成损害[92]。另外,氨向细胞内的渗透和解离增加了细胞维持生存所需的能量,则是从生物能量学观点提出的一种解释[85,93]。
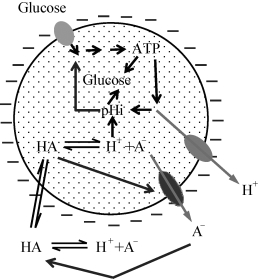
图1-2 微生物细胞对游离有机酸的胁迫响应模式[89]
注:图中所示为1个酵母细胞。细胞膜带负电荷,上有多个可以运输质子或阴离子的转运蛋白,包括1个葡萄糖载体、可将弱酸阴离子排出细胞的Pdr12转运蛋白和细胞质膜H+-ATPase。
pH对产甲烷菌的选择作用 微生物生存环境的pH对产甲烷菌群落具有较强的选择型。实验室研究或自然生态系统中存在产甲烷现象的环境pH范围在3~10[85]。耐酸毒性的产甲烷菌,往往存在于海洋或者具有低渗透压的北方冻土、沼泽、苔原等极端低温环境中[94]。迄今为止,所发现的大部分耐酸毒性的产甲烷菌为氢营养型产甲烷菌。Horn等人[95]发现,在pH 4.5的泥炭沼中,优势产甲烷菌分布在甲烷微菌目Methanomicrobiales和甲烷杆菌目Methanobacteriales,且低浓度的乙酸很可能是通过共生乙酸氧化和氢营养型甲烷化的联合途径降解。Kotsyurbenko等人[70]对西伯利亚酸性沼泽中的产甲烷菌群进行培养,发现随着pH的降低(3.8~6.0),产甲烷主导途径由乙酸发酵型转向氢营养型,并在pH 4.5时分离培养得到氢营养型的甲烷菌杆菌属菌株Methanobacterium sp.strain。Kim等人[96]也发现,在pH低于5的厌氧反应器中,甲烷化过程通过氢营养型途径进行。Taconi等人[97]研究了乙酸浓度为2 g/L的未缓冲体系中甲烷的产生规律,发现甲烷化可在初始pH 7.0和pH 4.5的情况下启动,且初始pH 4.5会使得甲烷产量比理论最大产量增加30%,作者认为系统较低的pH使得无机碳以碳酸分子的形式存在,从而有利于CO2还原型甲烷化反应的进行,使得甲烷产量增加。这进一步说明氢营养型产甲烷菌可在极酸性环境生存,而乙酸营养型产甲烷菌更喜好中性环境。
但也有研究发现,甲烷八叠球菌科Methanosarcinaceae具有较强的耐酸毒性特征。如Maestrojuan等人[98]分离出了可在pH 5.0的环境下生长的甲烷八叠球菌属Methanosarcina的菌株。而Staley等人[99]则发现,在城市生活垃圾厌氧消化填埋柱中,Methanosarcina barkeri能够在pH 5.0~6.25的酸性环境下成为高浓度VFAs逐渐降解的甲烷化中心。Steinberg和Regan[37]也发现,在pH 5.0的泥炭土中存在活跃生长的Methanosarcina。在碱性环境下,通常认为乙酸发酵型产甲烷菌更容易受到抑制,而氢营养型产甲烷菌具有更强的耐受性[100]。但van Leerdam等人[101]则发现,Methanosarcina mazei在pH 8.3的厌氧消化反应器中仍在降解甲硫醇。(https://www.daowen.com)
2.VFAs浓度
易降解生物质废物厌氧消化过程中,水解—酸化和乙酸化—甲烷化两相的不平衡可使得VFAs累积达到十几克每升的浓度水平,进而产生酸胁迫。VFAs浓度可指示厌氧消化过程不同相间是否平衡,常被用作评价工艺是否稳定运行的重要指标[36]。作为厌氧消化过程中重要的中间代谢产物,VFAs是发酵过程的产物和甲烷化的重要底物,在一定的浓度范围内可促进各反应的顺利进行,但浓度过高时则会对厌氧消化系统产生毒害作用。如Siegert和Banks[102]研究了VFAs对厌氧消化不同阶段的影响,发现在pH 7.0的环境中,VFAs浓度高于2 g/L时,纤维素水解开始受到抑制;VFAs浓度高于4 g/L时,葡萄糖发酵开始受到抑制;当VFAs浓度高于6 g/L时,产甲烷化反应开始受到抑制。任南琪等人[12]通过研究不同种类VFA对产甲烷菌的影响发现,丁酸浓度高于2 g/L时,比产甲烷速率降低,产甲烷菌的活性被缓慢抑制;丙酸浓度高于0.31 g/L时,比产甲烷速率下降,产甲烷菌被快速抑制;当乙酸高于2.34 g/L时,比产甲烷速率开始下降,当乙酸浓度达到4.01 g/L时,比产甲烷速率锐减,产甲烷菌的活性被严重抑制。而Wang等人[103]则发现,pH 7.0时,当发酵产物乙醇、乙酸和丁酸浓度分别达到2.4、2.4和1.8 g/L时,甲烷化反应并未受到抑制,而当丙酸浓度达到0.9 g/L时,产甲烷菌受到显著抑制,而且其活力难以恢复。而Amani等人[104]研究了VFAs对富集了产乙酸菌和产甲烷菌的混合菌群的影响,通过响应曲面法分析发现,高浓度乙酸对丙酸、丁酸氧化以及甲烷化过程均会产生抑制,且高浓度乙酸对甲烷化的影响程度要高于丙酸。不同的研究结果中,VFAs毒性的差异可能是由于研究体系的不同,如底物、接种污泥、pH和反应器类型等的差异导致。
由于高浓度游离有机酸对微生物细胞的损害,VFAs对产甲烷菌的毒性受到pH的极大影响。当反应器内呈酸性(pH<7)时,游离VFAs所占的比例较高,产甲烷细菌易于受到更高程度的抑制。Anderson等人[105]发现,游离态乙酸的起始抑制浓度为0.5 mmol/L。Fukuzaki等人[106]则发现,0.5~2.0 mmol/L的游离态乙酸对乙酸营养型产甲烷菌(包括甲烷鬃毛菌和甲烷八叠球菌)产生抑制。不同种类的产甲烷菌对游离有机酸的耐受力不同,相对于乙酸营养型产甲烷菌,氢营养型产甲烷菌具有较强的耐受力,但在高酸度下仍然会受到游离乙酸的胁迫[70,107]。van Kessel和Russell[108]观测到,100 mmol/L的乙酸浓度下,pH的降低使得瘤胃产甲烷菌迅速受到抑制;而相同pH下,乙酸浓度的增加也会降低甲烷的产率。Horn等人[95]和Bräuer等人[107]也报道了氢营养型产甲烷菌受到高浓度游离态有机酸抑制的现象。
乙酸作为甲烷化的底物,浓度过高时将会对产甲烷菌产生显著的底物抑制效应。Clarens和Moletta[109]研究了高温55℃下Methanosarcina sp.MSTA-1的生理特性,发现其生长半饱和速率常数为10.7 mmol/L,在乙酸浓度为400 mmol/L时(初始pH中性)已经完全抑制了甲烷化反应和产甲烷菌的生长。Lepistö和Rintal[110]发现,高温70℃下乙酸对产甲烷反应的抑制模式符合Haldane模型,当乙酸浓度超过4.6 mmol/L即开始产生抑制。Fukuzaki等人[106]研究了乙酸浓度对富含甲烷鬃毛菌的厌氧污泥和Methanosarcina barkeri产甲烷速率与生长速率的影响,发现游离乙酸对两者活力的影响符合二级底物抑制模型,两者的饱和速率常数分别为4.0μM和104μM。Illmer和Gstraunthaler[111]发现,实际运行的生物质废物厌氧消化反应器内,当乙酸浓度累积到150 mmol/L时,产气量开始下降,工艺过程开始恶化。而Lins等人[21]也发现,150 mmol/L浓度的乙酸(初始pH 7.2)的甲烷化过程出现显著的迟滞期(>10 d),表明该乙酸浓度已对甲烷化产生抑制。
厌氧消化系统中,利用乙酸的微生物包括甲烷鬃毛菌Methanosaeta sp.、甲烷八叠球菌Methanosarcina sp.、共生乙酸氧化细菌,以及硝酸盐还原细菌、硫酸盐还原细菌、铁还原细菌等。但在氧化态氮、硫、铁等电子受体缺乏时,主要是前三者竞争乙酸。由于不同的嗜乙酸微生物具有不同的乙酸亲和力和生长速率,乙酸浓度会极大地影响微生物的菌群结构。如甲烷鬃毛菌属Methanosaeta可利用乙酸的最低浓度为7~70μmol/L,但其生长速率较低,而甲烷八叠球菌属Methanosarcina的生长速率较高,但对乙酸的亲和力较弱,其乙酸利用最低限值为0.2~1.2 mmol/L。因此,在乙酸浓度高于1 mmol/L的环境中往往是甲烷八叠球菌属Methanosarcina占优势,而在乙酸浓度低于1 mmol/L时,往往是甲烷鬃毛菌属Methanosaeta占优势[112,113]。乙酸浓度对于共生乙酸氧化细菌的影响并不明确。Hori等人[23]、Petersen和Ahring[74]发现共生乙酸氧化途径在乙酸浓度为0.2~1 mmol/L的高温反应器中占主导。Shigematsu等人[76]在研究一个中温下以乙酸为基质的恒化器时,发现低乙酸浓度(0.2 mmol/L)下共生乙酸氧化途径占优势,而较高的乙酸浓度下(4 mmol/L)则有利于乙酸发酵型途径的进行。但在另外的一些高温反应器中,即使VFAs浓度高达数十mmol/L(以乙酸浓度计),共生乙酸氧化仍然为乙酸甲烷化的主要途径[5]。而在共生乙酸氧化细菌及氢营养产甲烷菌的培养实验中,则可以看到,高乙酸浓度刺激了菌株的生长。Schnürer等人[61]则观察到,当乙酸浓度降低至30 mmol/L时,中温的共生乙酸氧化菌株即停止生长。
3.氨浓度
在生物质废物的厌氧消化过程中,氨主要是通过氨基酸的酸化过程产生。由于氮是微生物的营养物质,微生物利用氨氮作为其氮源,低于12 mmol/L的氨浓度(以NH3计)有利于厌氧消化系统的运行[114]。但氨浓度过高时,则会对微生物产生毒害作用。在各种参与厌氧消化的微生物中,产甲烷菌对氨最敏感,容易因受到氨的抑制而停止生长[17]。由于受到其他物质的协同或拮抗作用和络合反应的影响,不同研究体系中氨对产甲烷菌的抑制水平存在很大差异。另外,厌氧消化原料和接种物、环境因素(温度和pH),以及微生物的驯化等因素也对氨的毒性产生很大影响。在文献中,氨对产甲烷反应的抑制浓度阈值具有较大的范围,达到50%抑制时的总氨氮浓度(Total Amonium Nitrogen,TAN)由121 mmol/L到1 000 mmol/L(以NH+4-N计)不等[8];而当游离氨态氮浓度(Free Amonia Nitrogen,FAN)达到6 mmol/L(以NH3-N计)时,即已对甲烷化代谢产生抑制[115]。
通常认为,乙酸营养型产甲烷菌比氢营养型产甲烷菌更容易受到氨的抑制,但也有相反结论的报道[28,116]。而多营养型的甲烷八叠球菌比严格乙酸营养型的甲烷鬃毛菌更能耐受氨毒性[34]。因此,氨浓度成为影响厌氧消化系统内微生物菌群结构和甲烷生成途径的重要因素。Karakashev等人[40]研究了13个厌氧消化反应器的微生物菌群结构和产甲烷途径,发现在高氨氮、高VFAs的反应器中,甲烷鬃毛菌消失,甲烷主要通过共生乙酸氧化和氢营养型甲烷化联合途径产生。Nettmann等人[57]也在其研究中发现了相似的规律。Schnürer和Nordberg[117]、Westerholm等人[22]发现,TAN浓度超过214 mmol/L时,共生乙酸氧化现象被激活,共生乙酸氧化细菌和氢营养型产甲烷菌开始取代甲烷鬃毛菌成为优势菌群。但是也有研究发现,在高氨氮环境下,也存在大量的甲烷八叠球菌和甲烷鬃毛菌[77,118],而甲烷八叠球菌甚至成为耐受高氨胁迫的优势菌种[119,120]。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







