与其他非甾体抗炎药一样,布洛芬主要用于类风湿性关节炎、强直性脊柱炎、骨关节炎等关节和肌肉病变,也用于一般的镇痛治疗。虽然它具有解热作用,但由于这方面作用较弱,一般不将其作为退热药。本品为白色结晶性粉末;稍有特异臭味,几乎无味;本品在乙醇、丙酮、氯仿或乙醚中易溶,在水中几乎不溶;在氢氧化钠或碳酸钠试液中易溶;本品的熔点为74.5~77.5℃。
布洛芬是新一代重要的非甾体消炎镇痛药物。传统的消炎止痛药阿司匹林已沿用了近百年,但它存在疗效低、用药量大(通常以克为单位)、有一定副作用等缺点。布洛芬作为阿司匹林的替代品,其解热、镇痛、消炎作用大于阿司匹林,而副作用却比阿司匹林小得多。因此,自20世纪70年代末上市以来,以其疗效高、副作用小为特点而获得迅速发展。1987年,它在全部解热镇痛消炎药物的23亿美元销售额中占18%的份额,1993年上升至30%以上。目前,全世界布洛芬的总产量为8000t左右。布洛芬作为一种重要的α-芳基丙酸类非甾体抗炎药物,药理研究证实(S)-布洛芬在体内抑制前列腺素合成的活性是(R)-对映体的160倍。在人体内,(R)-对映体与辅酶A形成的酯能够替代甘油三酯中的天然脂肪酸形成杂化甘油三酯,干扰正常的脂代谢和膜功能,因而(R)-布洛芬具有毒副作用。单一的(S)-型对映体比外消旋体的疗效更好、毒副作用更小,已于1997年在瑞士获得认可。除了化学不对称合成和拆分外,以酶或微生物细胞为手性催化剂的生物拆分也是制备(S)-布洛芬的一条有效途径。
7.3.5.1(R,S)-布洛芬的非水相酶促酯化
1.非水相酶促酯化拆分布洛芬的技术路线
非水相酶促酯化拆分布洛芬的技术路线[以优先酯化(S)-布洛芬的脂肪酶为例]如图7-12所示。具体过程:消旋的布洛芬与醇在水解酶催化下发生对映选择性的酯化反应生成(S)-布洛芬酯以及剩余的(R)-布洛芬;然后经过分离步骤将布洛芬酯与布洛芬分离;然后用化学方法将(S)-布洛芬酯水解可生成(S)-布洛芬;(R)-布洛芬加入碱在一定温度下进行消旋化反应,生成消旋的布洛芬,可作为反应的原料重新投入反应中。已有多篇文献报道酶促酯化拆分布洛芬。
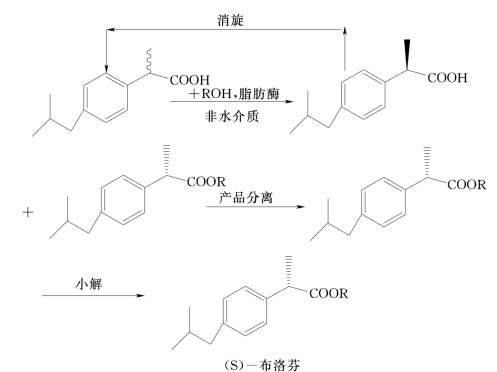
图7-12 非水相酶促酯化拆分布洛芬的工艺路线
2.举例
Sánchez等人利用固定化的根霉(Rhizomucor miehei)脂肪酶(Lipozyme® IM20)在异辛烷中催化布洛芬与正丁醇发生对映选择性的酯化反应,生成(S)-布洛芬正丁酯。在装载了5.8g Lipozyme® IM20脂肪酶的填充床反应器中反应100h,转化率>45%,e.e.>92%,产生6g(S)-布洛芬正丁酯。
(1)批式反应。用于正交试验的批式反应在一个25m L的反应器中进行,反应体积为10m L。用水饱和的异辛烷作为溶剂,丁醇作为酯化反应的底物,添加酶量为10mg/m L。反应在一定温度下进行,转速为250r/min。
(2)正交试验。进行了三因素三水平的正交试验,以获得最高的E值为优化目标,确定的最佳反应条件:反应温度40℃,布洛芬的浓度为50mmol/L,丁醇与布洛芬的摩尔比为1∶9。此时E值为110。
(3)连续填充床反应器的构建与运行结果。一个空的不锈钢的高效液相色谱柱被用来作为管状的填充床反应器。其规格为30cm(长)×7.8mm(内径),体积为14.3m L。将5.8g Lipozyme®IM20固定化酶(密度为1.12g/m L)填充入反应器,实际的工作体积为9.1m L。反应器浸没在一预先设好温度的水浴中。
反应混合物(异辛烷、布洛芬和丁醇)通过微量滴定管泵入反应器中。反应液的流速通过安装流速控制软件的电脑来控制。(www.daowen.com)
可以看出,除了系统刚启动的3h之外,其余时间的转化率(平均值为45.5%,标准偏差为1.6%)和产物(S)-布洛芬丁酯的e.e.值(平均值为93.9%,标准偏差为0.7%)都维持基本恒定,波动很小。经过100h反应,共产生6g(S)-布洛芬正丁酯,说明反应器在操作的时间范围内保持了很好的稳定性。
(4)底物光学纯度的分析方法。采用Chiracel OD手性柱,测定底物布洛芬的对映体过量值(流动相为正己烷∶异丙醇∶三氟乙酸=98∶2∶0.1,流动相流速为1.0m L/min)。
7.3.5.2(R,S)-布洛芬酯的选择性水解
1.水解反应拆分布洛芬的技术路线
首先消旋的布洛芬经化学方法与醇发生酯化反应生成相应的布洛芬酯;其次布洛芬酯在水解酶催化下发生对映选择性水解反应,产生(S)-布洛芬以及剩余的(R)-布洛芬酯;然后经过分离步骤将布洛芬酯与布洛芬分离,(R)-布洛芬酯加入碱在一定温度下进行消旋化反应,生成消旋的布洛芬酯,可作为反应的原料重新投入反应中;而(S)-布洛芬经酸化、洗涤、干燥等步骤后即可得到纯品。酶催化水解反应制备(S)-布洛芬国内外均有文献报道。
2.酶催化水解制备(S)-布洛芬举例
徐诗伟等利用一株具有高度立体选择性的皮状丝孢酵母(Trichosporon cutaneum)T185对5种布洛芬酯的不对称水解进行了研究,并在克级规模制备了(S)-布洛芬,其e.e.值达93%。
(1)细胞的培养及不对称水解反应。将于28℃生长2d的T158麦芽汁琼脂斜面培养物移入新鲜培养基,于28℃、200r/min振荡培养24h,接种于新鲜培养基内经18h培养后,投加2%(体积分数)的布洛芬消旋酯,然后在上述培养条件下进行不对称水解反应,转化70h。研究表明,在5种底物中,皮状丝孢酵母对甲酯和异丙酯具有较高的选择性,而对乙酯的选择性略低,但活性最高。实验表明底物浓度在1.0%~3.0%范围内时,随着底物浓度增加,产物(S)-布洛芬的e.e.值无明显区别,而布洛芬生成量随底物浓度提高而逐渐增加,但其增长率低于底物浓度的增长,导致转化率明显降低。最适宜的pH值为6.5~7.0,28~37℃,拆分能力无显著变化。
(2)(S)-布洛芬对映体过量值的测定。手性高效液相色谱法:首先将布洛芬衍生为相应的二苯酰胺衍生物,然后利用N-3,5-二硝基苯甲酰-(R)-苯甘氨酸的共价型手性色谱柱(RDNB-PG,25cm×4.6mm)分析,流动相为正己烷-异丙醇(98∶2),流速为1m L/min,检测器波长254nm。具体过程如下。
1)制备布洛芬二苯酰胺。首先用氯化亚砜将布洛芬转化为酰基氯,然后加入二苯胺,反应生成二苯酰胺衍生物,反应步骤按下列两步进行。第一步,布洛芬样品的酰胺衍生化:称取2mg布洛芬样品置于100mm×10mm试管中,加1滴(约50μL)氯化亚砜,在85℃水浴中加热10min,蒸发除去过量氯化亚砜至干,加入0.5m L 4mg/m L二苯胺氯仿溶液,振荡10min,蒸去氯仿。以正己烷-异丙醇(98∶2)定容至一定体积,同时衍生消旋布洛芬标准样品备用。第二步,微生物或酶水解反应液中布洛芬的酰胺衍生物:取一定量水解反应液,用浓盐酸调至p H≤3,以2倍反应液体积的正己烷提取。取0.5m L提取液置于100mm×10mm试管中,蒸发溶剂至干。然后加1滴氯化亚砜,其余步骤同第一步中所述。
2)(S)-(+)-布洛芬e.e.值的测定。将上述以正己烷-异丙醇(98∶2)平衡的布洛芬二苯胺溶液进样HPLC系统。其对映体在(R)-DNB-PG柱上得到完全分离,测定对映体的峰高值(H)。
(3)(S)-布洛芬的提取和物理性质的测定。用15个250m L三角瓶,每瓶装80m L培养基,布洛芬乙酯的浓度为2%,投加底物总量为23g,水解68h经提取,得到(S)-布洛芬5.50g,收率27.2%,熔点为48.4~49.5℃,![]() (c=1,EtOH),e.e.值为93%。同时回收布洛芬乙酯10.75g,
(c=1,EtOH),e.e.值为93%。同时回收布洛芬乙酯10.75g,![]() =-26.6°(c=1,Et OH),底物回收率为46.7%,其可经消旋化后重新使用。
=-26.6°(c=1,Et OH),底物回收率为46.7%,其可经消旋化后重新使用。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





