糖苷酶(glycosidases)能催化糖苷键水解,又称糖水解酶(glycohydrolases)。该酶不需要任何辅酶,是真正的水解酶。糖苷酶有两大类:外糖苷酶和内糖苷酶,前者仅水解末端糖苷键,后者可水解糖链中部的糖苷键。
1.糖苷酶的催化特性
糖苷酶对底物有较高的专一性,但不是绝对专一性。它对糖苷配基(非糖部分)缺乏特异性,这些配基(烷氧基RO-)可作为水解反应的离去基团。当用另一种亲核性强的化合物(如糖、伯醇或仲醇等)与之反应时,将会取代原来的配基生成新的糖苷化合物。
糖苷酶催化的反应存在两种不同机制,这两种机制分别使异头碳的构型发生保留或转化(见图4-10)。通过选择适当的α-或β-型糖苷酶可以控制异头碳的立体构型。在构型转化的反应中,羟基直接取代糖苷配基RO-,导致异头碳构型的转化。在构型保留的反应中,有两次构型转化反应,最终导致构型保留。在构型保留的反应过程中,酶分子中谷氨酸残基的羧基进攻糖苷键,形成共价的糖基-酶中间体,后者被另一个亲核取代基从相反方向进攻,通过异头碳的两次构型转化,使反应底物异头碳构型保留。
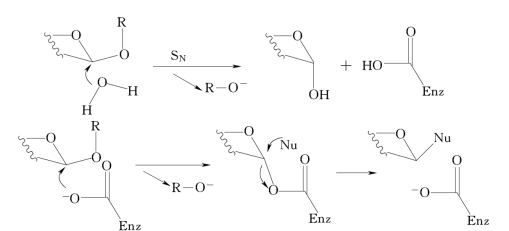
图4-10 糖苷酶催化糖苷键水解机制
2.糖苷合成(https://www.daowen.com)
糖苷酶水解的逆反应可用于糖苷合成,利用游离单糖作为底物直接进行糖苷合成反应称为直接糖基化,这是一个热力学控制反应。由于反应的平衡常数有利于水解反应,因此必须采用高浓度的单糖和亲核试剂,反应产率一般很低,产物为粘稠糖浆。采用选择性吸附剂吸附反应中产生的糖苷,可降低反应产物糖苷的浓度,有利于反应朝合成方向进行。也可利用水-有机溶剂两相体系作为反应介质或者采用PEG修饰的糖苷酶,以促进反应朝向糖苷合成方向进行。
糖苷合成中利用活化型糖苷作为底物,进行糖苷合成反应称为转糖基反应,这是一个动力学控制反应。采用活化型糖苷可以控制转糖基反应的速度大于糖苷水解的反应速度,以使合成的糖苷有较高的产率。活化型糖苷分组中的配体(非糖部分)具有良好的离去基团性质,常用的活化糖基供体有氟化糖苷、叠氮化糖苷和芳基化糖苷(如对硝基苯基糖苷)等。反应过程中先形成酶-糖苷中间体,后者与亲核性试剂反应生成新糖苷。
糖苷酶与糖基转移酶相比,糖苷酶更容易获取,且糖苷酶不需要昂贵的活化型糖基核苷(如UDP-Gal),新生成的异头碳构型可以控制。糖苷酶催化反应的缺点使产率低、产物常为混合物。糖苷酶催化转糖基反应的立体选择性核区域选择性受到许多因素的影响,如反应的温度、有机溶剂、活化供体的反应活性、糖苷配基的性质以及受体糖苷的异头碳构型等。提高转糖基作用区域性和立体选择性的一种简便方法是利用受体糖苷的异头碳构型来调控,这项技术被称为异头碳控制法。当甲基-α-D-葡萄糖苷作为受体,对硝基苯基-β-N-乙酰基-D-半乳糖胺苷作为供体,在β-半乳糖苷酶催化下进行转糖基反应,转化产物1,4-和1,6-糖苷的比率约为5∶1。而当采用甲基-β-D-葡萄糖苷作为受体时,则产生相应的1,3-和1,4-糖苷产物的比率为4∶1。
环状芽孢杆菌(Bacillus cirulans)β-半乳糖苷酶可催化对硝基苯基-β-D-半乳糖苷与乙基-βDN-乙酰硫代葡糖胺苷缩合形成二糖类化合物,后者在米曲霉α-半乳糖苷酶催化下与对硝基苯基-α-D-半乳糖苷生成三糖。β-半乳糖苷酶是使用最多的一种糖苷酶,已有基因工程产品上市。它的热稳定性好,可用于多种糖苷合成。
除了合成天然糖苷外,一些非天然醇也被用作转糖基反应的亲核试剂,制备一些非天然糖苷,这些反应的选择性与糖苷配基性质有关。β-半乳糖苷酶可用于消旋体环状1,2或1,3二醇及仲醇的拆分。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








