单加氧酶(mono-oxygenases)可以使氧分子(O2)中一个氧原子加入到底物分子中,另一个氧原子使还原型NADH或NADPH氧化并产生水(H2O),单加氧酶催化的反应类型见图4-5。单加氧酶催化反应在生物催化的手性合成中有着重要的应用。
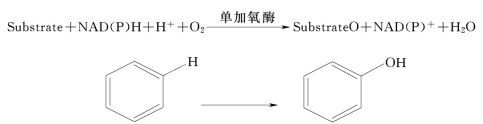
图4-5 单加氧酶催化的氧化反应类型
4.2.1.1 细胞色素P450类(cytochrome P450type,Cyt P450)单加氧酶
Cyt P450是一种以铁卟啉为辅基的蛋白质,因还原型P450与一氧化碳结合的复合物在450nm有一强吸收峰而得名。它们主要存在于动物体肝脏内,催化外源性化合物氧化,具有解毒功能。同样许多微生物中也存在Cyt P450。虽然这些酶之间有差别,如辅酶不同(NADH或NADPH),但在绝大多数Cyt P450单加氧酶中这些酶蛋白分子中与血红素相连的一段氨基酸序列(26个氨基酸残基)都相同。生物催化氧化过程中的活泼氧是由酶和辅基与氧分子相互作用而产生的。以过渡态金属(Fe,Cu)为辅基的单加氧酶大多数属于细胞色素P450类,它们的催化机制可以用恶臭假单胞菌樟脑羟化酶为例来加以说明,见图4-6。
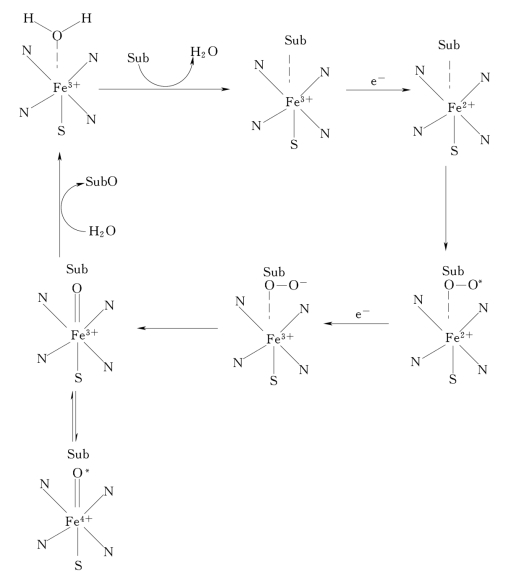
图4-6 Cyt P450类单加氧酶催化机制(www.daowen.com)
铁卟啉环中Fe+与卟啉环平面上的四个氮原子分别形成两个共价键和两个配位键,在卟啉环正上方与水分子形成一个配位键,在正下方与酶蛋白分子中的半胱氨酸残基的硫原子形成一个配位键。当底物结合到酶分子中时,底物将取代水分子与铁卟啉环接近。通过电子传递系统(NADH、FMN、Fe-S、Cytb5等)将电子转移给铁卟啉环中的铁,使Fe3+被还原为Fe2+。分子氧与Cyt P450结合形成氧和Cyt,然后氧从铁中获得电子,Fe2+被氧化为Fe3+。氧合Cyt P450再从电子传递系统接受一个电子,使氧分子的共价键弱化,最终氧分子裂解,其中1个氧与2个氢离子形成水而离去,另一个氧使Fe3+氧化为Fe4+或Fe5+,后者可作为强亲电试剂进攻底物,并促使氧与底物结合,最后酶将单加氧产物[Sub O]释放,同时使铁的价态恢复为Fe3+,酶恢复原形完成一个催化循环。
4.2.1.2 黄素类单加氧酶
以核黄素为辅基的单加氧酶具有与P450类单加氧酶不同的反应机制。反应过程中NADPH首先还原酶-FAD复合物,产生酶-FADH2,后者再被分子氧氧化为氢过氧化物(FAD-4a-OOH),然后脱去质子形成过氧阴离子,它可作为亲核试剂进攻底物中羰基生成四面体中间体,后者通过分子内碳骨架重排形成酯或内酯,最后从FAD-4a-OH中脱去水分子恢复为酶-FAD复合物原形。
Cyt P450催化机制与高价过渡态金属离子化学催化剂的催化机制相似。而以FAD为辅酶的单加氧酶催化机制则与有机过氧化物或过氧羧酸的催化机制相似。
许多单加氧酶结合在细胞膜上,很难分离。因此,单加氧酶催化的反应往往用完整的微生物细胞作为生物催化剂,这样也有利于NADH或NADPH的循环使用,但这种方法的缺点是产物会进一步被代谢,使产率降低。因此,添加抑制催化产物降解酶的抑制剂或采用降解酶的基因缺陷突变株,均可抑制微生物细胞引起的产物分解副反应。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








