立体异构体:其分子由相同数目和相同类型的原子组成,是具有相同的连接方式但构型不同的化合物;其分子具有相同的元素组成(也有相同的官能团组成),但是官能团在三维空间上的排列不同,这种立体异构体称为构型异构体。构型异构体不能通过键的旋转,而只有通过键的断裂和形成才能互相转变。构型异构体有几何异构体和旋光异构体两种。
1.几何异构体
化合物由于碳-碳双键或环上碳-碳单键上的一系列取代基的相对位置不同,导致三维结构不同而形成的异构体互称为几何异构体。
(1)顺/反异构体。下面以2-丁烯说明几何异构体。甲基在双键同侧的异构体为顺式,而甲基在双键异侧的异构体为反式。尽管还有具有同样分子式的结构,但它们不是2-丁烯的几何异构体。由于不可能围绕碳-碳双键旋转,只有通过断裂和形成两个共价键而相互转变。几何异构体具有不同的物理性质,混合在一起很容易被分开。
环体系的几何异构体也采用同样的方法标记。1,2-二甲基环己烷具有两个可能的结构,在通常的温度和压力下,无法围绕碳-碳双键旋转。只有通过一系列键的断裂和形成才能从一个几何异构体转变为另一个几何异构体。同样,尽管环体系中能够发生构象的改变,但是也只有通过共价键的断裂来改变取代基的相对位置。几何异构体具有不同的物理性质和化学性质,能够被分离。
(2)Z/E异构体。当几何异构体被3或4取代基取代后(此处不将氢作为取代基),顺反标记则无法满足要求。可采用另一种标记体系,此体系根据取代基确定基团优先顺序,规定原子序数高的取代基优先。如1-溴-1-氯-2氟乙烯的两种几何异构体,Br原子序数大于Cl,因此Br优先于Cl,C-2上F优先于H。因此,当两个高优先的取代基位于同一侧,此构型标记为Z,源自德文zussamen(一起)。相反地,当两个高优先顺序的基团位于分子的两侧,此构型被标记为E,源自德文entgegen(相对)。
常见基团的优先顺序从低到高依次为:-H<-CH3,-CH2CH3<-CH-CH2<-Ph<CH2OH<-CHO<-COR<-COOH<-COOR<-NH3<-NR2<-OH。在判断Z/E构型之前,应根据基团的原子序数判断各取代基的优先顺序。Z构型表示高优先的基团位于分子的同侧,而E构型意味着它们分别处于分子的异侧。
2.旋光异构体
旋光异构体的一个例子是乳酸,其2号碳原子与4个不同的基团(H、OH、CH3、COOH)相连(见图2-1),4个基团围绕着不对称碳原子有两种不同的排列方式且两种排列方式互成镜像关系,其中2号碳原子称为手性中心(chiral center),也可以称为立体中心(stereogcnic center),但“不对称碳”(asymmetric carbon)的提法现在已经很少用了。它们互为镜像,结构互不重叠,只有通过断裂和形成两个共价键才能互变。与几何异构体不同,这些手性化合物在非手性环境中具有相同的物理性质,不容易从混合物中分离出来。(www.daowen.com)
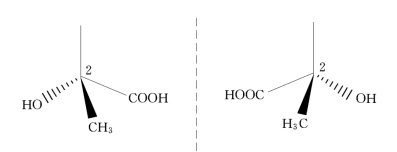
图2-1 乳酸的旋光异构体
(1)对映异构体(enantiomer)及外消旋体。一对化合物分别具有一个或者多个手性中心并且两者互为实物与镜像的关系,称为对映异构体。“enantio”在古希腊语中是“相反”的意思,“对映体”是一种特殊的立体异构体,是指无法相互重叠的互为镜像的一对分子。对映异构体在非手性环境中具有相同的物理和化学性质(比如熔点、沸点和溶解度),唯一的不同是它们对于偏振光的偏振方向不同,它们对偏振光偏转角度相同但方向相反,因此常被称为旋光异构体。
例如,乳酸对映体使平面偏振光顺时针旋转,即偏振光右旋,叫右旋物质,常用符号“+”或“d”表示,其中“d”来自单词dextrorotatory(顺时针)。乳酸使平面偏振光顺时针旋转,那偏振光左旋,叫左旋物质,常用符号“-”或“l”表示,其中“l”源自单词levorotatory(逆时针)。
(+)-乳酸和(-)-乳酸,或(+)-酒石酸和(-)-酒石酸都是对映异构体。手性分子在手性条件下表现出手性,在非手性条件下不能表现出手性。加热和溶解于水都是非手性条件,因此对映体的熔点和在水中的溶解度相同。偏振光是手性条件,所以对映异构体的旋光性不同。对映异构体与无手性的试剂反应的速度相同,与手性试剂反应的速度则不同。生物体内的各种酶具有很高的手性,因此对映异构体的生理作用有很大的差别。
手性化合物的右旋和左旋对映体的等摩尔混合物称为外消旋体或外消旋混合物。当然,它的旋光值应该是零,因为两种对映体的数值相等方向相反的旋光度彼此抵消。如d-乳酸和l-乳酸的1∶1混合物对平面偏振光不产生净偏转,这一比例的对映体混合物称为外消旋体。外消旋混合物在其分子名称的前面冠以(±)dl或rac。
(2)非对映异构体(diastcreoisomer)及内消旋体。非对映异构体(diastcreoisomer)是指分子具有2个或多个手性中心并且分子间为非镜像关系的立体异构体。具有1个以上手性中心的化合物存在许多对对映异构体或非对映异构体,非对映异构体被定义为具有相同化学组成,但不是镜像、分子中的1个或多个不对称中心具有不同的构型而彼此不同的物质。非对映异构体之间不呈镜面对称,具有不同的物理性质,其混合物能够被分离。非对映异构体是旋光异构体,具有旋光性,但在某种情况下它的旋光度为零,这就是内消旋体。
(3)立体结构的命名法。立体化合物的命名有D、L命名法。这种方法是以D-甘油醛或L-丝氨酸为参考得到的。一般要先按费歇尔投影式来表示的。以D-甘油醛为相同的大小排列称为D型。还有一种国际命名法是1956年Chan,Ingold,Prelog提出的R、S命名规则。它是根据手性碳原子直接相连的四个基团所占空间位置的序列确定的。其规则如下:①把与手性中心相连的4个原子或原子团(a,b,c,d)确定一个先后次序,如a>b>c>d。②把次序最小的基团(d)指向我们的方向(对面),然后观察其余基团的序列。从大到小,如果是顺时针方向排列,这个构型定为R;如果是逆时针方向,这个构型为S。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







