ROH经常被用作抗氧化剂,它能够被活性氧自由基氧化生成ROH·+,这一氧化反应被认为是ROH抗氧化的一条途径。然而,ROH能否作为安全的抗氧剂取决于ROH·+反应活性的强弱或者是否存在有效清除ROH·+的途径。以上结果表明,ROH·+是一个反应活性很强的物质,它不仅能够与疏水性的亲核试剂DMA和DPA发生电子转移反应,与亲水性的自由基清除剂NaN3发生加成反应,还能够与Lyso,Trp,Cys和亚油酸发生反应,这预示着ROH具有潜在的光毒性,会引起蛋白质和生物膜的损伤。当ROH单独作为抗氧化剂使用时,可能会有促氧化的风险。然而,在胶束体系中产生的ROH·+能够有效地与水溶性抗氧化剂VC发生反应,这一结果表明,当ROH作为抗氧化剂清除活性氧自由基时,所生成的ROH·+能够被VC快速清除[67]。因此,选择能够清除ROH·+的抗氧化剂与ROH配伍使用,或许能够有效避免ROH的光毒性或者促氧化作用。为此,本文考察了一系列抗氧化剂与ROH·+的反应活性。
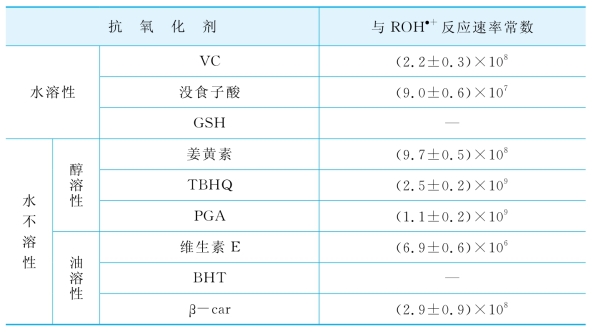
和第3章相同,所选抗氧化剂主要分为水溶性和水不溶性两类,在水不溶性的抗氧化剂中又可分为脂溶性的和醇溶性的。反应速率常数的计算,均是利用公式(2-13),所得到的速率常数见表4-2。从表4-2可以看出,总体上讲,醇溶性抗氧化剂与ROH·+的反应活性最强,水溶性的次之,脂溶性的最差。ROH·+对所选抗氧化剂反应活性的趋势与ATRA·+大体一致,但是ROH·+能够与β-car发生反应,事实上,β-car常被用于区分类视黄醇阳离子自由基和视黄基碳正离子[64,66,69],因为β-car与碳正离子不发生反应,而与阳离子自由基发生电子转移反应,生成β-car阳离子自由基(λmax=1 040nm)。根据上一章分析,由于β-car和ATRA·+在微乳中分布位置的差异阻止了它们之间的反应,ROH的醇羟基的极性没有ATRA的羧基强,所以ROH·+在微乳中的分布可能相对更倾向于油相,进而能够与β-car发生反应。但是这一假设无法解释为什么BHT与ROH·+无法反应。影响类视黄醇阳离子自由基与抗氧化剂之间反应的因素可能很多(例如抗氧化剂的分子结构和氧化还原电势),很难找出统一的机理去解释。但不管怎样,通过比较它们的反应速率常数,可以初步判断不同的抗氧化剂清除ROH·+的能力。
表4-2 在pH=7.4条件下,ROH·+与所选抗氧化剂的反应速率常数(单位:M-1s-1)(https://www.daowen.com)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




