固体自溶液中的吸附比气-固吸附要复杂得多。这是因为溶液至少有两个组分:溶剂与溶质。固-液吸附涉及溶质、溶剂和吸附剂三者分子间错综复杂的作用。对于气相吸附,可通过高真空处理脱除固体表面的气体,可使气-固吸附从零开始。而对于液-固吸附,固-液界面不可能清零,总会有溶液中的各组分分子。即便最简单的双组分稀溶液,当溶质的吸附达最大值时,固-液界面上仍然存在溶剂分子,也就是说溶液各组分的竞争吸附是不可避免的。当比表面积较大的固体在溶液中吸附任一溶质或溶剂时,存在着竞争性地优先吸附或顶替吸附现象。一般来说,溶质和溶剂均能被吸附,吸附层可视为溶质分子与溶剂分子的二维溶液。由于固体对溶剂与溶质的相互作用会有差异,结果使溶液在界面吸附层的浓度与体相的浓度不一致。若溶液吸附层浓度大于其在体相的浓度,则对溶质是正吸附,对溶剂为负吸附;反之,对溶质为负吸附,对溶剂为正吸附。溶液吸附量定义如前,即单位质量的吸附剂吸附溶质物质的量(mol/kg﹣1),吸附量的测定是在某温度下将一定质量mn的固体吸附剂加到一定体积V及已知浓度c0,i的溶液中,不断搅拌,达到吸附平衡后再测定溶液的浓度ci,则溶质的吸附量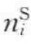 由下式计算:
由下式计算:
式(5-15)所得的吸附量通常称为表观吸附量,此式忽略了溶剂和其他组分吸附的影响。对于稀溶液,表观吸附与真实吸附近似相等,但对于浓溶液则不然。再者,有时杂质的影响也不可忽略。例如对于稀溶液的吸附,溶剂中的杂质很可能与溶质浓度的数量级相近,且吸附剂的某些可溶性杂质会使得溶液成分复杂化。例如,硅胶对苯中硝基苯的吸附等温线会因溶液中含有微量的水而大不相同。此外,液体的扩散速度受到相对分子质量和分子间相互作用的影响,固-液界面吸附达到平衡的时间一般要比气-固吸附的时间长,对于多孔固体,特别是微孔固体,达到吸附平衡所需的时间更长。溶剂与溶质在固体表面的吸附性能取决于它们与表面分子作用力的强弱。与固体表面性质相近的组分易被吸附。液相吸附的测定方法主要有浸泡法、循环法和色谱法等。(https://www.daowen.com)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






