单分子膜的研究与制备具有广泛的理论及实用价值,分别简述如下。
1.理论方面的应用
(1)测定成膜物分子的相对分子质量。对于相对分子质量未知的某种成膜物,称取质量mn的成膜物,配制低浓度的铺展液,在总面积为AT的区域内铺展成膜,并确保所制备的单分子膜处于气态膜状态,通过改变AT的大小来测试其π-AT曲线。根据表面理想气体状态方程,可得
通过实验所测数据,绘制πAT-π曲线。利用作图法,求π0时πAT的值,代入式(3-44)即可获得相对分子质量M值。
(2)通过对单分子膜进行研究,可以确定某些化合物的分子结构,还可以通过单分子膜性能的测试探索细胞膜的生理机制。本书第4章将对肺泡单分子膜的行为特征及其生理机制进行详细探讨。
2.实际方面的运用——防止水分蒸发
据Lamer估算,仅美国西部水库水分蒸发而损失的水分,每年就有2.0×1010m3。显然,如能有效地减少水的蒸发,对资源及干旱地区的农作物生产是十分有利的。如何利用单分子膜来实现这一目的呢?其原理又是什么?先从水的蒸发过程入手进行探讨。
所谓蒸发,即分子从液相转移到气相的过程(见图3-26),在此过程中,水分子必须穿过液相转移到界面,然后脱离界面进入气相,并穿过气相一段距离后才能成为自由的气相分子。过程中必然受到阻力。若界面为平面,则蒸发量Q与蒸发阻力、气-液浓度差△c、界面面积A等因素有关,可表达为
图3-26 水分蒸发示意图
式中,θ为时间;Rt为阻力系数。
蒸发阻力主要包括液相阻力、界面阻力和气相阻力三项,即
Rt=R1+Ri+Rg (3-46)
式中,R1为液相分子扩散时分子间碰撞产生之阻力;Rg为气相分子扩散时分子间碰撞产生之阻力;Ri为位于界面的分子由于溶剂化而引起状态变化的阻力,即单分子膜所产生的阻力。
膜阻力由于成膜物质在水中的溶解度很小,实际上对水的活度并无影响,因此单分子膜的存在并未影响到水的平衡蒸气压,而只是影响了水的蒸发速率,即改变了蒸发动力学性质。例如,脂肪酸类单分子膜的膜压π从0增加到30~40mN/m时,水分蒸发速率将下降60%~90%,其原因即膜阻力Ri增大之故。根据分子运动论可导出膜阻力与单分子膜的表面压π和相对分子质量M的函数关系符合下式:
式中,α为液面上的凝聚比,实测的α值为0.34。
从式(3-47)可以看出,在同一表面压π下,Ri随碳原子数增加而增大。对同种成膜物质,单分子膜的π越大,Ri也相应地增大。
实验结果表明,通常只有凝聚膜才有良好的抑制水分蒸发作用。另外,当单分子膜对水分子的阻力较大时,其对氧气等气体分子的渗透阻力也较大,故实际情况中还要考虑单分子膜对氧气等气体应具有一定的透过性,否则水生生物将无法生存。研究表明,足够高的膜压下的长链脂肪醇单分子膜具有所要求的性能。
3.表面膜中的化学反应
不溶性单分子膜上的化学反应是指成膜物质之间或成膜物质与基底液(载膜液)或气相中某组分间的化学反应。多数情况下,底液中的成分会作为反应物或催化剂参与界面反应。膜上化学反应的进行通常伴随着分子面积、表面压、表面电势等界面性质的变化。因此,可以借助其中一些参数的测定来监测反应的进行。例如可以用固定膜压、改变膜面积或固定膜面积而改变膜压的方法研究反应动力学。
膜反应动力学方程通式 设Ja,Jb分别为1mol A,B两组分所具有的某种性质的量(如A或π),它具有加和性,即整个物系的性质表示为(https://www.daowen.com)
J=naJa+nbJb (3-48)
考察不可逆反应 A→B
反应初始时刻,膜中全部为组分A,组分B为零,体系的量J为J0,且有下式:
当反应时间为∞时,膜中组分A全部变为组分B,体系的量J为J∞,且有下式:
反应中的某一时刻θ,膜中含有两种组分,体系的量J为
式(3-51)两边同时乘以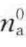 ,得
,得
将式(3-49)和式(3-50)代人式(3-52),整理得
式(3-53)为膜反应动力学方程的通式,下面根据具体的膜反应模式,做进一步的探讨。
膜压恒定产物溶解的膜反应 当π恒定时,膜物质分子的浓度也是恒定的,随着反应的进行,生成的产物被溶解进入了液相,变量为膜面积,即J=A,当t→∞,na→0时,A∞=0,可得
当膜中组分A的浓度不变时,一般可认为它符合一级反应速率定律,即
A =A 0e﹣kθ (3-55b)
通过实验测定膜面积随时间的变化关系,即可得知反应转化率随时间的变化关系,进而求得反应速率常数。
膜压固定而产物不溶的膜反应 这类反应的特点是随着反应的进行,产物越来越多。由于表面压恒定,故膜面积随之增大。将通式中的J换成膜面积A,可得
当基底液中参加反应的物质浓度近似恒定不变时,可视为一级反应,则式(3-56)可表达为
A-A∞=(A0-A∞)e﹣kθ (3-57)
膜面积不变而膜压改变的膜反应 当膜面积恒定时,膜压将是组分的加和函数,因此此时也可将通式写成:
π-π∞=(π0π∞)e﹣kθ (3-58)
式(3-58)成立的前提条件是此膜符合表面理想状态方程。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







