1.铺展系数与界面张力
液体2在液体1上是否能铺展形成液-液界面呢?以水面为例,在水面上滴一滴不溶或微溶于水的液体2时,会出现以下三种情况。
(1)液体2迅速展开;
(2)液体2根本不展开,保持滴状浮在水面:
(3)液体2最初几滴展开,继续滴加的液体不再铺展,而是收缩成液滴浮在水面。
产生上述现象的原因仍在于液-液界面张力的变化,下面以苯-水体系进行定量讨论。在纯水表面加一滴苯,苯滴迅速展开,继续滴加则苯滴收缩,并形成晶状液滴浮于水面,如图3-3所示。设水和苯的表面张力分别为Γ1和Г2,水-苯界面张力为Γ12,其中Г2和Γ12与水面的夹角分别为θ和φ,三个力呈平衡状态,根据水平方向受力分析,有如下关系:
Г1=Г2cosθ+Γ12cosφ (3-14)
由于晶状液滴一般很薄,θ和φ均可近似为0,式(3-14)可简化为
Г1=Г2+Γ12 (3-15)
在这三股力中,Г1使液滴铺展,而Г2和Γ12则试图使其收缩,当Γ1-(Г2+Г12)>0时,液滴铺展开;Г1-(Г2+Г12)<0时,液滴收缩。
令 S2/1=Г1-(Г2+Γ12) (3-16)
通常将S2/1称为铺展系数,其值的正负可作为液体2在液体1表面上是否铺展的判据,即当S2/1>0时,液体2在液体1表面展开;当S2/1<0时,液体2在液体1表面收缩。
表3-3列出了一些液体在水面上的铺展系数。从表中数据可以看出,脂肪醇和油酸等液体能在水面上铺展,而二硫化碳和邻二甲苯却不能。一般来说低表面张力的液体易于在高表面张力的液面上展开,反之则不行。另外,我们看到苯的铺展系数为9.3(单位:mN/m),应该能在水面铺展,那又为什么继续滴加会呈现晶状液滴收缩起来呢?这是因为两种互不相溶的液体之间或多或少会有少许溶解,会互相饱和,从而引起两液体表面张力的变化,而纯液体的数据只能判断两液体刚解除时的铺展情况,随后的状态要由相溶且达到饱和后的两液体的表面张力重新计算铺展系数,此时,Γ1和Г2分别变为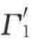 和
和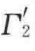 ,真实的铺展系数S2/1则变为
,真实的铺展系数S2/1则变为
表3-3 液体2在水面上的铺展系数(20℃)
对于苯-水体系,在苯与水接触相溶并达到饱和后,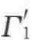 和
和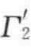 分别为62.2mN/m和28.8mN/m,将其代入上式可得(www.daowen.com)
分别为62.2mN/m和28.8mN/m,将其代入上式可得(www.daowen.com)
S′2/1=62.2mN/m-28.8mN/m-34.6mN/m=﹣1.2mN/m<0
由此可见,最初苯在水面上铺展(S2/1为9.3mN/m),而继续滴加的苯会在水面上逐渐收缩为晶状液滴。
2.铺展系数的理论基础
如上所述,根据液-液体系的铺展系数值,就可判断液体2能否在液体1表面成功铺展,那么这一判据有无理论基础呢?因铺展过程为一自发过程,即自由焓减少的过程,如果能证明当S2/1>0时, <0,那就表明S2/1与自由焓变化一样可作为过程的判据,且具有明确的物理意义。下面将从表面热力学理论出发进行推导。
<0,那就表明S2/1与自由焓变化一样可作为过程的判据,且具有明确的物理意义。下面将从表面热力学理论出发进行推导。
在恒温、恒压条件下,界面自由焓G仅为各相面积A1,A2和A12的函数,即
G=f(A1,A2,A12) (3-18)
因G为状态函数,其全微分形式为
在铺展过程中,液相1的面积减少,液相2和液-液界面相的面积增加,有
dA2=dA12=﹣dA1 (3- 20)
将式(3-20)代入式(3-19),并都用dA12表达,有
根据界面自由焓的定义式,有:
将式(3-22)代入式(3-21),并两边同时除以dA12,可得
对式(3-23)积分,可得铺展过程的自由焓变为
由于铺展过程中液-液界面的面积是增加的,即△A12>0,由式(3-24)可知,当S2/1>0时,铺展过程的自由焓是降低的,即 <0,这表明铺展过程能自发进行。
<0,这表明铺展过程能自发进行。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





