溶液的表面张力与溶质在表面的吸附行为密切相关,吉布斯(Gibbs)根据热力学导出了著名的Gibbs吸附等温线方程,过程简述如下。
设二元溶液在恒温下达到平衡,n1和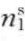 为溶剂在体相和表面相的物质的量,n2和
为溶剂在体相和表面相的物质的量,n2和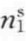 为溶质在体相和表面相的物质的量,A为溶液的表面积,考虑到表面对物系性质的影响,体系自由焓变化为
为溶质在体相和表面相的物质的量,A为溶液的表面积,考虑到表面对物系性质的影响,体系自由焓变化为
dG=Vdp-SdT+ГdA+∑μidni (2-30)
在恒温、恒压下,将式(2-30)应用于表面相,有
在T,p,Г和μ等强度参数恒定的条件下,对式(2-31)积分得
因为自由焓为状态函数,具有全微分的性质,所以有
比较式(2-33)与式(2-31)得
对于均匀溶液体相,有
n1dμ1+n2dμ2=0 (2-35a)
变换上式,得
当吸附达到平衡时,同一组分在表面相和体相中的化学位相等,故有
将式(2-36)代入式(2-34b),经整理可得
由式(2-38)和式(2-37)可得M 与Г的关系为
体相溶质的化学位与其活度系数之间的关系为
dμ2=RTd ln a2 (2-40)
将式(2- 40)代入式(2- 39),经整理得(www.daowen.com)
对于理想溶液或稀溶液,可用浓度c代替活度a,故有
式(2-42)就是著名的Gibbs吸附等温线方程,式中M是单位表面积的溶质吸附量,也叫比表面吸附量或表面过剩量(surface excess);c为溶质在体相中的浓度。由式(2-38)可知,表面过剩量是表面浓度与体相浓度的差值。对于一般的水溶液,表面过剩量不等于表面浓度,但在极稀溶液中,溶质往往全部富集于表面,这时可近似认为两者相等。
Gibbs方程的热力学推导是严格的,但还需经过实验验证。这个工作直到Gibbs导出此式50年后才由McBain和他的学生们完成。他们设计了一个装置,让一个刀片以11m/s的速度迅速刮过溶液表面,刮下一薄层液体,其厚度约0.1mm,根据被刮下液体重量w和浓度c以及溶液浓度c0和刮过的面积A,可按下式计算出吸附量:
McBain等的实验结果不但证明溶液表面有吸附,而且证明表面非活性物质在表面为负吸附。
根据Gibbs方程,可导出比表面吸附量与溶液浓度及表面张力之间的关系为
式(2-44)表明,比表面吸附量与表面张力对浓度的导数成正比,并且有:
当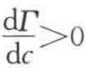 时 M<0,负吸附
时 M<0,负吸附
当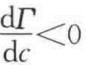 时 M>0,正吸附
时 M>0,正吸附
前述的三类水溶液的表面张力与浓度的函数关系如图2-14所示,下面根据式(2-43)分析一下这三类溶液的表面特征。
第Ⅰ类型 如图2-14所示的曲线A,由于其表面张力随浓度增加而增加,故有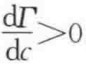 , M<0,为负吸附,表明溶质在表面相的浓度低于体相的浓度,溶质对溶剂来说是表面惰性,又称为表面惰性剂。
, M<0,为负吸附,表明溶质在表面相的浓度低于体相的浓度,溶质对溶剂来说是表面惰性,又称为表面惰性剂。
第Ⅱ、Ⅲ类型 如图2-14所示的曲线B和C,由于其表面张力随浓度增加而降低,故有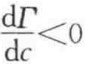 ,M>0,为正吸附,表明溶质在表面相的浓度高于体相的浓度,溶质对溶剂而言为表面活性,又称为表面活性物质。特别是第Ⅲ类水溶液,当其溶质浓度较低时,
,M>0,为正吸附,表明溶质在表面相的浓度高于体相的浓度,溶质对溶剂而言为表面活性,又称为表面活性物质。特别是第Ⅲ类水溶液,当其溶质浓度较低时,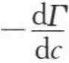 的值很大,M值也很大,表明溶质的表面活性特别强,通常将符合第Ⅲ类曲线的溶质称为表面活性剂(surface active agent)。
的值很大,M值也很大,表明溶质的表面活性特别强,通常将符合第Ⅲ类曲线的溶质称为表面活性剂(surface active agent)。
图2-15 表面活性剂溶液的Г-lgc曲线
表面活性剂主要是长链极性有机物(包括离子型化合物)。这类溶质因能在很低浓度时显著降低水的表面张力,并影响多种界面性质,从而影响铺展、润湿、乳化、起泡、分散、浮选、黏附等物理化学过程而具有重要意义。
表面活性剂水溶液的表面张力随浓度的变化规律,常以Г-lgc曲线的形式来表示,如图2-15所示,从图中可以看出,极低浓度时这两种表面活性剂水溶液的表面张力均随lgc缓慢下降,浓度变大时,其下降速度也明显变大,至一定浓度后,Γ-lgc呈直线关系,经过一转折点后,表面张力便趋于恒定。这是表面活性剂在溶液中形成胶束的结果,转折点的浓度称作临界胶束浓度(CMC),是表面活性剂性能的重要参数。当表面活性剂纯度不高时,曲线在CMC附近有时会出现最低点,如图2-14中曲线C的虚线所示。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








