人体内某些元素平衡失调就会危害到人类的健康并引起疾病,除了要了解元素的种类和功能之外,还要理解饮食、营养与健康的关系,树立平衡营养观念,这样有利于预防疾病、增强体质。
6.1.2.1 人体的酸碱平衡
人的体液pH总是维持在一定范围内,这就是人体的酸碱平衡,酸碱浓度的微小变化就能对正常细胞的功能产生很大的影响。
细胞外液正常的pH是7.4,变化幅度为7.35~7.45,维持生命的极限是7.0~7.8。例如,心肌细胞若低于7.35,心肌收缩力将减弱,若高于7.45,心脏收缩力则过强。此外,人体内上千种酶必须在特定的pH范围内才能发挥它们的活性作用。人体内各种体液的pH见表6-2。
表6-2 人体内各种体液的pH
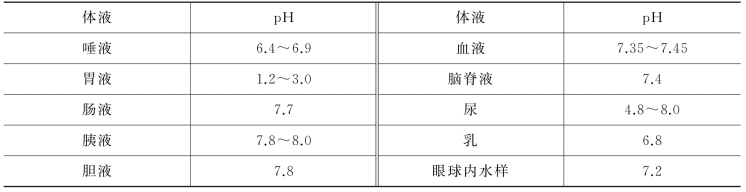
从表6-2中可以看出,人体的体液偏碱性,而胃液的pH在1.5左右,这是因为只有在酸性条件下,胃蛋白酶才能将食物中的蛋白质消化同时杀灭很多细菌。
6.1.2.2 人体内的酸碱缓冲体系
尽管经常有酸性、碱性物质进入体液,但体液的pH并没有显著变化。这是因为所有体液都是缓冲系统,这些缓冲系统中的化学物质能与各种酸、碱结合,防止体内的H+过多或过少。生物体中的3种主要缓冲体系包括蛋白质缓冲剂、碳酸氢盐缓冲剂和磷酸盐缓冲剂(表6-3),每种缓冲体系所占的比例在各类细胞和器官中是不同的。
表6-3 人体内的主要缓冲体系
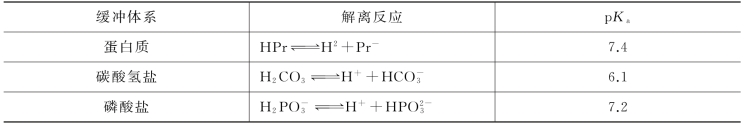
碳酸氢盐缓冲剂存在于所有体液中,是碳酸和碳酸氢根离子的混合物。当摄入强酸时,其立即与碳酸氢根离子化合生成碳酸,这一缓冲系统使强酸变成了弱酸,体液不会变成强酸性。当加入强碱时,缓冲体系中的碳酸就会与之生成水和碳酸氢盐,体液不会变成强碱性。一般成年人体内的血液大约为5 L,其中血浆和红细胞是最基本的组成。红细胞中含有血红蛋白分子以及酸脱水酶,这种酶能催化碳酸的形成和分解。
![]()
由Henderson-Hasselbach方程可知:
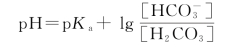
血浆的pH取决于碳酸氢盐和碳酸的比例。通过调节该比例使体液的酸碱度得到缓冲,pH保持在7.35±0.05范围内。例如,在正常代谢反应中产生大量的酸与碳酸氢盐形成难解离的碳酸,有效去除了游离的氢离子。碳酸中的CO2又能通过肺部排除,从而稳定了血浆pH。
pH的调控对人体非常重要,正常人血液的pH为7.35~7.45,当pH低于7.35时会发生酸中毒,pH低于7.0会发生严重的酸中毒导致昏迷死亡;pH高于7.45就会发生碱中毒,pH高于7.8就会发生严重的碱中毒导致手足抽搐致死。
血液中的缓冲系统是人体控制酸碱平衡的第一道防线。其次,可通过呼吸中枢来调节血液中碳酸的浓度,维持血液pH恒定。除碳酸外,还有磷酸、硫酸、尿酸和酮酸等其他一些酸在细胞代谢过程中生成。这些酸进入细胞外液会引起酸中毒。人体通过肾脏来排出多余的酸或碱,调节血浆中NaHCO3的含量,保持血液正常的pH。如果发生较长时间的酸中毒时,骨骼组织也参与酸碱的调节作用,骨骼中钙盐分解,有利于对H+的缓冲:
![]()
在上述反应中,每1 mol Ca3(PO4)2可以缓冲4 mol H+。
6.1.2.3 人体内的化学元素平衡
人体内的化学元素分为必需元素和非必需元素,这两类元素在人体内的浓度和生物效应是不同的。确定某种元素是否为必需元素除了与该元素在体内的浓度有关外,还与它的存在状态和生物活性密切相关。
对于每种必需元素,都有相应的最佳健康浓度,有的具有范围较大的体内恒定值,有的安全浓度范围则比较狭窄,即最佳浓度和中毒浓度之间的差距很小。元素浓度和生物功能的相关性可用图6-1和图6-2表示。(https://www.daowen.com)
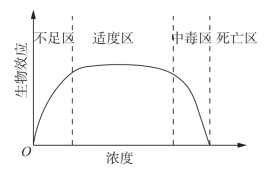
图6-1 必需元素效应图
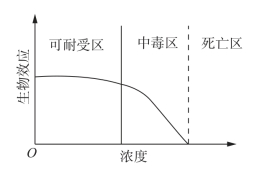
图6-2 有害元素效应图
在人体中,任何一种必需元素缺乏或过量,都会对生物造成影响。所有生物都处于非平衡的稳态中,而这种稳态调节机制只能在一定范围内有效,当摄入金属离子过多时,就会对生物体产生毒害作用。一些化学元素缺乏或过量对人体的影响见表6-4。
在营养物质中,必需元素的最适宜浓度范围是不同的,窄的如铜和硒,铜的正常范围是2~5 mg·kg-1,有害范围是250~500mg·kg-1;硒在0.1mg·kg-1时是有益的,含量达到10 mg·kg-1时则是致癌的;一般成年人对铬的摄入量为0.05~0.20mg·d-1;成年人应摄入的铁量男性为10 mg·d-1,女性为18 mg·d-1,如果摄入量长期少于1 mg·d-1,就会出现脸色苍白等缺铁性贫血症状,但摄入量长期多于200 mg·d-1,则会出现中毒症状。如非洲班图人常过度摄入铁质,故出现了众多消化道出血患者和肝脏中毒患者。
表6-4 元素缺乏或过量对人体的影响
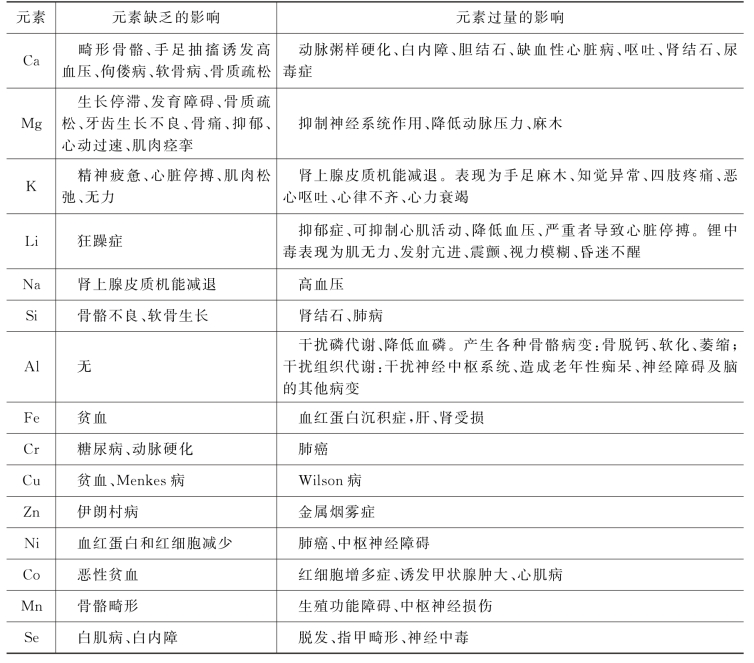
此外,不同元素的不同适宜范围除了与元素有关外,还和人体的个体差异有关,如性别、年龄、身体状况等。对于婴儿来说,适宜的浓度范围很狭窄,如未断乳的婴儿对元素镉、汞、铅、钚、镭较敏感,因此在儿童食品中各种添加剂的用量是被严格控制的。值得注意的是有毒有害物质被摄入后,并不一定马上对人造成伤害,而是在人体内蓄积,在达到一定浓度以后可能会突然爆发。生物体具有强大的自我平衡机制,当外部环境发生相当大的变化时,这种机制能使机体内部并不随之发生显著的变化。比如虽然我们每天摄取不同的食物,但是血液的化学成分几乎保持恒定。这种自动平衡机制也能使人体内必需微量元素的浓度水平维持在最佳范围之内。当体内必需微量元素缺乏时,这种机制能提高人体对该元素的吸收率,并首先保证最紧要的器官和组织拥有合适的该元素的浓度;当该种元素过剩时,也能在一定程度上降低人体对该元素的吸收率,并能将已过量摄入的该元素排泄到体外。当然,这种平衡调控是有一定限度的。
目前,市场上有各种营养强化保健品,从健康的观点出发我们不应该盲目地补充营养,否则会造成某些元素在体内的蓄积,并可能产生危害。平时,要注意均衡饮食,多样化的膳食既是获得各种适量基本营养素最好的方法,也是避免物质达到有害剂量的有效方法。
6.1.2.4 人体内的沉淀溶解平衡
人体中的骨骼由水、有机质、无机盐等组成。其中水约25%~35%。在剩余的固体物质中,约40%是有机质,60%以上是无机盐。无机盐决定骨骼的硬度,有机质决定骨骼的弹性和韧性。骨盐以钙和磷的化合物为主要成分,骨盐中包括磷酸钙、碳酸钙、柠檬酸钙等。正常情况下,血中的钙、磷与骨中的钙、磷维持动态平衡。例如,牙齿的釉质是人体中最硬的组织,主要成分是羟基磷灰石[Ca10(OH)2(PO4)6],它存在这样一个平衡:
![]()
当遇到酸性物质时,酸中的H+向釉质内扩散,使羟基磷灰石溶解,钙离子及磷酸根游离出来,该过程称为“脱矿”。若外部环境中钙离子、磷酸根等浓度比釉质间隙内更高时,可以向内扩散,使相应矿物盐再沉积,该过程又称为“再矿化”,再矿化即是人体自身防龋齿的过程。
进餐之后,口腔中的酶分解食物产生如乙酸(CH3COOH)、乳酸(CH3CH(OH)COOH)等有机酸,如果摄入糖果、冰激凌和含糖饮料这类高糖食品时,会促进牙齿的脱矿作用,当牙齿的釉质层被破坏时,龋齿就开始了。因此一定要坚持饭后刷牙。大多数牙膏中含有氟化物,如NaF或SnF2,这些氟化物能帮助防止龋齿。因为再矿化过程中F-取代了OH-而形成氟磷灰石[Ca(PO4)3F],牙齿的釉质发生了变化,氟磷灰石是更难溶的化合物,不易与酸反应,从而使牙齿有较强的抗酸能力,有利于防止龋齿。但是如果氟过量摄入时又会形成氟斑牙。
6.1.2.5 人体内的水平衡
水约占人体质量的2/3,是人体的主要成分。它是生命最重要的组成物质,体内严重缺水或水过剩都会给人体健康带来极大损害。水把生命所需营养物质输送到全身各部分,参与机体的新陈代谢,参与了人体内所有的化学反应和化学平衡。人体失去10%的水,会产生酸中毒,失去20%~25%的水就会死亡。
为了维持水在体内的平衡,水的排出量会随着饮水量的改变而改变。正常情况下,机体通过体内丘脑下部的神经中枢等调节水平衡来控制渴感和肾脏排水。发烧、高蛋白膳食、干热气候、呕吐、腹泻和外伤损害都会扰乱机体对水的正常需要。
6.1.2.6 人体内的电荷平衡
电荷平衡是人体内的基本平衡,主要指细胞液内外的阴阳离子平衡。细胞外液的阳离子主要是Na+、Ca2+,阴离子主要是Cl-。细胞内液阳离子主要是K+、Ca2+,阴离子是![]() 。细胞液内外的电荷平衡不仅影响信息的传导,还影响着渗透压的平衡。细胞内外由于离子浓度差形成膜电势,人的思维、视觉、听觉、触觉、细胞的分泌等各种生理功能均与膜电势有关。
。细胞液内外的电荷平衡不仅影响信息的传导,还影响着渗透压的平衡。细胞内外由于离子浓度差形成膜电势,人的思维、视觉、听觉、触觉、细胞的分泌等各种生理功能均与膜电势有关。
除以上平衡外,人体中的化学平衡还有配位平衡、各元素间的平衡等。人体中的各种平衡相互联系、相互影响。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





