镍镉电池(Ni-Cd,Nickel-Cadmiun Battery)因其碱性氢氧化物中含有金属镍和镉而得名。镍镉电池结构及外形示意图如图3-30所示。
镍镉蓄电池的正极材料为球形氢氧化镍,充电时为NiOOH,放电时为Ni(OH)2。负极材料为海绵状金属镉或氧化镉粉以及氧化铁粉,氧化铁粉的作用是使氧化镉粉有较高的扩散性,增加极板的容量。电解液通常为氢氧化钠或氢氧化钾溶液,为了增加蓄电池的容量和循环寿命,通常在电解液中加入少量的氢氧化锂(大约每升电解液加15~20g)。充放电过程的反应如下:
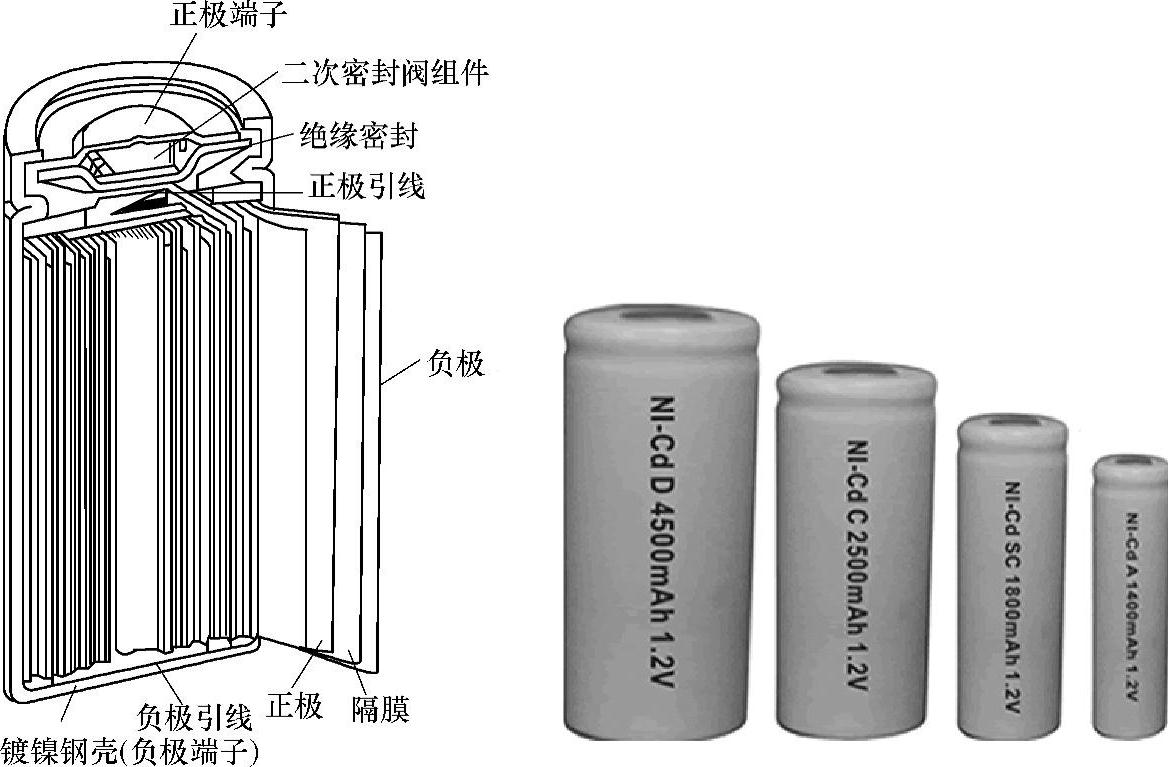
图3-30 镍镉电池结构及外形示意图
正极充放电反应为
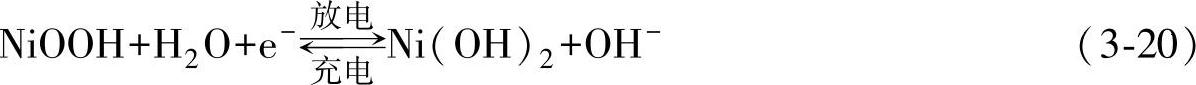
负极充放电反应为
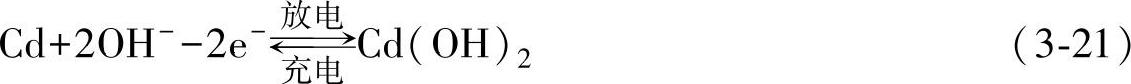
电池总反应为
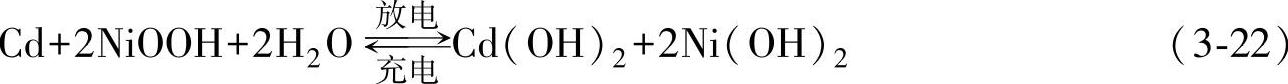
1.镍电极反应机理
镍电极充电时,首先是电极中Ni(OH)2颗粒表面的Ni2+失去电子成为Ni3+,电子通过正极中的导电网络和集流体向外电路转移;同时Ni(OH)2颗粒表面晶格OH-中的H+通过界面双电层进入溶液,与溶液中的OH-结合生成H2O。上述反应先是发生在Ni(OH)2颗粒的表面层,使得表面层中质子H+浓度降低,而颗粒内部仍保持较高浓度的H+。由于浓度梯度,H+从颗粒内部向表面层扩散。
镍电极充电时,由于质子H+在NiOOH/Ni(OH)2,颗粒中扩散系数小,颗粒表面的质子浓度降低,在极限情况下会降低到零,这时表面层中的NiOOH几乎全部转化为NiO2。电极电势不断升高,反应如下:
NiOOH+OH-→NiO2+H2O+e- (3-23)(https://www.daowen.com)
由于电极电势的升高,导致溶液中的OH-被氧化,发生如下反应:
4OH--4e-→O2↑+2H2O (3-24)
因此,在充电过程中,镍电极上会有O2析出,但这并不表示充电过程已全部完成。通常情况下,在充电不久时镍电极就会开始析氧,这是镍电极的一个特点。在极限情况下,表面层中生成的NiO2并非以单独的结构存在于电极中,而是掺杂在NiOOH晶格中。NiO2不稳定,会发生分解,析出氧气。
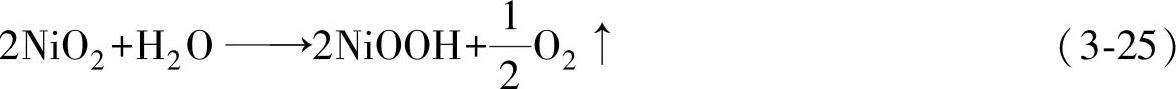
2.镉电极的反应机理
镍镉电池的负极活性物质是海绵状金属镉,放电产物是难溶于KOH溶液的Cd(OH)2。镉电极的放电反应机理是溶解-沉积机理,放电时Cd被氧化,生成Cd(OH)-3进入溶液,然后再形成Cd(OH)2沉积在电极上。Cd(OH)-3在碱液中的溶解度为9×10-5mol/L,该浓度可以使镉电极具有较高的反应速率,这也是镍镉电池能够高倍率放电的主要原因。电极的放电机理为首先发生OH-的吸附:
Cd+OH-→Cd-OH吸附+e- (3-26)
随着电板电势不断升高,镉进一步氧化,生成Cd(OH)3-进入溶液:
Cd-OH吸附+2OH-→Cd(OH)-3+2e- (3-27)
当界面溶液中Cd(OH)-3过饱和时,Cd(OH)2就沉积析出:
Cd(OH)-3→Cd(OH)2↓+OH- (3-28)
生成的Cd(OH)2附着在电极表面上,形成疏松多孔的Cd(OH)2,有利于溶液中的OH-继续向电极内部扩散,使内部的海绵状镉也通过溶解沉积过程转化为Cd(OH)2,实现内部活性物质的放电。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








