燃料电池是一种不燃烧燃料而直接以电化学反应方式将燃料的化学能转变为电能的高效发电装置。为满足汽车的使用要求,车用燃料电池必须具有高比能量、低工作温度、起动快、无泄漏等特性。在众多类型的燃料电池中,质子交换膜燃料电池(Proton Exchange Membrane Fuel Cell,简称PEMFC)完全具备这些特性,所以燃料电池汽车普遍使用聚合物电解质膜(PEM)燃料电池,也被称作质子交换膜电池或固体聚合物电解质燃料电池,使用氢气和空气中的氧气产生发电。
PEMFC在原理上相当于水电解的“逆”装置。其单电池由阳极、阴极和质子交换膜组成,阳极为氢燃料发生氧化的场所,阴极为氧化剂还原的场所,两极都含有加速电极电化学反应的催化剂,一般采用铂/碳或钌/碳为电催化剂,质子交换膜为电解质,氢或净化重整气为燃料,空气或纯氧为氧化剂,带有气体流动通道的石墨或表面改性的金属板为双极板。燃料电池工作原理如图4-2所示。
发电的基本过程是:电池的阳极(燃料极)输入氢气(燃料),氢分子(H2)在阳极催化剂作用下被离解成为氢离子(H+)和电子(e-),H+穿过燃料电池的电解质层向阴极(氧化极)方向运动,c-因通不过电解质层而由一个外部电路流向阴极;在电池阴极输入氧气(O2),氧气在阴极催化剂作用下离解成为氧原子(O),与通过外部电路流向阴极e-和燃料穿过电解质的H+结合生成稳定结构的水(H2O),完成电化学反应放出热量。(www.daowen.com)
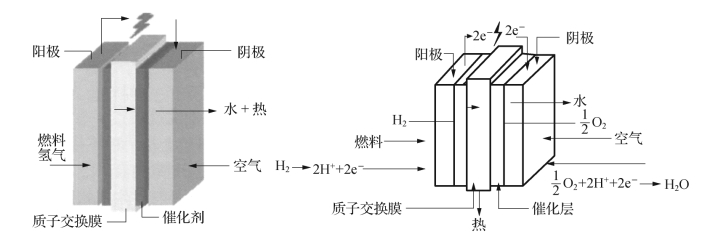
图4-2 燃料电池工作原理
这种电化学反应与氢气在氧气中发生的剧烈燃烧反应是完全不同的,只要阳极不断输入氢气,阴极不断输入氧气,电化学反应就会连续不断地进行下去,c-就会不断通过外部电路流动形成电流,从而连续不断地向汽车提供电力。与传统的导电体切割磁力线的回转机械发电原理完全不同,这种电化学反应属于一种没有物体运动就获得电力的静态发电方式。因而,燃料电池具有效率高、噪声低、无污染物排出等优点,这确保了FCV成为真正意义上的高效、清洁汽车。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




