1)地下水中常见的成分
地下水含有多种元素,有的含量大,有的含量甚微。地壳中分布广、含量高的元素,如O,Ca,Mg,Na,K等在地下水中最常见。有的元素如Si,Fe等在地壳中分布很广,但在地下水中却不多;有的元素如Cl等在地壳中极少,但在地下水中却大量存在。这是因为各种元素的溶解度不同的缘故。所有这些元素都是以离子、化合物分子和气体状态存在于地下水中的,并且以离子状态为主。
地下水中含有数十种离子成分,常见的阳离子主要有:![]() 及Fe2+等,阴离子主要有:
及Fe2+等,阴离子主要有:![]() 及
及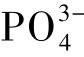 等,但一般情况下在地下水化学成分中占主要地位的是以下6种离子:
等,但一般情况下在地下水化学成分中占主要地位的是以下6种离子:![]() 离子。它们决定了地下水化学成分的基本类型和特点,是人们评价地下水化学成分的主要项目。
离子。它们决定了地下水化学成分的基本类型和特点,是人们评价地下水化学成分的主要项目。
地下水中溶解的气体有N2,O2,CO2,H2S,CH4及Rn等。一般情况下,地下水的气体含量不高,每升只有几毫克到几十毫克。地下水中的氧气和氮气主要来源于大气,它们随着大气降水及地表水补给地下水。硫化氢是在缺氧的环境中由于微生物的作用,将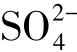 4还原成H2S的。CO2来源于大气中的CO2,或有机物氧化以及深部碳酸盐岩石在高温下分解而成。
4还原成H2S的。CO2来源于大气中的CO2,或有机物氧化以及深部碳酸盐岩石在高温下分解而成。
以碳、氢、氧为主的有机质,经常以胶体方式存在于地下水中。大量有机质的存在,有利于进行还原作用,从而使地下水化学成分发生变化。很难以离子状态溶于水的化合物也往往以胶体状态存在于地下水中,其中分布最广的是Fe(OH)2,Al(OH)3及SO2。
2)氢离子浓度(pH值)
地下水酸碱度用氢离子浓度或pH值来衡量。地下水的氢离子浓度主要取决于水中的![]() 和H2CO3的数量。pH值是水中氢离子浓度的负对数值,即pH=lg[H+]。纯水中,H+和OH-的浓度是相等的,即[H+]=[OH-]=10-7,pH=7,水呈中性。水中H+的离子浓度大于OH-的浓度,即pH<7时,水呈酸性;水中H+的离子浓度小于OH-的浓度,即pH>7时,水呈碱性。自然界中大多数地下水的pH值为6.5~8.5。根据pH值可将水分为五类,见表6.4。
和H2CO3的数量。pH值是水中氢离子浓度的负对数值,即pH=lg[H+]。纯水中,H+和OH-的浓度是相等的,即[H+]=[OH-]=10-7,pH=7,水呈中性。水中H+的离子浓度大于OH-的浓度,即pH<7时,水呈酸性;水中H+的离子浓度小于OH-的浓度,即pH>7时,水呈碱性。自然界中大多数地下水的pH值为6.5~8.5。根据pH值可将水分为五类,见表6.4。
表6.4 按pH值划分水的类型
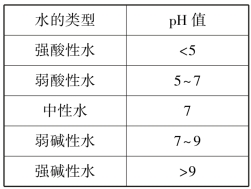
3)总矿化度
地下水中所含各种离子、分子与化合物(不包括气体)之总和称为地下水的总矿化度,以g/L表示来水的矿化程度。通常以在105~110℃温度下蒸干后所得的干涸残余物的含量来确定。根据矿化程度可将水分为5类,见表6.5。(https://www.daowen.com)
表6.5 水按矿化度的分类单位:g/L
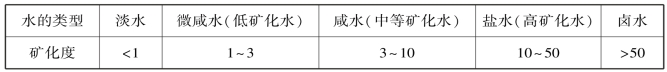
矿化度与水的化学成分之间有密切的关系:淡水和微咸水常以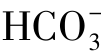 为主要成分,称重碳酸盐水;咸水常以
为主要成分,称重碳酸盐水;咸水常以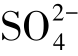 为主要成分,称硫酸盐水;盐水和卤水则往往以Cl-为主要成分,称氯化物水。
为主要成分,称硫酸盐水;盐水和卤水则往往以Cl-为主要成分,称氯化物水。
高矿化水能降低混凝土的强度,腐蚀钢筋,促使混凝土分解,故拌合混凝土时不允许用高矿化水。高矿化水中的混凝土建筑应注意采取保护措施。
4)硬度
地下水中钙镁离子的含量是以硬度来表征的。地下水中Ca2+和Mg2+的含量超出一定指标时,如作为生活和工业用水都有不良影响:会使肥皂去污力下降;在锅炉中成垢,水垢不易传热,浪费燃料,甚至会因传热不均而引起爆炸。因此人们对水中的Ca2+,Mg2+含量给予了高度的重视。水中Ca2+,Mg2+含量的多少用“硬度”来表示。
硬度的大小,我国目前广泛采用德国度(H°)表示方法。一个德国度相当于1L水中含有10mgCaO或7.2mgMgO。
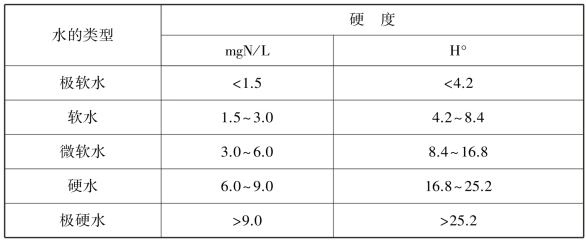
由于1L水中含28mgCaO相当于1mg当量,所以,1mg当量的硬度相当于以德国度表示的硬度2.8度,于是,知道了Ca2+,Mg2+的毫克当量数后再乘以2.8,即可换算成德国度。地下水按硬度可分为5类,见表6.6。
表6.6 地下水按硬度分类
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





