
一、法规框架
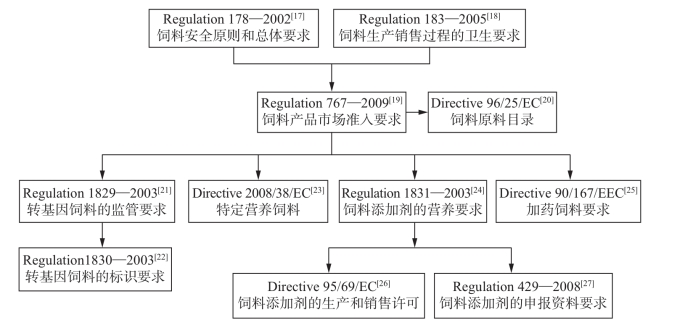
图8-2 欧盟饲料与饲料添加剂的法规框架
饲料与饲料添加剂首先必须满足Regulation 178—2002的总体安全要求和Regulation 183—2005的卫生要求方可进入欧盟市场,欧盟对饲料与饲料添加剂的监管兼顾供食动物与非供食动物(包括宠物),欧洲食品安全局(EFSA)是饲料与饲料添加剂的监管机构。
根据Directive 96/25/EC饲料原料可分为下列12大类:①谷物类产品及副产品;②油籽、油果类产品及副产品;③豆科植物种子类产品及副产品;④块茎、根类产品及副产品;⑤其他种子、果子类产品及副产品;⑥牧草及粗饲料;⑦其他植物类产品和副产品;⑧奶产品;⑨陆生动物产品;⑩鱼和海洋动物产品及副产品; 矿物质;
矿物质; 杂类产品。其代码的编码方式与食品添加剂类似。根据Regulation 767—2009,欧盟专门汇编了饲料原料目录,该目录包含原料代码、原料名称、原料详细描述及必须标识的成分含量,该目录本身是非强制性的,但必须标识成分含量的要求是强制性的。
杂类产品。其代码的编码方式与食品添加剂类似。根据Regulation 767—2009,欧盟专门汇编了饲料原料目录,该目录包含原料代码、原料名称、原料详细描述及必须标识的成分含量,该目录本身是非强制性的,但必须标识成分含量的要求是强制性的。
根据Regulation 1831—2003饲料添加剂分为4大组22小类,详见表8-1。
表8-1 饲料添加剂分类
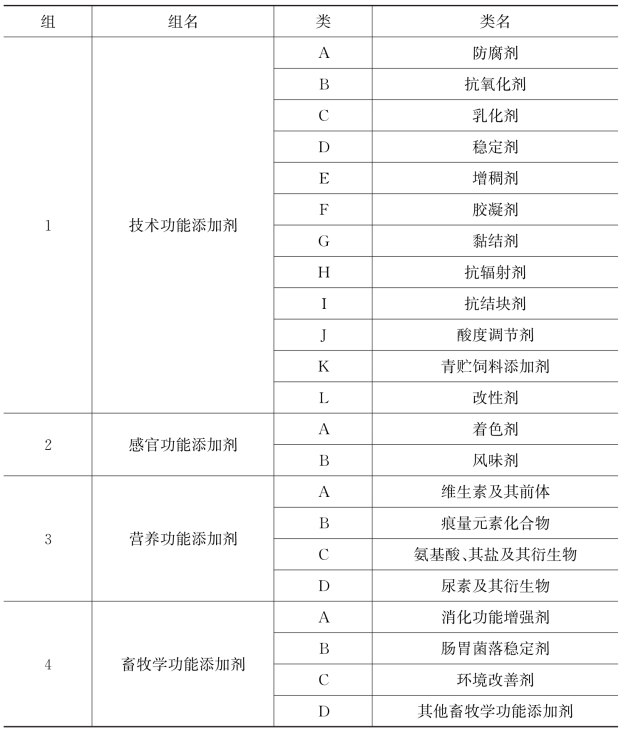
基于企业申请登记的结果,欧盟将获得批准的饲料添加剂汇编成Regulation 1831—2003的附录。原来的第5组球虫和组织滴虫抑制剂已于2012年禁止成为饲料添加剂,抗生素在欧盟禁止其成为饲料添加剂。
二、新饲料成分的申请与审批
根据Regulation 767—2009饲料原料目录是非强制性目录,除饲料禁用成分外,如果要使用目录中未列入的新原料必须立即向欧盟饲料商业委员会通报,该委员会会根据用户意见、欧洲食品安全局(EFSA)及科学技术依据决定是否更新目录。
根据Regulation 1831—2003,任何人不得使用未经批准的或用途未经批准的饲料添加剂。新饲料添加剂和新饲料添加剂用途必须经申报并获得批准后,其产品方可投放市场。对畜牧学功能添加剂和使用转基因(GMO)成分作为饲料成分的,只有申报者才有权将产品投放市场。
申请人必须向欧盟委员会递交如下资料信息方可申请,详细资料要求及格式见Regulation 429—2008的附录。
(1)申请人名称及地址;
(2)新饲料添加剂名称、功能、规格要求;
(3)详细生产工艺描述、饲料及食物中该添加剂鉴定方法;
(4)饲料添加剂安全数据资料;
(5)使用条件、方法、用量及标识内容;
(6)三个备检样品及送检信息;
(7)是否含有GMO成分信息及是否需要入市后监控;
(8)上述各部分的总结;
(9)如含有GMO成分,该成分的生产是否获得批准的信息。
基于由欧盟委员会转交的资料信息,EFSA会对该饲料添加剂或新用途进行风险评估,并做出是否对该添加剂或新用途批准的决定。
根据Regulation 178—2002和Regulation 183—2005的法规要求,任何从事生产、储运及销售饲料或饲料添加剂的企业必须事前在欧盟成员国主管当局登记注册后方可从事相关业务活动。
根据Regulation 183—2005和Directive 95/69/EC的规定,从事生产及销售饲料添加剂相关产品的,除了在成员国主管当局登记注册外,还必须获得主管当局批准后方可进行相关业务活动。获得批准的最低要求如下。
(1)生产设施:能满足生产饲料添加剂相关产品的要求,确保能避免污染及交叉污染的发生,能确保最终产品的质量。
(2)生产相关人员:具备相关的教育程度及职业技能,理解并履行自己的职责,能确保最终产品的质量。
(3)生产工艺过程:生产过程必须按工艺要求进行,整个过程必须按要求监控。
(4)质量管理:生产场所必须有完备的质量管理体系,从原料、生产过程,到最终产品严格按质量要求进行监控管理。
(5)储存:原材料及成品必须按规格要求检验入库,储存场所必须具备必要的储存体条件,储存时物料标识清晰,防止混淆及交叉污染。(www.daowen.com)
(6)文件资料管理:所有相关文件资料必须管控,确保饲料添加剂产品可以追溯,欧盟对该生产的监管要求明确。
(7)经销商管理:确保产品到达用户前完整。
(8)客户投诉管理及产品召回:有完整的客户投诉处理机制及能确保将产品召回的机制。
欧盟境外企业从事饲料或饲料添加剂生产及销售活动的,必须由欧盟内代理机构履行境内企业相同的登记及许可要求。
四、产品标识
根据Regulation 767—2009的规定,饲料与饲料添加剂标识的原则是:在产品特性、用途、生产方法、质量、数量、保质期及适用动物对象上不允许误导用户,尤其不允许暗示产品不具有的特性。
饲料产品基本标识要求为:①必须区分饲料原料、复合饲料及补充饲料;②生产商名称及地址;③相关生产登记和/或批准号码;④生产批号;⑤净容量;⑥所含饲料添加剂及含量;⑦水分含量。
饲料原料除基本标识要求外还必须标识下述内容:①原料名称及代码;②原料目录中必须标识的成分含量;③适用动物;④使用方法;⑤除技术功能添加剂外其他添加剂的保质期。
复合饲料除基本标识要求外还必须标识下述内容:①适用动物;②使用方法;③保质期;④原料成分组成;⑤原料目录中必须标识的成分含量。
特定营养目的的饲料除基本标识要求外还必须按Directive 2008/38/EC的规定进行标识。
宠物饲料除基本标识要求外还必须标识特定的联系电话号码以便于用户了解特定信息。
根据Regulation 1831—2003的规定,饲料添加剂必须标识如下内容:①批准的饲料添加剂的名称;②生产商名称及地址;③净容量;④相关生产登记和/或批准号码;⑤使用方法、适用动物生产;⑥添加剂的识别号码;⑦批号及生产日期。
除此,饲料添加剂还必须标明功能组别,如是添加剂预混料必须清晰标明。
五、转基因产品的监管
根据Regulation 1829—2003的规定,在欧盟转基因饲料指的是含有转基因成分、由转基因成分构成或来源于转基因产物但不含有转基因成分的饲料。
转基因饲料不得损害动物健康、人体健康和环境,不能误导用户、不能通过损害动物产品的特性来损害和误导消费者,转基因饲料与同类非转基因饲料不得有差别。未经批准任何人不得生产销售转基因饲料,转基因饲料必须充分满足Regulation 178—2002规定的安全要求方可获得批准。
为获得转基因饲料的批准,申请者必须向成员国及主管机构递交如下资料:
(1)申请者名称及地址;
(2)饲料名称及规格;
(3)转基因活体成分信息;
(4)详细生产工艺、饲料用途;
(5)所有确保饲料安全性的研究试验资料;
(6)与非转基因饲料无区别的分析方法;
(7)申明不会引起伦理或宗教关注的理由;
(8)投放市场的条件及使用方法;
(9)样品采集及转基因成分的鉴定方法;
(10)对照样品的可获取性;
(11)上市后监控的机制;
(12)标准的案宗格式。
转基因饲料的申请必须标明是否是含有转基因成分、由转基因成分构成或来源于转基因产物但不含有转基因成分的饲料。基于递交的资料,EFSA会对该转基因饲料进行风险评估,并作出是否批准该转基因饲料的决定。
根据Regulation 1830—2003和Regulation 1830—2003的规定,当转基因饲料中转基因成分含量低于0.9%时,可以不标注,除此外,任何转基因饲料必须标明GMO信息。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






