1.结晶和重结晶
结晶和重结晶是从液体中分离溶解固体的一种实验技术,用于产品的提纯和杂质的去除。结晶是用于产品的初步分离,重结晶则是用于固体样品的提纯工序。
结晶是指在溶液溶质形成晶体的过程,其原理是利用不同的物质在同一种溶剂中的溶解度不同而进行的固体间的分离。其结晶方法一般有三种:蒸发结晶、冷却结晶和升温结晶。蒸发结晶是通过蒸发而汽化掉一部分溶剂,使得溶质达到饱和而结晶。一般用于溶质的溶解度随温度变化不大,而杂质的量较少在蒸发过程中不会达到饱和的体系中,分离氯化钠和碳酸钾等工艺就是利用蒸发结晶来进行的。冷却结晶一般用于溶质随温度降低溶解度大幅降低的体系,应用时一般采用加热蒸发浓缩后再降温的手段,使得温度变化大而使结晶顺利进行。利用此原理分离的有硝酸钾和硫酸镁等的分离。升温结晶适用于一些溶质其溶解度随着温度升高而降低的体系,如从饱和石灰水中析出氢氧化钙,后续需要进行趁热过滤。
除去以上三种结晶方法,若遇到难以分离的物质还可以通过加入与原溶剂互溶的第二溶剂降低溶质的溶解度来促成结晶,以及加入晶种来诱导结晶等措施来完成结晶过程。在操作结晶过程时还要注意过饱和度、温度、搅拌速度等操作条件对结晶晶体大小的影响,控制参数得到理想尺寸的晶体。
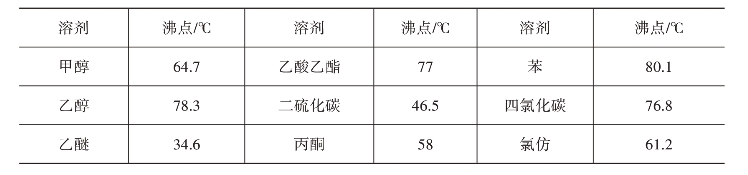
重结晶是指将结晶出来的晶体重新溶解在适当的溶剂中,再经过加热、蒸发、冷却等步骤重新得到晶体的过程。其原理是利用杂质和溶质在不同溶剂不同温度下的溶解度不同,将晶体用合适的溶剂进行再次结晶而得到高纯晶体。在此工艺中选择合适的溶剂至关重要,一般来说一种理想的溶剂需要符合以下条件:第一,不与被提纯的物质发生化学反应;第二,在较高温度时能溶解大量的被提纯物质,而在室温或者低温时只能溶解少量的提纯物质;第三,体系中杂质在溶剂中的溶解度极小或者极大,溶解度极小时需要将杂质在溶剂热过滤时被滤去,而溶解度极大时需要将杂质留在溶剂母液中不被析出;第三,溶剂的沸点低(一般选择在50℃~85℃)且容易挥发,与结晶物分离容易;第四,无毒或者毒性很小,廉价易得。表1-4中列出了重结晶中常用溶剂的沸点。
表1-4 重结晶中常用溶剂的沸点
2.离子交换技术
离子交换技术是对特定物质通过离子交换和吸附的作用,达到分离、置换、浓缩以及提纯等效果的。一般是采用具有功能团的不溶性高分子化合物也就是高分子树脂,其结构是由高分子骨架、离子交换基团和空穴三部分所组成。一般来说离子交换树脂可以按照以下几种方法分类:第一种,按物理结构分类的孔径为5 nm的凝胶型树脂和孔径为20~100 nm的大孔型树脂;第二种,按树脂所用原料单体分类的酚醛系列、苯乙烯系列、丙烯酸系列、乙烯吡啶系列和环氧系列等;第三种,按照树脂的离子交换功能团分,如弱酸性阳离子交换树脂、强酸性阳离子交换树脂、弱碱性阴离子交换树脂和强碱性阴离子交换树脂,这种分类是最常见的分类。还有一些特殊的离子交换树脂,如螯合树脂、氧化还原树脂、电子交换树脂等。
其分离过程是在离子交换容器内,装填一定高度的离子交换树脂,当含有某一金属离子的水溶液流过时,容器内的特殊树脂吸附其中金属离子的过程。以Y型沸石分子筛的离子交换为例,当水溶液中存在HCl时,发生的交换反应如下所示:
![]()
离子交换技术一般用于水中盐类的去除,水中的阳离子与阳树脂的H+离子进行离子交换,而水中的阴离子与阴树脂的OH-离子进行离子交换,从而达到脱盐的目的。除了脱盐水和软化水,离子交换技术还可以用于贵重金属的分离、维生素的提纯、饮料糖浆的脱色等等。图1-23是水处理设备中的离子交换柱。

图1-23 水处理设备中的离子交换柱
由于离子交换反应的可逆性,离子交换树脂在应用失效后,可用酸、碱或其他再生剂进行再生,恢复其交换能力,从而使得离子交换树脂能够长期反复地使用,这一性质是离子交换技术最重要的。
3.膜分离技术
膜分离技术指的是利用天然的或者人工合成的具有选择透过性的膜,在外界能量或者化学位差作为推动力对双组分或者多组分的溶质或者溶剂进行分离、分级、富集和提纯的技术。
可用来进行分离的膜可分为以下几个种类:高分子膜、液体膜和生物膜。其中高分子膜又可以分为带电的阳离子膜和阴离子膜以及不带电的膜(如过滤膜、超滤膜、纳米滤膜、反渗透膜等)。常见的高分子有机膜有纤维素脂类、聚酚类、聚酰胺类等。大概有一百多种高分子有机膜已经被合成制备出来,有四十多种已经被工业中应用,其中纤维素脂类膜的应用最广。(www.daowen.com)
膜分离技术在工业中的发展很早,早在20世纪50年代初为了在海水中提取淡水,就开始了对反渗透膜的研究,在20世纪60年代已经实现了工业化。首先在工业中出现的分离膜是超过滤膜(简称UF膜)、微孔过滤膜(简称MF膜)和反渗透膜(简称RO膜)。在20世纪80年代研制成功了气体分离膜,使得功能膜的地位也进一步提高。
膜分离技术有其特有的优点:第一,由于膜分离过程不同于蒸馏、结晶以及蒸发过程,不涉及相变,所以分离过程能量损耗低;第二,分离一般在常温下进行,所以对于一些热敏性物质的分离很有优势,有效成分容易保持;第三,膜分离组件一般结构紧凑,操作方便且维修成本低,容易自动化。图1-24是膜分离的原理图和膜组件图。
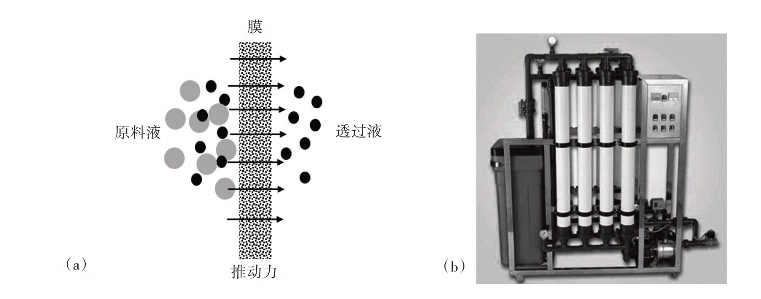
图1-24 膜分离技术原理图和膜组件设备图(a)原理图(b)膜组件设备图
(a)原理图(b)膜组件设备图
4.色谱技术
色谱技术用于分离提纯化合物一般称为层析分离法,是目前分离有机物或生化物质应用最广泛的一种手段。色谱法分离物质具有选择性好、分辨率高、分离设备简单易得、分离条件温和、操作方便等优势。
其基本原理是利用待分离物各组分的溶解度、吸附能力、立体化学特性、分子大小、带电情况、离子交换作用大小及特异的生物学反应的差异,使其在流动相与固定相之间的分配系数不同,随流动相在固定相中前进速度的不同而得到不同分布程度的色谱带而进行分离和检测的。与固定相相互作用力弱的组分,在移动时受到的阻力小,移动的速度相对较快;与固定相的相互作用力大的组分,在移动时受到的阻力大,移动的速度相对慢。在实验时通过分步收集流出液,就可以得到样品中的某一单一组分。
在一定的温度和压力下,当色谱分离过程达到平衡状态时,决定分离的主要参数分配系数可用下式来表示:
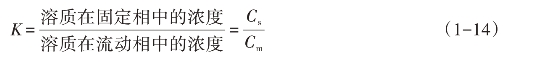
分配系数K是由组分和固定相的热力学性质决定的,它是某一个溶质的特征值,只与固定相和分离温度这两个参量有关,而与固定相和流动相的体积以及分离管柱的特性等无关。一般情况下,温度和分配系数成反比。
样品中各组分的K值的差异决定了色谱分离的效果,一般情况下,K值小的溶质,表示其在固定相中的浓度小,在洗脱过程中出现的时间较早;而K值大的表示其在固定相中的浓度大,在洗脱过程中出现的时间较晚。
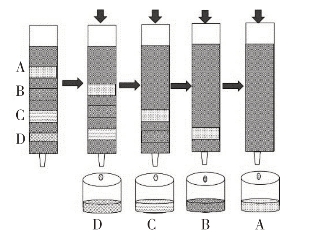
图1-25 色谱柱分离示意图
在操作中可以对色谱技术进行分类:第一类,是利用滤纸作为载体,点样后用流动相展开使各组分分离;第二类,是将适当的基质在玻璃或是塑料等光滑表面上均匀涂铺成薄层,作为固定相,点样后利用流动相展开后进行色谱分离;第三类,是将固定相装载到色谱管中,在顶端加入样品和流动相,在柱中进行色谱分离。其中第三类分离方法应用最广,实验室中多采用玻璃的色谱柱。而在工业生产中一般采用内壁光滑的不锈钢色谱柱,为了便于观察,会在管壁上设置可视的玻璃段。图1-25是色谱柱分离示意图。色谱柱中经常使用的吸附剂有活性炭、碳酸钙、氧化铝、硅胶和氧化镁等。其中活性炭吸附剂由于粒径太小而且吸附能力很强,一般只用于杂质含量较低的体系,用途不是太广。氧化铝吸附剂由于可以作为酸性吸附剂、碱性吸附剂和中性吸附剂来使用,所以是应用最广的一类吸附剂。有机酸的分离一般要用到pH为4~5的酸性氧化铝;醛、酮和脂类的化合物一般要用到pH为7.5的中性氧化铝吸附剂;生物碱、胺和碳氢化合物等碱性物质就要用到pH为9~10的氧化铝吸附剂了。对于一些带有多种官能团的物质(如天然产物),由于其对弱酸和弱碱都很敏感,所以可以选用天然的纤维素或者淀粉来分离。
选择好适当的分离吸附剂后,下一步的洗淋剂的作用就是将被分离物质从吸附剂上洗脱下来。淋洗剂的极性和对被分离物质的溶解度大小对于分离效果非常重要。在具体操作时,通常是极性的物质需要用低活性的吸附剂和强极性的淋洗剂,而非极性的物质需要用高活性的吸附剂和非极性的淋洗剂来进行。极性小的溶剂可以选择正己烷、石油醚、四氯化碳、苯、氯仿等;极性强的溶剂有甲醇、乙醇、丙酮、乙酸乙酯等。使用时为了便于回收最好采用一种溶剂,若没有合适的溶剂可以使用两种或者两种以上的混合溶剂。混合溶剂的配比需要在薄层板上进行试验,从而找出最佳配比进行使用。
在实际操作时,由于可对被分离物质的成分大概估计,所以在选择吸附剂和洗淋剂时,可根据其各组分分子结构估计其吸附能力,选择合适的吸附剂、洗淋剂和所需的分离柱尺寸。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







