在前面的分析中,已经使用了晶体结构中的一些概念,比如硅原子之间的相互位置、晶格常数等,因此有必要对半导体的晶格结构进行简单的说明,这对半导体物理基础的进一步了解和掌握有帮助。
固体有晶体和非晶体之分。晶体具有一定的外形、固定的熔点,更重要的是组成晶体的原子(或离子)至少是在μm量级的较大范围内都是按一定的方式规则排列而成的。晶体又分为单晶与多晶,单晶是指整个晶体主要由原子(或离子)的一种规则排列方式所贯穿,常用的半导体材料硅、锗、砷化镓等都是单晶。其中硅和锗为元素半导体,砷化镓称为化合物半导体。多晶则是由很多小晶粒(每个可以看成单晶)杂乱地堆积而成的。除晶态半导体外,尚有非晶态半导体,如非晶态硅、非晶态锗等,它们没有规则的外形,也没有在μm量级的较大范围内都是按一定的方式规则排列,只是在若干原子间距内的较小范围内存在结构上的有序排列。二维情形下的非晶、多晶和单晶示意图如图2-13所示。
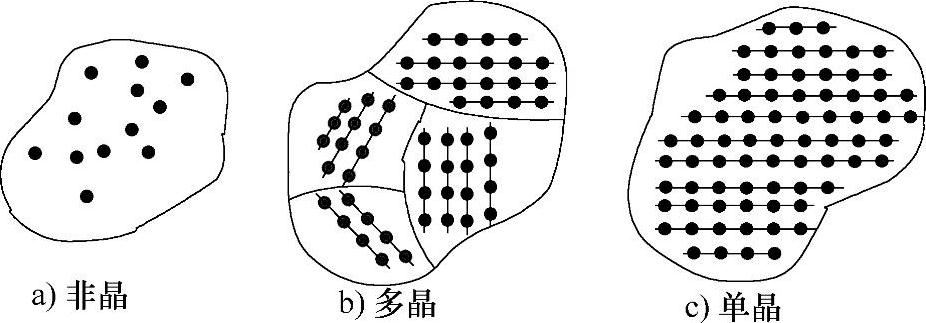
图2-13 非晶、多晶和单晶的示意图
对于单晶硅来说,它由硅原子组成,通过两个原子间共有一对自旋相反配对的价电子把原子结合成晶体。如前所述,这种依靠共有自旋相反配对的价电子所形成的原子间的结合力,称为共价键。由共价键结合而成的晶体称为共价晶体,硅和锗都是典型的共价晶体。共价键具有饱和性和方向性。饱和性是指每个原子与周围原子之间的共价键数目有一定的限制。硅和锗等Ⅳ族元素有4个未配对的价电子,每个原子只能与周围4个原子共价键合,使每个原子的最外层都成为8个电子的闭合壳层,因此共价晶体的配位数(即晶体中一个原子最邻近的原子数)只能是4。方向性是指原子间形成共价键时,电子云的重叠在空间一定方向上具有最高密度,这个方向就是共价键方向。共价键方向是四面体对称的,即共价键是从正四面体中心原子出发指向它的四个顶角原子,共价键之间的夹角为109°,这种正四面体称为共价四面体,显然其是正四面体,在几何领域中也称为阿基米德固体,如图2-14a所示。如果将其放置到一个正方体中,将一个硅原子放置到正方体的中心位置,其他4个硅原子放置到正方体的顶点,则可以形成如图2-14b所示的情况。
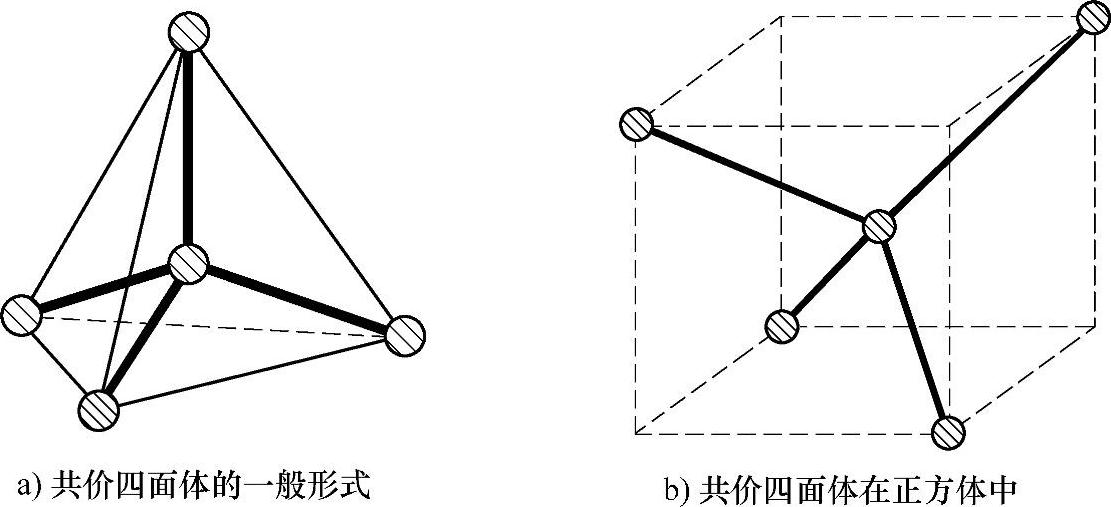
图2-14 Ⅳ族元素共价结构示意图
图2-14中,原子间的连线表示共有一对价电子,线的方向表示共价键方向。共价四面体中,如果把原子粗略看成圆球,并且最邻近的原子彼此相切,圆球半径就称为共价四面体半径。单纯依靠图2-14那样的一个四面体还不能表示出各个四面体之间的相互关系,为充分展示共价晶体的结构特点,图2-15画出了由多个共价四面体所组成的一个硅晶体结构的晶胞(或称为元胞),称为金刚石结构晶胞,它是一个正立方体,整个硅晶体就是由这样的晶胞周期性重复排列而成的。不难发现,金刚石结构晶胞中有8个原子。该正立方体的边长称为晶格常数,图中用a来表示。表2-4给出了几种金刚石结构晶胞的晶格常数。
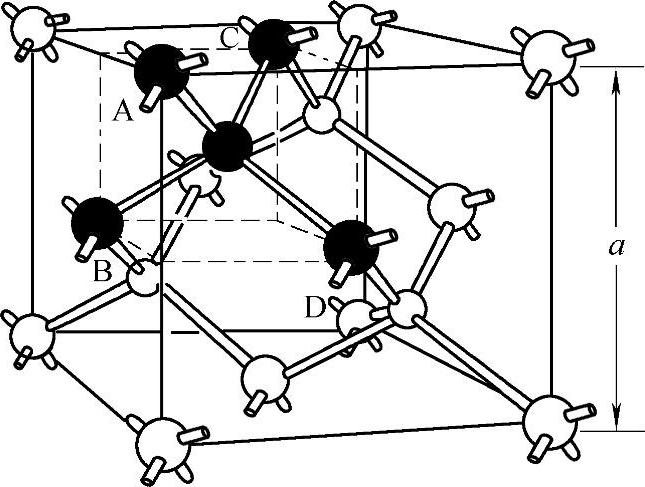
图2-15 硅的晶胞示意图
表2-4 几种金刚石结构晶胞的晶格常数

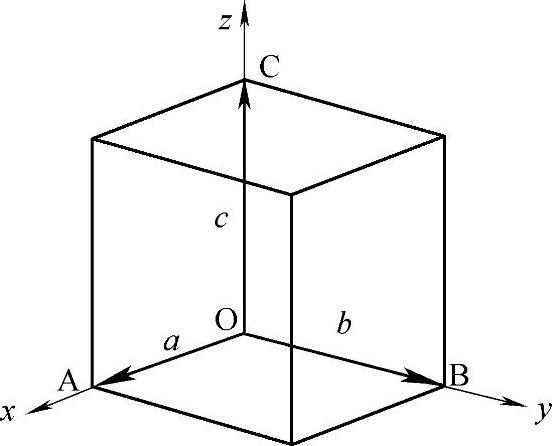
图2-16 晶体的晶轴
由此可以简单推算出晶体中硅原子浓度为
N0=8/a3=[8/(5.43×10-10)3]m-3=5.0×1028/m3 (2-12)
晶体是由晶胞周期性重复排列构成的,整个晶体就像网格,称为晶格,组成晶体的原子(或离子)的重心位置称为格点,格点的总体称为点阵。对硅这种具有金刚石结构的立方晶系,通常取某个格点为原点,再取立方晶胞的三个互相垂直的边OA、OB和OC为三个坐标轴,称为晶轴,则硅的晶胞可如图2-16所示,图中OA、OB和OC长度就是晶格常数a,一般以a作为晶轴的长度单位。OA、OB和OC称为晶胞的三个基本矢量,用a、b、c表示。(https://www.daowen.com)
通过晶格中任意两格点可以作一条直线,而且通过其他格点还可以作出很多条与它彼此平行的直线,而晶格中的所有格点全部位于这一系列相互平行的直线系上,这些直线系称为晶列,晶列的取向称为晶向。晶格中的所有格点也可看成全部位于一系列相互平行等距的平面系上,这样的平面系称为晶面族。
在硅的晶体中,有3个晶面和3个晶向是最重要的。图2-17画出了立方晶系的这些晶面和晶向。图中,数字相同的晶面和晶向是垂直的,比如(100)垂直于[100],(111)垂直于[111]。
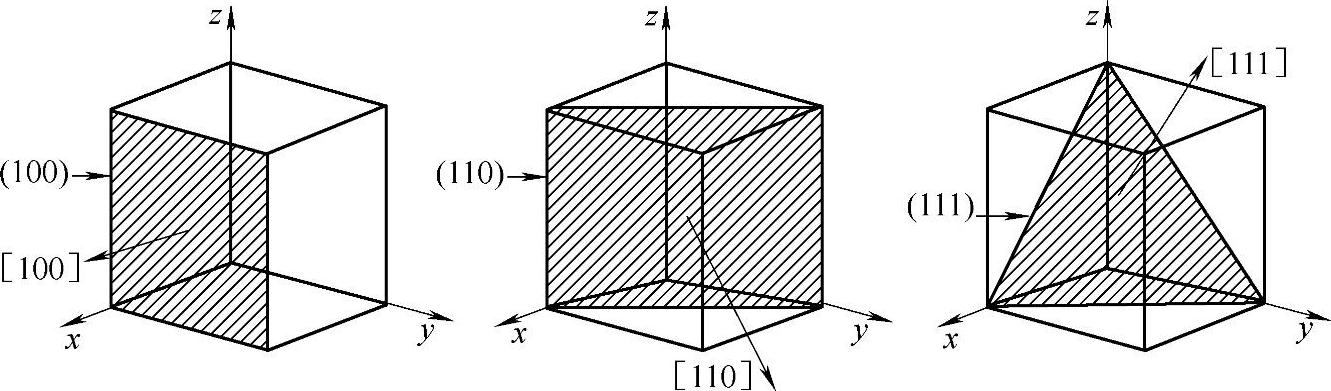
图2-17 晶体中重要的3个晶向和3个晶面
在图2-17中,(100)面可以是立方体的任意一个表面。(110)面包含立方体的两条边,并且沿着面对角线将立方体切割成相同的两部分。沿一个顶点和最远的两个顶点切割立方体的面是(111)面。[100]、[110]和[111]这3个晶向分别垂直于对应的晶面。[100]这个晶向数学上可以用方向R来表达
R=[1,0,0]*[a,b,c]T
显然,在此晶体中存在多个晶向,其中有很多是等价的晶向,可分成3类等价晶向,使用尖括号来表示,罗列如下:
<100>代表了[100]、[010]、[001]、[-100]、[0-10]和[00-1]6个等价的晶向;
<110>代表了[110]、[011]、[101]、[-110]、[0-11]、[10-1]、[-1-10]、[0-1-1]、[-10-1]、[1-10]、[01-1]和[-101]12个等价的晶向;
<111>代表了[111]、[11-1]、[1-11]、[-111]、[1-1-1]、[-11-1]、[-1-11]和[-1-1-1]8个等价的晶向。
这样,任何一个<100>晶向都是沿着立方体的某一条边,任何一个<110>晶向都是对角穿过立方体,并且平行于晶体的某一个面,任何一个<111>晶向都是沿立方体的体对角线方向。这些晶面和晶向对于制作半导体器件是很重要的。借助于更生动的图形表达方式,图2-18中的透视图举例说明了立方晶体的三个重要的不同种类的平面。
在硅材料的加工中,有各种各样的试剂都可以腐蚀硅。其中一些通常为快速腐蚀的试剂,易于忽略原子平面的存在。设想将一块硅通过某种保护材料层的一个小的环形开口暴露在一种上述试剂中的情况,保护层并不接触到腐蚀剂。此时,所产生的不断增加的凹陷趋向为一个球形表面形状。这样的蚀刻剂称为各向同性的蚀刻剂。各向同性的反义词是各向异性,这为慢反应刻蚀剂优先去除结合较弱的原子而不去除结合较强的原子提供了条件。结果是推进的表面形成了不同于结晶平面的小平面。在硅(或金刚石和四面体)结构中,(111)面具有不寻常的高原子密度,从图2-15就可以发现这一点。设想含有原子A、B和C的(111)面的情况。注意在数量上与该平面所包含的原子A、B和C的数目相等的X原子及其相关原子构成与该平面非常接近的第二个(111)平面。结合X原子和D原子的共价键与那些(111)平面相垂直。于是D原子和所示的其他两个面心原子形成了另一个(111)面,它和X原子平面的间距是共价键的全长。还有一个与D原子平面非常接近的另一个(111)面。因此这些(111)平面的图形是间隔很小并且牢固结合的两个平面(遵从平面间共价键密度),紧接着是一个伴有低共价键密度的相对较大间距。于是,有可能沿着两对(111)平面之间的表面劈开硅晶体。这一方法已经大量地用在将包含数百个集成电路的硅片划成单个集成电路(或在初期划成单个晶体管)的加工中。注意图2-15中,如果开始划片的表面构成一个(110)面,那么被打破的(111)面的边缘将垂直于“晶片”或者被叫做管芯的更小的单个晶片的表面。有时选择这种取向,便于自动化加工。在制造晶闸管这种大尺寸和大电流的电力半导体器件和制造MOSFET这种小尺寸和小电流的器件,同样选择硅晶体,选取的晶向有所不同。因为涉及半导体加工工艺,在此不进行展开分析。
在这里着重分析具有金刚石结构的元素晶体。而在周期表中的Ⅲ族和一个Ⅴ族元素同样可能组成化合物晶体的结构,一般称其为闪锌矿结构,此时也可以得到外壳层电子总数为8。有很多这样的化合物晶体,并不局限于Ⅲ族和Ⅴ族的组合,除了Ⅲ-Ⅴ族组合的砷化镓外,还可以有Ⅳ-Ⅳ族组合的碳化硅,以及Ⅱ-Ⅵ族组合的硫化锌等,它们也都是闪锌矿结构。实际上,是由硫化锌提供了硫化锌结构这个名字。从另一个角度说,硫化锌结构是具有共价键和类似图2-15格点构造的所有两种成分结构的统称。值得注意的是,这些化合物晶体的重要性日渐增长。
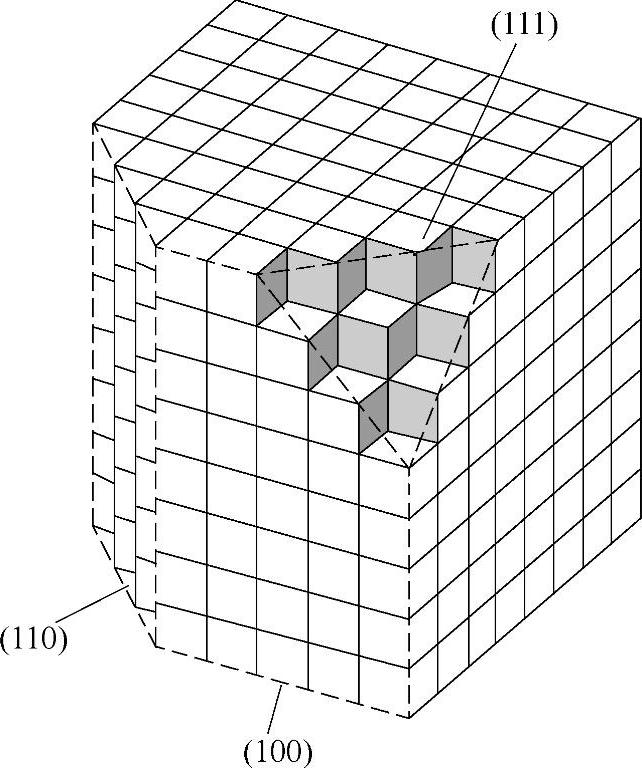
图2-18 三个重要晶面 在晶体上的示意图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






