1.阀控铅蓄电池的密封原理
铅酸蓄电池在充电后期,正极会析出氧气,负极析出氢气,直接造成了电池的水损耗,这是电池不能密封的直接原因。为了使气体少析出或不析,阀控电池采取了以下措施:
1)采用无锑合金,严格控制铁、铀等杂质含量,提高了负极析氢电位,使得负极析氢较困难。
2)采用阴极吸收技术,使超细玻璃纤维隔板处于不饱合吸酸状态,具有一定贫液度,这为气体扩散创造了有利条件,使正极产生的氧气扩散至负极,与海绵状铅产生下列反应:
O2+2Pb→2PbO
PbO+2H2 SO4→PbSO4+2H2 O
PbSO4+2e→Pb+SO42-
这样正极分解水产生的氧气又在负极还原成水。合理设计可以使电池的氧气点合效率达99%以上,基本上没有水的损耗。图5-27为氧循环复合原理示意图。
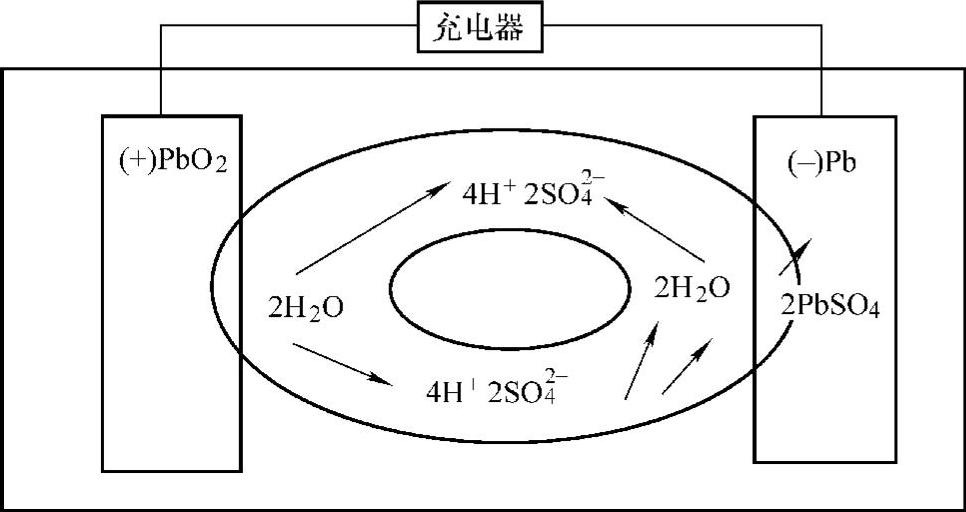
图5-27 氧循环复合原理示意图
O2与Pb的反应使负极去极化,极化电位进一步降低,更有利于抑制氢气在负极的析出,而氧气通过氧循环复合反应又回到体系中。(https://www.daowen.com)
通过以上措施,电池在运行过程基本无气体溢出,也就无水损耗,因此可以实现密封。
2.阀控铅蓄电池的放电
在外电网断电时,蓄电池将放出能量维持供电。蓄电池放电时的化学反应方程式为
PbO2+2H2 SO4+Pb→PbSO4+2H2 O+PbSO4
上式表明:正极板上二氧化铅逐渐变为硫酸铅,负极板上的铅也逐渐变为硫酸铅,电解液中的稀硫酸逐渐变为水,故电解液的密度逐渐下降,蓄电池两端电压也逐渐下降。因此,可以根据蓄电池两端的电压下降的数值,来判定蓄电池的放电深度。一般蓄电池放电终了电压与其放电的快慢有关系:放电快,其终了电压就低;放电慢,其终了电压就高。
蓄电池放电电流越小,蓄电池端电压能维持输出电压稳定的时间越长;放电电流越大,蓄电池维持其输出电压稳定的时间就越短。若蓄电池以0.05C速率放电,放电时间将长达20h;若蓄电池以2C速率放电,则放电时间只有10min。若对一块12V蓄电池以7C的速率放电,接通负荷的瞬间造成蓄电池输出电压由12V降至10.2V,维持10.2V只有20s左右。若在此条件下继续放电,当放电时间超过50s时,蓄电池组的端电压将下降至6V左右,这意味着很有可能造成对蓄电池永久性的损坏。因此,控制好放电电流,尽量避免大电流放电是延长蓄电池寿命的重要因素。
3.阀控铅蓄电池的充电
蓄电池放电终了必须及时充电。蓄电池充电的化学反应方程式为
PbSO2+2H2 O+PbSO4→PbO2+Pb+2H2 SO4
可以看出:蓄电池充电时,正极板上的硫酸铅逐渐变为二氧化铅;负极板上的硫酸铅逐渐变为海绵状铅;电解液中的硫酸分子逐渐增加,水分子逐渐减少,故电解液的密度逐渐增加,蓄电池两端电压逐渐上升。因此,可根据蓄电池两端的电压数值来判断蓄电池充电程度。例如,一块12V蓄电池充电终了电压为13.75V。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







