1.摩尔质量(MB)的计算
(1)摩尔质量的定义 根据GB 3102.8—1993规定,质量m除以物质的量n,称为摩尔质量M,即
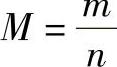
摩尔质量的SI单位为kg/mol,在分析化学中常用g/mol。
可以看出,摩尔质量是一个包含物质的量nB的导出量。因此,在用到摩尔质量这个量时,必须指明基本单元。对于同一物质,选定的基本单元不同,其摩尔质量也不同。
(2)摩尔质量的计算 计算摩尔质量的关键是确定基本单元,基本单元确定之后,摩尔质量是很容易求得的。当采用g/mol作为摩尔质量单位时,任何物质的摩尔质量等于选定基本单元B的相对粒子质量Br,即
MB=Br
当基本单元B是原子时,则Br就是相对原子质量Ar;当B是分子时,则Br就是相对分子质量Mr,依此类推。例如:
基本单元H+的摩尔质量M(H+)=1.008g/mol。
基本单元NaOH的摩尔质量M(NaOH)=40.00g/mol。
基本单元H2SO4的摩尔质量M(H2SO4)=98.08g/mol。
基本单元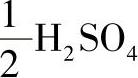 的摩尔质量
的摩尔质量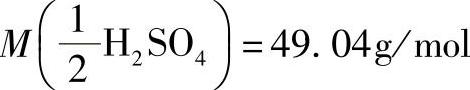 。
。
基本单元KMnO4的摩尔质量M(KMnO4)=158.03g/mol。
基本单元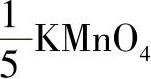 的摩尔质量
的摩尔质量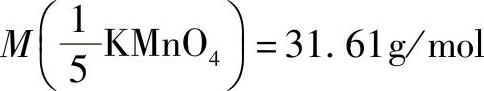 。
。
基本单元K2Cr2O7的摩尔质量M(K2Cr2O7)=294.18g/mol。
基本单元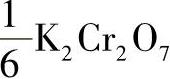 的摩尔质量
的摩尔质量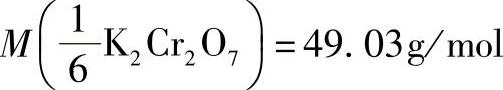 。
。
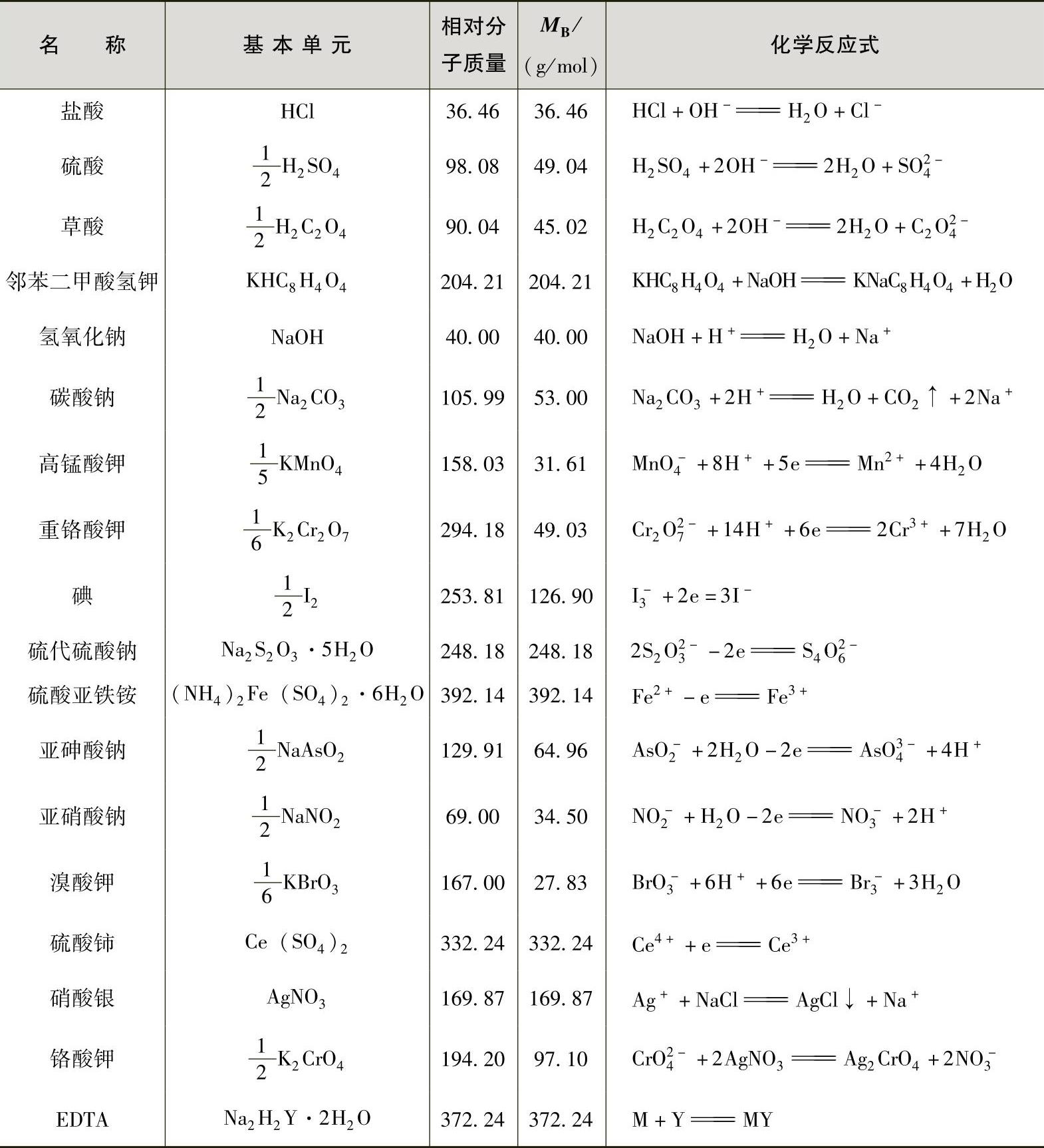
可见,对于同一物质,选定的基本单元不同,其摩尔质量也不同。实验室常用物质的摩尔质量MB见表1-2。表1-2中的MB是按“等物质的量规则”,以习惯和简便为原则确定基本单元进行计算的,使用时应注意。
等物质的量规则是一条很重要的法则,它是滴定分析的理论基础。
表1-2 常用物质的摩尔质量(MB)
在化学反应中,消耗了的两种反应物的物质的量必相等。这就是等物质的量规则,即
nB=nT
或 cBVB=cTVT
或 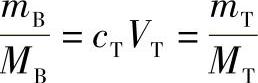
式中 nB、nT——分别表示物质B、物质T的物质的量(mol);
cB、VB——分别表示物质B的物质的量浓度(mol/L)和体积(L);
cT、VT——分别表示物质T的物质的量浓度(mol/L)和体积(L);
mB、MB——分别表示物质B的质量(g)和摩尔质量(g/mol);(https://www.daowen.com)
mT、MT——分别表示物质T的质量(g)和摩尔质量(g/mol)。
等物质的量规则,主要应用于配制标准溶液时的计算和滴定分析结果时的计算。
2.用固体溶质配制物质的量浓度
计算公式为

式中 mB——应称取溶质B的质量(g);
cB——物质B的物质的量浓度(mol/L);
V——欲配制溶液体积(mL);
MB——物质B的摩尔质量(g/mol)。
例4 欲配制0.1mol/L的Na∶H溶液2000mL,应如何操作?
解 已知M(NaOH)=40.00g/mol,将已知数据代入式(1-5)计算:
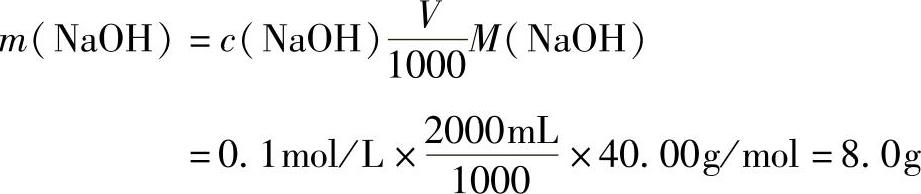
配法:称取NaOH8.0g,溶于水中,冷却后稀释至2000mL,混匀,存放在塑料瓶中备用。
3.用液体溶质配制的物质的量浓度

式中 mB——应称取溶质B的质量(g);
cB——物质B的物质的量浓度(mol/L);
MB——物质B的摩尔质量(g/mol);
V——欲配制溶液体积(mL);
v——应量取液体溶质B的体积(mL);
ρ0——液体溶质的密度(g/mL);
x0%——液体溶质的质量分数。
例5 用密度为1.84g/mL的H2SO4配制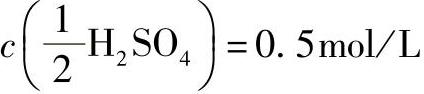 溶液250mL,应如何操作?
溶液250mL,应如何操作?
解ρ0=1.84g/mL的H2SO4的质量分数x0%=98%,其摩尔质量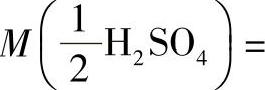
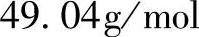 。将已知数据代入式(1-6)和式(1-7)计算:
。将已知数据代入式(1-6)和式(1-7)计算:
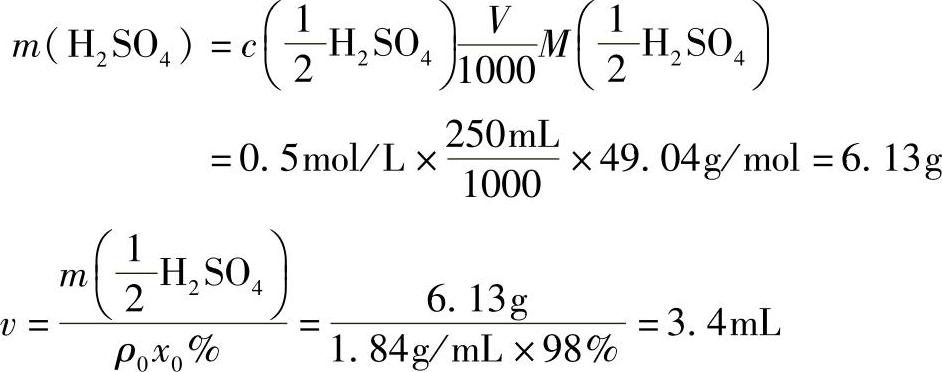
配法:量取浓H2SO43.4mL,缓慢注入水中,冷却后稀释至250mL,混匀。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。



