【摘要】:热力学平衡包括:①热平衡即系统的各部分温度相等,温度梯度为零。在不考虑重力场影响的情况下,力平衡是指各部分的压力相等。综上所述,热力学平衡一般是指系统在一定的条件下,其自由能不可能再进一步地最小化。此时,系统处于热力学平衡态。比如,在恒温、恒压下,系统达到热力学平衡态时,其Gibbs自由能达到此种状态下的最小值。图8.3示意了系统能量随一些状态变量的变化情况。
热力学平衡包括:①热平衡即系统的各部分温度相等,温度梯度为零。②力平衡即系统各部分之间、系统与环境之间没有不平衡力的存在。在不考虑重力场影响的情况下,力平衡是指各部分的压力相等。③相平衡即达到相平衡时,各相的数量、组成不随时间而变。④化学平衡即各物质间有化学反应时,达到平衡后,系统的组成不随时间而变。
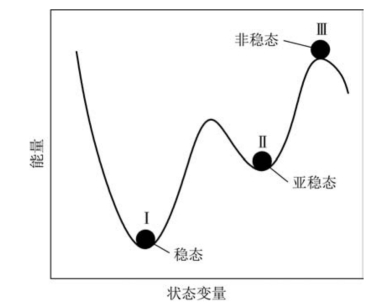
综上所述,热力学平衡一般是指系统在一定的条件下,其自由能不可能再进一步地最小化。此时,系统处于热力学平衡态。比如,在恒温、恒压下,系统达到热力学平衡态时,其Gibbs自由能达到此种状态下的最小值。若在恒温、恒压下,Gibbs自由能未达到此种状态下的最小值,则系统处于亚稳态或不稳态。图8.3示意了系统能量随一些状态变量的变化情况。状态Ⅰ处于最低能量状态。如果状态变量发生波动,则能量可能升高至状态Ⅱ或状态Ⅲ。此时,系统有回到状态Ⅰ的趋势。当能量在状态Ⅲ时,状态变量的一点微小波动,都会使系统向状态Ⅰ或Ⅱ变化,故状态Ⅲ为非稳态。
 (https://www.daowen.com)
(https://www.daowen.com)
图8.3 系统能量分布示意图(引自Mittemeijer,2013)
当系统在状态Ⅱ时,状态变量微小的波动不足以使系统回到状态Ⅰ。只有当状态变量的波动较大时,系统才回到状态Ⅰ。故系统在状态Ⅱ可维持较长时间。状态Ⅱ称为亚稳态或介稳态(metastability)。首次清晰地提出亚稳态概念的是Ostwald。要使系统从状态Ⅱ向状态Ⅰ转变,需提供一定的能量,即要越过一个势垒,这一点我们在玻璃及扩散等章节提到过。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
相关文章





