1.组元特性
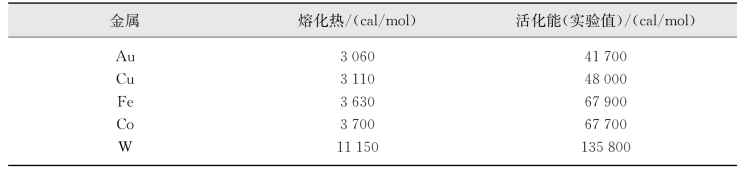
(1)键能。键能大,原子间作用强,则物质的熔点高、熔化热值大。熔化热值大的金属,其原子的自扩散活化能一般也较大,见表7.4。
表7.4 一些金属的熔化热和扩散活化能(引自徐祖耀,1986)

续表
(2)键性。共价键有方向性和饱和性。间隙原子的扩散不利于体系能量的降低。因而,共价键物质的自扩散活化能通常高于熔点相近的金属之活化能。比如,Ag和Ge的熔点接近,Ge主要由共价键结合,其扩散活化能为289 kJ/mol,而Ag的扩散活化能为184 kJ/mol。
(3)原子尺寸。较小的原子容易扩散,如H、B、C等容易在金属的间隙位扩散。在离子晶体中,通常阳离子较小,故阳离子的扩散系数往往大于阴离子的扩散系数。比如,NaCl晶体,其Cl-的扩散活化能约为Na+的两倍。
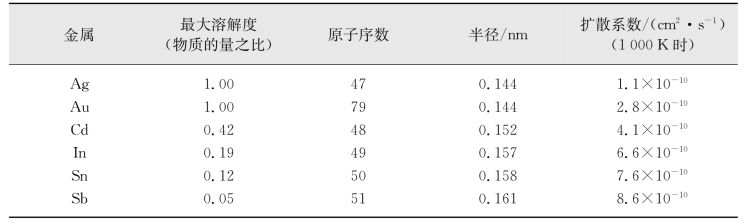
(4)溶解度与原子价。通常固溶体中溶解度较小的元素,其扩散也较容易。表7.5列出了一些元素在Ag中的最大溶解度和扩散系数。实验还表明,在以一价贵金属为溶剂的合金里,原子价大于溶剂的溶质元素,其扩散活化能小于溶剂金属的扩散活化能,并且溶质的原子序数大,活化能小。
表7.5 某些元素在Ag中的扩散系数(引自潘金生,2011)
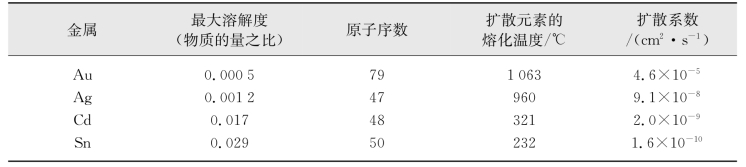
(5)组元间的亲和力。组元间的亲和力大,即电负性相差大。这样,溶质原子与溶剂原子结合力大。结果溶质原子的扩散就困难。如表7.6所示,在Pb中固溶的一些元素,当它们与Pb的性质相差较大时,扩散系数也大,而Pb在Pb中的扩散(相当于亲和力最大),其扩散系数即自扩散系数却很小。
表7.6 一些金属在Pb中的扩散系数(引自张联盟,2008)(www.daowen.com)
续表
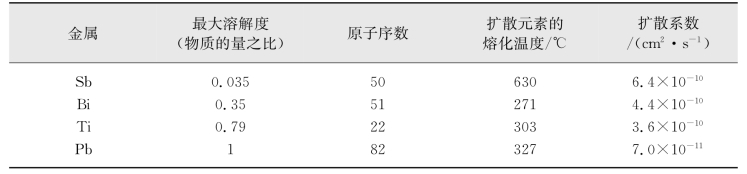
(6)在周期表中离基体元素的距离越远,则往往活化能越低,扩散容易。如表7.5所示,Sb离Ag最远,它在Ag中的扩散系数最大。表7.6也可看出这种趋势。
总的说来,在周期表中,一些离基体元素较远的元素,其扩散较容易。但也不是所有扩散元素都是这样。因而,以上组元间性质对扩散系数的影响还是比较复杂的,人们还不是非常清楚它们对扩散系数的影响。这方面的工作还有待进一步地深入研究。
2.组元浓度
图7.6所示的w-Clnr曲线表明D与浓度c有关。实验数据表明,固溶体中的溶质浓度对扩散系数的影响是通过活化能Ea、指前因子D0这两个参数来起作用的。
通常,活化能Ea增加,D0也增加;Ea减小,D0也减小。但这两个参数的变化并不成比例,而且Ea还处于指数项中。因此,浓度改变时,扩散系数可能减小,也可能增加。比如,在Au-Ni合金中,Ni的质量分数增加,各扩散系数D、DAu、DNi均明显下降。在不含C的γ-Fe中,950℃时Fe的自扩散系数为0.5×10-12cm2/s。当γ-Fe中C的质量分数达到1.1%时,Fe的自扩散系数增大到9×10-12cm2/s。实际上,浓度引起的扩散系数,其变化不会超过2~6倍。这主要是由于Ea在变化时,D0也在变化所致。
因此,我们在前面求解扩散微分方程时,将D视为与c无关的常数是不符合实际情况的。在那里,我们仅是为了计算方便才做相应简化的。尽管这种简化与实际不符,但在一些要求不高的场合,做此简化而获得的结果还是可以接受的。而且,这种简化也是科学研究、工程应用常采用的一种方法。
3.杂质(第三组元)
在二元合金中加入杂质(第三组元)会影响合金体系的扩散系数。然而,这种影响比较复杂:有的杂质促进扩散、有的阻碍扩散。比如,在碳钢中加入质量分数为4%的Co可使C在γ-Fe中的扩散系数增大一倍;加入质量分数为3%的Mo或1%的W,则可使C在γ-Fe中的扩散系数减少一半。Ni、Mn的加入则对C在γ-Fe中的扩散系数影响不大。Al-Mg合金中,引入质量分数为2.7%的Zn可使Mg在Al中的扩散速率减半。
杂质的引入还会影响扩散方向。1948年,Darken将单相奥氏体Fe-C合金(C、Si的质量分数分别为0.45%、0.05%)与Fe-C-Si合金(C、Si的质量分数分别为0.49%、3.80%)焊在一起组成扩散偶。初始时,扩散界面两侧C的质量分数非常接近,可以认为C的浓度梯度为零。然后,将扩散偶置于1050℃扩散退火1.109×106s(约13 d)。结果表明,在扩散界面Fe-C-Si合金一侧,C的质量分数下降;而Fe-C合金一侧,C的质量分数增加。这是由于Si的加入使C的化学势上升,故含较多Si的合金中C向含Si很少的合金中做上坡扩散。
杂质影响D主要是通过以下一些途径达到的:改变原有组元的活度,进而影响化学势;产生点阵畸变、改变空位浓度(尤其是不等价离子的引入),从而改变扩散活化能和原子(离子)空位的迁移率;细化晶粒增加了短路扩散的通道等,但若引入的杂质与基体材料形成化合物,则会使扩散活化能增加。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







