【摘要】:CsCl型结构的示意图如图2.27所示。其Strukturbericht符号为B2,Pearson符号为cP2。Cl原子位于8个角顶,Cs原子占据体心位。Cs、Cl原子的配位数都是8。每个晶胞有2个原子,1个CsCl“分子”,即Z=1。图3.15βCuZn与β'CuZn结构示意图β′-CuZn与β-CuZn有一定联系。而β′-CuZn中的原子排布为有序态,如图3.15所示,因而晶体结构保持了CuZn的化学式。460℃以上转化为β-CuZn,其强度、延展性、韧性都较好,故含有β-CuZn的黄铜适宜压力加工。
CsCl型结构(Caesium chloride)的示意图如图2.27所示。它属于简单立方点阵、等轴晶系,空间群为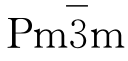 。其Strukturbericht符号为B2,Pearson符号为cP2。Cl原子位于8个角顶,Cs原子占据体心位。Cs、Cl原子的配位数都是8。每个晶胞有2个原子,1个CsCl“分子”,即Z=1。晶胞中原子的位置:Cl(0,0,0)、Cs(0.5,0.5,0.5)。具有这种结构的材料比较少,主要是β′-CuZn、β′-AgZn、β′-AuZn、FeAl等金属间化合物。
。其Strukturbericht符号为B2,Pearson符号为cP2。Cl原子位于8个角顶,Cs原子占据体心位。Cs、Cl原子的配位数都是8。每个晶胞有2个原子,1个CsCl“分子”,即Z=1。晶胞中原子的位置:Cl(0,0,0)、Cs(0.5,0.5,0.5)。具有这种结构的材料比较少,主要是β′-CuZn、β′-AgZn、β′-AuZn、FeAl等金属间化合物。
 (https://www.daowen.com)
(https://www.daowen.com)
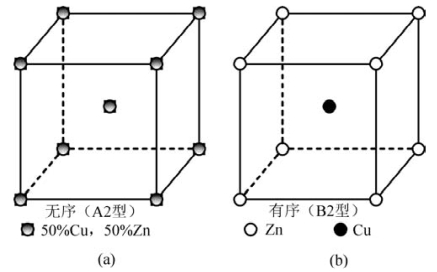
图3.15 (a)βCuZn与(b)β'CuZn结构示意图(50%表示原子占据此位的概率)(引自蔡珣,2010)
β′-CuZn与β-CuZn有一定联系(图3.15)。图3.15(a)为β-CuZn,它属于体心立方点阵。该结构中,每个原子位置被一个Cu或Zn原子占据的概率为50%,故原子排布成无序态。而β′-CuZn中的原子排布为有序态,如图3.15(b)所示,因而晶体结构保持了CuZn的化学式(在面心立方点阵的晶体结构中也有类似现象,如Cu3Au为有序、Cu1-xAux为无序)。室温下β′-CuZn较脆、强度高、延展性低。460℃以上转化为β-CuZn,其强度、延展性、韧性都较好,故含有β-CuZn的黄铜适宜压力加工。而一定数量的β′-CuZn会使普通黄铜塑性下降、强度提高。当Zn的质量分数大于45%时,β′相使黄铜强度、塑性急剧下降,故无实用价值。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
相关文章






