一、判断题
1.√ 2.√ 3.√ 4.× 5.√ 6.× 7.×
8.× 9.× 10.√ 11.× 12.× 13.√ 14.√
15.√ 16.√ 17.× 18.√ 19.× 20.√ 21.×
22.√ 23.× 24.√ 25.√ 26.√ 27.× 28.√
29.√ 30.× 31.√ 32.√ 33.√ 34.√ 35.√
36.√ 37.√ 38.√ 39.√ 40.× 41.√ 42.√
43.√ 44.√ 45.√ 46.√ 47.√ 48.× 49.√
50.√ 51.√ 52.× 53.√ 54.√ 55.√ 56.√
57.√ 58.√ 59.√ 60.× 61.× 62.√ 63.×
64.√ 65.× 66.√ 67.√ 68.× 69.√ 70.√
71.√ 72.√ 73.√ 74.× 75.√ 76.× 77.√
78.× 79.√ 80.× 81.√ 82.√ 83.√ 84.√
85.√ 86.√ 87.√ 88.√ 89.√ 90.√ 91.√
92.√ 93.× 94.× 95.× 96.√ 97.√ 98.√
99.√ 100.√ 101.× 102.√ 103.× 104.× 105.√
106.√ 107.√ 108.√ 109.√ 110.√ 111.× 112.√
11.3√ 114.√ 115.√ 116.× 117.√ 118.× 119.√
120.√ 121.× 122.√ 123.√ 124.√ 125.× 126.√
127.√ 128.√ 129.√ 130.√ 131.√ 132.√ 133.√
134.√ 135.× 136.√ 137.× 138.× 139.× 140.√
141.√ 142.× 143.√ 144.× 145.× 146.√ 147.√
148.× 149.√ 150.× 151.√ 152.× 153.√ 154.×
155.√ 156.√ 157.√ 158.√ 159.× 160.√ 161.√
162.× 163.× 164.√ 165.× 166.√ 167.√ 168.×
169.√ 170.√ 171.× 172.√ 173.√ 174.× 175.√
176.√ 177.√ 178.√ 179.√ 180.√ 181.× 182.√
183.√ 184.√ 185.× 186.√ 187.√ 188.× 189.√
190.× 191.× 192.√ 193.√ 194.× 195.√ 196.√
197.√ 198.√ 199.× 200.× 201.× 202.√ 203.√
204.√ 205.× 206.√ 207.× 208.√ 209.× 210.√
211.√ 212.√ 213.× 214.× 215.√ 216.√ 217.√
218.× 219.× 220.× 221.√ 222.√ 223.× 224.√
225.√ 226.√ 227.× 228.√ 229.√ 230.√ 231.√
232.√ 233.√ 234.√ 235.√ 236.√ 237.√ 238.√
239.√ 240.√ 241.√ 242.√ 243.√ 244.× 245.×
246.√ 247.√ 248.× 249.√ 250.√ 251.× 252.√
253.√ 254.√ 255.√ 256.× 257.√ 258.× 259.×
260.√ 261.× 262.× 263.× 264.× 265.× 266.×
267.√ 268.√ 269.√ 270.√ 271.√ 272.√ 273.×
274.√ 275.√ 276.√ 277.√ 278.√ 279.√ 280.√
281.√ 282.× 283.√ 284.× 285.× 286.√ 287.√
288.√ 289.√ 290.√ 291.× 292.√ 293.× 294.×
295.× 296.√ 297.√ 298.√ 299.× 300.× 301.×
302.× 303.× 304.√ 305.× 306.√ 307.× 308.√
309.× 310.√ 311.√ 312.× 313.× 314.√ 315.×
316.× 317.× 318.√ 319.× 320.√ 321.× 322.√
323.× 324.√ 325.× 326.√ 327.√ 328.√ 329.×
330.√ 331.√ 332.× 333.× 334.√ 335.× 336.√
337.× 338.√ 339.√ 340.× 341.√ 342.√ 343.√
344.√ 345.√ 346.× 347.√ 348.√ 349.√ 350.√
351.× 352.√ 353.√ 354.× 355.√ 356.× 357.×
358.√ 359.√ 360.× 361.× 362.× 363.× 364.×
365.√ 366.× 367.√ 368.√ 369.× 370.× 371.√
372.× 373.√ 374.√ 375.× 376.√ 377.√ 378.×
379.√ 380.√ 381.× 382.√ 383.√ 384.× 385.×
386.√ 387.× 388.√ 389.√ 390.√ 391.√ 392.×
393.√ 394.× 395.√ 396.√ 397.√ 398.√ 399.√
400.√
二、选择题
1.B 2.D 3.A 4.A 5.B 6.A 7.C
8.C 9.B 10.A 11.C 12.C 13.C 14.D
15.B 16.D 17.C 18.C 19.D 20.D 21.D
22.A 23.A 24.B 25.A 26.C 27.B 28.A
29.D 30.D 31.A 32.C 33.C 34.D 35.A
36.B 37.C 38.D 39.B 40.D 41.A 42.D
43.A 44.D 45.C 46.B 47.C 48.A 49.A
50.B 51.C 52.D 53.A 54.B 55.A 56.C
57.C 58.D 59.A 60.D 61.C 62.D 63.C
64.B 65.A 66.B 67.D 68.D 69.B 70.A
71.A 72.D 73.B 74.C 75.E 76.B 77.A
78.E 79.C 80.C 81.C 82.B 83.A 84.C
85.B 86.C 87.B 88.A 89.A 90.A 91.A
92.A 93.A 94.C 95.D 96.B 97.A 98.D
99.A 100.A 101.C 102.D 103.A 104.D 105.C
106.C 107.B 108.A 109.B 110.C 111.C 112.C
113.B 114.A 115.C 116.A 117.B 118.D 119.D
120.D 121.D 122.D 123.C 124.D 125.D 126.C
127.C 128.C 129.A 130.A 131.C 132.C 133.B
134.C 135.D 136.C 137.D 138.B 139.B 140.C
141.C 142.B 143.C 144.B 145.A 146.B 147.A
148.D 149.B 150.C 151.A 152.B 153.B 154.A
155.A 156.C 157.D 158.B 159.D 160.A 161.A
162.A 163.C 164.C 165.B 166.C 167.D 168.A
169.C 170.D 171.C 172.B 173.D 174.C 175.C
176.D 177.C 178.C 179.D 180.B 181.D 182.C
183.D 184.C 185.A 186.A 187.B 188.D 189.B
190.B 191.D 192.D 193.B 194.D 195.D 196.B
197.B 198.A 199.A 200.B 201.D 202.A 203.A
204.D 205.B 206.D 207.B 208.C 209.C 210.B
211.A 212.A 213.A 214.B 215.A 216.A 217.C
218.C 219.C 220.D 221.A 222.C 223.C 224.A
225.C 226.B 227.A 228.C 229.B 230.A 231.D
232.B 233.D 234.C 235.C 236.D 237.D 238.C
239.A 240.C 241.D 242.C 243.A 244.B 245.C
246.C 247.A 248.B 249.B 250.D 251.A 252.D
253.D 254.A 255.B 256.C 257.B 258.A 259.D
260.C 261.C 262.D 263.C 264.D 265.C 266.D
267.B 268.A 269.D 270.D 271.C 272.A 273.B
274.A 275.B 276.A 277.B 278.C 279.C 280.A
281.A 282.D 283.C 284.D 285.A 286.B 287.A
288.B 289.C 290.C 291.A 292.D 293.D 294.C
295.D 296.C 297.D 298.C 299.A 300.B 301.D
302.C 303.B 304.D 305.B 306.C 307.B 308.C
309.D 310.A 311.C 312.B 313.C 314.C 315.C
316.D 317.A 318.D 319.B 320.C 321.B 322.C
323.D 324.B 325.C 326.C 327.A 328.A 329.C
330.A 331.D 332.A 333.C 334.A 335.C 336.A
337.B 338.D 339.C 340.C 341.A 342.B 343.C
344.D 345.C 346.A 347.D 348.A 349.A 350.C
351.B 352.A 353.A 354.A 355.D 356.C 357.B
358.D 359.C 360.C 361.C 362.B 363.A 364.B
365.C 366.A 367.C 368.C 369.C 370.C 371.C
372.B 373.C 374.B 375.A 376.A 377.B 378.C
379.D 380.C 381.D 382.D 383.A 384.C 385.B
386.B 387.C 388.A 389.B 390.C 391.D 392.D
393.C 394.D 395.C 396.D 397.B 398.B 399.C
400.B 401.D 402.D 403.B 404.B 405.D 406.A
407.A 408.D 409.B 410.B 411.B
三、简答题
1.答:不是同一概念。酸度是指溶液中H+的浓度,准确地说是H+的活度。酸的浓度是未离解和已离解酸的浓度。
2.答:指示剂的变色范围全部或大部分落在滴定突跃范围内。
3.答:在生产和储藏过程中,因吸收空气中的CO2而产生部分Na2CO3。可采用双指示剂法测定烧碱中NaOH和Na2CO3的含量。
4.答:用其控制溶液的酸度,使溶液酸度基本保持不变。
6.答:有三种类型。①自身指示剂,如高锰酸钾;②氧化还原指示剂,如次甲基蓝;③专属指示剂,如可溶性淀粉。
7.答:不能。因为温度超过90℃时H2C2O4容易分解,导致标定结果偏高。
8.答:因为在碱性溶液中I2与S2O32-将发生反应,即
S2O32-+4I2+10OH-=2SO42-+8I-+5H2O
同时,I2在碱性溶液中发生歧化反应,即
3I.D+6OH-=IO3-+5I-+3H2O
在强酸性溶液中,Na2S2O3溶液会发生分解反应,即
S2O32-+2H+=SO2+S+H2O
同时,I-在酸性溶液中易被空气中的O2氧化,即
4I-+4H++O2=2I2+2H2O
9.答:沉淀滴定法是以沉淀反应为基础的滴定分析方法。用于沉淀滴定的反应必须符合以下条件:①沉淀的溶解度必须很小,要求反应能定量进行;②反应快速,不易形成过饱和溶液;③有确定重点的简单方法。
10.答:吸附指示剂的阴离子被吸附在胶体微粒表面之后,分子结构发生变形,引起吸附指示剂颜色变化,从而指示终点的到达。
11.答:有影响。如果K2CrO4指示剂的浓度过高或过低,沉淀Ag2CrO4析出就会提前或滞后。
12.答:有机沉淀剂具有较大的相对分子质量和较高的选择性,形成的沉淀具有较小的溶解度,并具有鲜艳的颜色和便于洗涤的结构,也容易转化为称量形式。使用有机沉淀剂,一方面能够降低沉淀的溶解度,同时还可以减少共沉淀现象及形成混晶的概率。
13.答:①沉淀剂应为易挥发或易分解的物质,在灼烧时可以除去;②沉淀剂应具有较高的选择性。
14.答:烘干可除去沉淀中的水分和挥发性物质,同时使沉淀组成达到恒定。灼烧可除去沉淀中的水分、挥发性物质和滤纸等,还可以使初始生成的沉淀在高温下转化为组成恒定的称量形式。
15.答:欲测组分的回收率是指欲测组分经分离或富集后所得的含量与它在试样中的原始含量的比值(数值以%表示)。对常量组分的测定,要求回收率大于99.9%,而对于微量组分的测定,回收率可为95%,甚至更低。
16.答:萃取效率是指物质在有机相中的总物质的量占两相中的总物质的量的百分率(数值以%表示)。它表示萃取的完全程度。单次萃取,萃取效率不高;多次萃取,萃取效率较高。
17.答:①溶剂纯度要高,以减少因溶剂而引入的杂质;②沸点宜低,以便于分离后浓缩;③被萃取物质在萃取剂中溶解度要大,而杂质在其中的溶解度要小;④密度大小适宜,易于两相分层;⑤性质稳定、毒性小。
18.答:分别调节标准液和待测液的离子强度和酸度,以掩蔽干扰离子。
19.答:由于在高浓度(通常大于0.01mol/L)时,吸收质点之间的平均距离缩小到一定程度,邻近质点彼此的电荷分布都会相互受到影响,此影响能改变它们对特定辐射的吸收能力,相互影响程度取决于浓度。因此,此现象可导致吸光度与浓度线性关系发生偏差。
20.答:①产品质量检验机构计量认证申请书;②产品质量检验机构仪器设备一览表;③产品质量检验机构质量管理手册。
21.答:Na2CO3与HCl发生反应生成的CO2溶于水中,使溶液呈酸性,从而使终点提前到达。
22.答:在气体的负压不太高时可用。
23.答:液-液萃取分离法简称萃取分离法。它是利用物质在两种不互溶(或仅微溶)的溶剂中溶解度的差异,达到分离纯化目的的一种分离试样的方法。该方法所需仪器设备简单,操作比较方便,分离效果好,既能用于大量元素的分离,又适合于微量元素的分离与富集。
24.答:闪点是有机化合物特别是易燃性物质的一个重要物理常数,不同类型的物质有不同的闪点值。测定闪点的方法有开口杯法和闭口杯法。
25.答:粪大肠菌群是一群需氧及兼性厌氧,在44.5℃培养,24~48h能发酵乳糖产酸并产气的革兰氏阴性无芽孢杆菌。
26.答:进行多次平行测定。
27.答:不能。因为如果使用时间过长,灯管的亮度会下降,寿命也会降低。
28.答:在保证用空白溶液能较好地调到100%透光度的情况下,应尽可能采用灵敏度较低档,这样仪器稳定性高。
29.答:应使用防护用品,瓶口不要对着人,宜在通风柜中进行。
30.答:化学灼伤时,应迅速解开衣服,清除皮肤上的化学药品,并用干净的水冲洗。
31.答:气相色谱的主要特点是选择性好,分离效率高,灵敏度高,分析速度快。
32.答:色谱定性的依据是保留数值,包括保留时间、相对保留时间、保留指数等。色谱定量的依据是峰高和峰面积。
33.答:主要的定性方法有:①纯物质对照法;②利用保留值经验规律定性;③利用其他方法定性,比如利用化学方法配合进行未知组分定性,结合其他仪器进行定性(如色谱-质谱联用、色谱-核磁共振联用等)。
34.答:无论采用峰高还是峰面积进行定量分析,其物质浓度(或含量)mi和相应的峰高或者峰面积Ai之间必须呈直线函数关系,符合数学式mi=fiAi。这是色谱定量分析的重要根据。色谱分析的准确度主要取决于进样量的重复性和操作条件的稳定程度。
35.答:色谱柱内填充的不移动的、起分离作用的物质叫固定相。根据固定性的不同,气相色谱可分为气固色谱法和气液色谱法两类。若色谱柱内填充的是一种固体吸附剂,如分子筛、活性炭、氧化铝等,则此时进行的分析叫作气固色谱法。若色谱柱内填充的是一种惰性固体[无吸附性、催化性,但有较大的比表面积(约1m2/g)和一定的机械强度],其表面涂有一层高沸点的有机化合物液膜(通常叫作固定液),则此时进行的分析叫作气液色谱法。
36.答:对固定液的要求有:①对样品中各组分都有溶解能力,而且具有选择性;②沸点高、蒸汽压力小,不易流失;③热稳定性好,在工作温度下不易发生分解、聚合等反应;④黏度和凝固点要低;⑤化学稳定性好,不与样品、载气等发生化学反应;⑥能牢固地附着在载体表面,形成均匀结构的薄层。
37.答:气液色谱常用的固定液有以下四类:①非极性十八烷(或角鲨烷、阿匹松等);②中等极性癸二酸辛酯(或邻苯二甲酸二壬酯、磷酸三苯酯、丁二酸二乙醇酯等);③极性苯乙腈(或二甲基甲酰胺等);④氢键型,如甘油(或季戊四醇等)。
38.答:色谱柱在使用前要进行老化处理,其目的是彻底除去残余的溶剂和挥发性杂质,促进固定液均匀、牢固地分布在载体表面。老化时的柱温应略高于操作时使用的柱温,但不能超过固定液的最高使用温度。应使用较低的载气流速,以使载气充分冲洗色谱柱。老化好的标志是接通记录仪后基线走得平直。
39.答:热导池之所以能够作为检测器,根据的是不同的物质具有不同的导热系数。各种组分和载气通过热导池时,气体组成及浓度如果发生变化,就会从热敏元件上带走不同的热量,使热敏元件的阻值发生变化,从而改变电桥的输出信号,该信号的大小和载气中组分的浓度成正比。热导池检测器的优点为:①结构简单、操作方便;②灵敏度适宜,稳定性好;③线性范围宽;④应用范围广,绝大部分样品都能测定;⑤不破坏样品,可与其他仪器联用。
40.答:有机物在氢火焰的高温下,被电离成带电的离子,这些离子在电场作用下进行定向流动,被收集成微弱电流,此电流的大小与进入检测器的有机物的质量成正比,因此可根据电流大小进行定量分析。氢火焰离子化检测器的特点是:①灵敏度高,比热导检测器高10~100倍;②死体积小,响应时间快;③线性范围宽;④结构简单,操作方便。
41.答:应具备三个条件:①样品中所有组分都必须出峰,否则结果不准确;②要已知各组分的校正因子;③各个峰之间要能较好地分离。
42.答:气固色谱法是用固体(一般指吸附剂)作为固定相的气相色谱法。气液色谱法是指将固定液涂在载体上作为固定相的气相色谱法。
43.答:内有固定相用以分离混合组分的柱管是色谱柱。具有吸附活性并用于色谱分离的固体物质是吸附剂。色谱柱内不移动的,起分离作用的物质是固定相。固定液是涂在载体表面上起分离作用的物质,在操作温度下不易挥发的液体。固定液是固定相的组成部分。在色谱柱中用以携带试样和洗脱组分的气体是流动相。用作流动相的气体称为载气。
44.答:柱效能是色谱柱在色谱分离过程中主要由动力学因素(操作参数)所决定的分离效能,通常用理论板数、理论板高或有效板表示。分离度(R)是两个相邻色谱峰的分离程度,以两个组分保留值之差与其平均峰宽值之比表示,即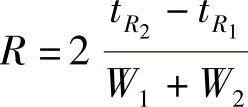 。灵敏度(S)是检测器的物质比变化ΔQ时相应信号的变化率,即
。灵敏度(S)是检测器的物质比变化ΔQ时相应信号的变化率,即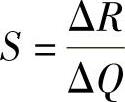 。检测限(D)是随单位体积的载气或在单位时间内进入检测器的组分所产生的信号等于基线噪声2倍时的量,即
。检测限(D)是随单位体积的载气或在单位时间内进入检测器的组分所产生的信号等于基线噪声2倍时的量,即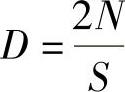 。
。
45.答:分配系数(K)是在平衡状态时,组分在固定液与流动相中的浓度之比。
46.答:试样中全部组分都显示出色谱峰时,测量的全部峰值经相应的校正因子校正并归一后,计算每个组分的质量分数的方法称为归一(化)法。在已知量的试样中加入能与所有组分完全分离的已知量的内标物质,用相应的校正因子校准待测组分的峰值,并与内标物质的峰值进行比较,求出待测组分的质量分数的方法是内标法。在相同的操作条件下,分别将等量的试样与含待测组分的标准试样进行色谱分析,比较试样与标准试样中待测组分的峰值,求出待测组分的含量的方法称为外标法。
47.答:分离系统的核心是色谱柱,它的作用是将多组分样品分离为单个组分。色谱柱分为两类:填充柱和毛细管柱(开管柱)。
48.答:载体又称为担体,作用是提供一个具有较大表面积的惰性表面,使固定液能在它的表面上形成一层均匀的液膜。由于载体结构与表面性质会直接影响柱的分离效果,因此在气液色谱中,要求载体表面应是化学惰性的,即无吸附性、无催化性且热稳定性要好。为了能涂布更多的固定液又不增加液膜厚度,要求载体比表面积要大,孔径分布均匀,另外还要求载体机械强度好,不易破碎。
49.答:气相色谱常用载体主要有硅藻土型及非硅藻土型两大类。选择载体的原则是:①固定液用量大于质量分数5%时,可选用硅藻土白色载体或红色载体;若固定液用量小于质量分数5%,可选用表面处理过的载体。②腐蚀性样品可选氟载体,而高沸点组分可选用玻璃微球载体。③载体粒度一般选用60~80目(粒径为0.2~0.3mm)或80~100目(粒径为0.15~0.2mm),高效柱可选用100~120目(粒径为0.125~0.15mm)。
50.答:气液色谱柱的制备有以下四个步骤:①色谱柱柱管的选择与清洗;②固定液的涂渍;③色谱柱的填充;④色谱柱的老化。
51.答:原子吸收光谱法的基本原理是:基于元素所产生的原子蒸气对同种元素所发射的特征谱线的吸收作用进行定量分析,即由一种特制的光源(元素空心阴极灯)发射出该元素的特征谱线,谱线通过该元素的原子蒸气时被吸收,产生吸收信号,所吸收的吸光度的大小与试样中该元素的含量成正比,即A=Kc。
52.答:相同之处:①它们均是依据样品对入射光的吸收来进行测量的,即经处理后的样品,吸收来自光源发射的某一特征谱线,经过分离之后,将剩余的特征谱线进行光电转换,经过记录器记录吸收强度的大小来测定物质含量;②两种方法都遵守朗伯-比尔定律;③就其设备而言,均由四大部分组成,即光源、单色器、吸收池(或原子化器)、检测器。
不同之处:①单色器与吸收器的位置不同。在原子吸收光谱仪中,原子化器的使用相当于吸收池,它的位置在单色器之前,而分光光度计中吸收池在单色器之后,这是由它们的吸收机理不同决定的。②从吸收机理上看,分光光度计是利用有色化合物对光的吸收进行测定的,属于宽带分子吸收光谱,它可以使用连续光谱(钨灯、氢灯等),比色皿中的有色液也较稳定。原子吸收光谱是窄带原子吸收光谱,因而它所使用的光源必须是锐线光源(空心阴极灯),在测量时必须将样品原子化,转化为基态原子,这在比色皿中是办不到的。
53.答:①灵敏度高。火焰原子吸收光谱对多数元素的测定灵敏度在10-6以上,少数元素采取特殊手段可达10-9级。无火焰原子吸收比火焰原子吸收还要灵敏几十倍到几百倍。②选择性好。共存元素对待测元素干扰少,一般不需要分离共存元素。③测定元素范围广,可以测定元素周期表中的70多个元素。④操作简便,分析速度快,分析方法容易建立,重现性好。⑤准确度高。可进行高精度的微量分析,准确度可达0.1%~1.0%。
54.答:①光源:主要部件是空心阴极灯,其作用是发射足够强度的特征谱线供测量用。②原子化器:分为有火焰和无火焰两种,其作用是将试样中的被测元素转变成基态原子(即自由原子蒸气)。③光学系统:主要部件是单色器,由光栅和反光镜等组成,其作用是把所需的特征谱线和其他谱线分开。④检测系统:主要部件为光电倍增管,其作用是把分光后的特征谱线转换为电信号。目前,有些仪器配有记录仪或电脑,可将电信号放大或记录下来,或直接显示为浓度值。
55.答:原子吸收光谱分析常用的分析方法有标准曲线法、标准加入法和浓度直接法。进行一项测定时通常的步骤是:①根据待测元素的灵敏度配制一份相当于0.1~0.5吸光度读数的标准溶液;②选择仪器的试验条件;③确定分析方法;④确定样品溶液的配制方法及是否需要采取分离、富集、前处理等;⑤确定是否需要消除干扰及消除的方法。
56.答:原子吸收光谱分析的标准曲线不能长时间使用。分光光度法测定时,在仪器、药品、操作手续不变的情况下,标准曲线一般改变不大,而原子吸收操作时,每次开机与前一次开机的原子化条件不可能完全一致,因此需每次开机均做标准曲线或再测标准溶液。
57.答:进行原子吸收光谱分析可能产生化学干扰、电离干扰、光谱干扰(背景吸收、邻近线干扰等)。消除方法如下:
1)化学干扰:利用温度效应消除;利用火焰气氛消除;加入释放剂,利用置换反应消除;加入保护剂;加入助熔剂;改变溶液的性质及雾化器的性能;预先分离干扰物质。
2)电离干扰:加入电离抑制剂(或称消电离剂)。
3)光谱干扰:其中主要是背景吸收(干扰),它是光谱干扰的一种特殊形式,包括分子吸收、光的散射等。火焰原子吸收光谱干扰的消除:利用零点调整消除;利用氘灯连续光谱扣除火焰的分析吸收干扰。光散射的消除:利用背景校正可以测量光散射的大小,求得被测元素吸收的真实信号。另外,还有基体效应(干扰),即溶液物理性质(黏度、张力、温度等)的变化使喷雾效率改变,产生吸光度的改变,样品和标准溶液中主要成分匹配可减少基体效应干扰。
58.答:测定结果灵敏度低的主要原因有:①元素灯发射背景太大;②元素灯工作电流太大,原子的自蚀效应导致谱线变宽,灵敏度降低;③火焰温度选择不适当,燃气与助燃气之比选择不当;④火焰高度选择不当;⑤雾化器调整不好,或因长期不用,喷嘴被盐或脏东西堵塞,使样品提取量减少,这是仪器灵敏度降低的主要原因;⑥撞击球与喷嘴的相对位置没有调好;⑦燃烧器与外光路不平行;⑧光谱通带选择不合适;⑨波长选择不合适;⑩燃气不纯;⑪ᣘᣢ空白溶液被污染,造成火焰状态不好,使空白吸收干扰增大,灵敏度降低;⑪ᣘ⑫雾化筒与燃烧缝严重锈蚀,雾化样品变成水珠;⑪ᣘ⑬雾化筒内有油膜或因长期不用而生锈,筒内积水,废液流动不通畅;⑪ᣘ⑭样品与标准溶液存放时间过长而变质,容器的吸附作用或化学反应的结果造成灵敏度降低;⑪ᣘ⑮火焰状态不好,摆动严重或呈锯齿状,使测定结果偏低;⑪ᣘ⑯燃气漏气或阀门开关不灵,造成工作条件改变;⑪ᣘ⑰气源压力不足。针对以上原因,采取相应措施,即可解决。
59.答:在原子吸收光谱分析中产生过大噪声的可能原因为:①火焰的高度吸收,当测定远紫外区的元素(如As或Se)时,分析过程中产生噪声可能较大;②空心阴极灯能量不足,伴随从火焰或溶液组分来的强发射,引起光电倍增管的高度噪声;③吸喷有机样品试剂(如油或甲基异丁酮)沾污了燃烧器;④灯电流、狭缝、乙炔气和助燃气流量的设置不恰当;⑤废液管状态不当,排液异常;⑥燃烧器狭缝被污染;⑦雾化器调节不当,雾滴过大;⑧乙炔钢瓶或空气压缩机输出压力不足;⑨检查空气过滤器,尤其发现在火焰中存在过量的钠发射时,不纯的乙炔也会有此发射。
针对以上可能产生故障的原因,采取以下方法即可排除:①采用背景校正有时可有所改善;②在允许的最大电流值内,增大灯的工作电流,换用能量大的新灯,试用其他吸收线进行分析,用化学方法去除溶液中能通过火焰产生强发射的干扰组分;③清洗燃烧器;④将灯电流、狭缝、乙炔气和助燃气的流量重新设置为一合适值;⑤更换排液管,重新设置水封;⑥清洗燃烧器的缝隙;⑦重新调节雾化器;⑧增加乙炔及空气的输出压力;⑨采取措施,纯化空气或乙炔气。
60.答:在原子吸收光谱分析中,分析结果偏高的可能原因有:①溶液中的固体未完全溶解,因而造成假吸收;②由于背景吸收造成假吸收;③未进行空白校正试验;④标准溶液变质;⑤由于谱线覆盖造成假吸收。
针对上述可能原因,采取下述方法即可解决:①调高火焰温度,使固体颗粒蒸发离解;②在共振线附近用同样条件再测定一次,把两次测的结果相减;③做空白校正试验;④由于标准溶液变质,所以需重新配制标准溶液;⑤降低试样浓度,减少假吸收。
61.答:在原子吸收光谱分析中,分析结果偏低的可能原因有:①试样挥发不完全,细雾颗粒大,在火焰中未完全离解;②标准溶液变质;③被测试样浓度太高,仪器工作在非线性部分;④试样被污染或存在其他物理化学干扰。
针对上述可能原因,采用下述方法解决:①调整撞击球和喷嘴相对位置,提高喷雾质量;②重新配制标准溶液;③减小试样浓度,使仪器工作在线性范围内;④消除干扰因素,更换试样。
62.答:对于火焰条件的选择,一般应按下述步骤进行:①按测定元素的性质选择火焰种类(通常在空气-乙炔火焰或氧化亚氮-乙炔火焰之间进行选择);②按照火焰种类选择燃烧器;③按照火焰种类选择喷雾器(空气-乙炔火焰及氧化亚氮-乙炔火焰可合用一个喷雾器,在相同压强下,氧化亚氮流量约为空气流量的80%,但具体对某一台仪器是否适用还要看仪器说明);④助燃气压强一般在0.15~0.2MPa/cm2之间调定[调定助燃气流量时,对某一特定雾化器,其吸液量及雾化效率等因素也就较固定(还与溶液性质等有关),在测定过程中,一般不再变动助燃气流量];⑤选定燃气流量,调定火焰的状态[选择时可用标准溶液吸喷,并改变流量(改变燃气流量时要重新调零),根据吸光度-流量变化情况,选用具有最大吸光度的流量范围中最小的流量,完成以上选择后,再确定燃烧器的高度。试验中,可以通过连续变化燃烧器高度,并吸喷标准溶液,观察吸光度的变化(也应注意零点有没有变化),选取具有最大吸光度的燃烧器高度]。
63.答:背景吸收是来自原子化器(火焰或无火焰)的一种光谱干扰。它是由气态分子对光的吸收以及高浓度盐的固体颗粒对光的散射所引起的。
(1)火焰成分对光的吸收 一般来说,波长越短,火焰成分的吸收越严重。这是火焰中的OH、CH、CO等分子或基团吸收光源辐射的结果。这种干扰对分析结果的影响不大,一般可以通过零点的调节来消除。
(2)金属的卤化物、氧化物、氢氧化物以及部分硫酸盐和磷酸盐分子对光的吸收 在低温火焰中,上述分子对测定结果的影响比较明显,例如碱金属的卤化物在紫外光区的大部分波段均有吸收,但在高温火焰中,由于分子分解而变得不明显。碱土金属的氧化物和氢氧化物分子在它们发射谱线的同一光谱区中呈现明显的吸收。这种吸收在低温火焰或温度较高的空气-乙炔火焰中较为明显,在高温火焰中则吸收减弱。
(3)固体颗粒对光的散射 当进行低含量或痕量分析时,大量盐类进入原子化器,这些盐类的微粒在光路中阻挡光束而发生散射现象,此时将引起假吸收。
由此可见,背景吸收(分子吸收)主要是由于在火焰(或无火焰原子化装置)中形成了分子或较大的质点,因此除了待测元素吸收共振线外,火焰中的这些物质———分子和盐类,也吸收或散射光线,引起部分共振发射线的损失而产生误差。这种影响一般随波长的减弱而增大,同时随基体元素浓度的增大而增大,并与火焰条件有关。无火焰原子化器比火焰原子化器有更严重的分子吸收。
64.答:原子吸收分光光度计在使用过程中,为了防止出现“回火”甚至爆炸的危险,通常混合室应呈相对密闭的状态,可采取以下两条措施:①废液排放管采取水封式,水封既可以将废液顺利地排放出去,又能防止燃料气体通过排放管逸出空间,否则会造成火焰不稳定,使读数指针摆动,甚至回火;②在混合室的后端设置有聚四氟乙烯制成的防爆垫(安全塞),当回火发生时,混合室内的可燃混合气体因燃烧而急剧膨胀,当混合室内压强增大到一定程度时,防爆垫能承受的压力将克服它与混合室之间的弹性配合力而自动脱离,使混合室呈开放状态,从而起到安全防爆作用。
65.答:近年来,许多原子吸收分光光度计都带有氘灯自动背景校正装置,用来自动扣除背景干扰。此方法比邻近非吸收线法方便、可靠。氘灯发射的是连续光谱,而吸收线是锐线,所以基态原子对连续光谱的吸收是很小的(即使是浓溶液,吸收也小于1%)。而当空心阴极灯发射的共振线通过原子蒸气时,基态原子和背景对它都产生吸收。氘灯背景校正法通过一个旋转的扇形反射镜使两束光交替地通过火焰进入检测器。当共振线通过火焰时,测出的吸光度是基态原子和背景吸收的总吸光度;当氘灯光通过火焰时,测出的吸光度只是背景吸收(基态原子的吸收可以忽略不计),两次测定值之差即为待测元素的真实吸光度。
66.答:原子吸收分光光度计按照仪器光路结构的不同,可将仪器分为单道单光束型、单道双光束型、双道单光束型及双道双光束型四种类型。
1)单道单光束型的原子吸收分光光度计是指仪器只有一个光源,一个分光系统,一个检测和显示系统,从光源中发出的光仅以单一光束的形式通过原子化器,分光系统和检测系统每次只能测定一种元素。该类仪器具有结构简单、造价低、灵敏度较高的优点,缺点是受光源强度波动影响较大,基线漂移。
2)单道双光束型原子吸收分光光度计是指从光源中发出的光被切光器分成强度相等的两束光,一束光通过原子化器,另一束光不通过原子化器,只作为参比光束,两束光交替地进入分光系统和检测系统。该类仪器中两束光来自同一光源,光源的任何波动可以由参比光束的作用而得到补偿,从而消除了光源强度波动的影响,提高了仪器的稳定性。
3)双道单光束型的仪器有两个光源,两个分光系统,两个检测、显示系统,而光束只有一路。该类仪器利用两个独立的分光系统和两个独立的检测系统对两路光源进行分光和检测,同时给出两种元素的检测结果,故一次可以测定两种光速,并可以方便地进行背景吸收和扣除。
4)双道双光束型的仪器采用两种不同的光源,具有两个分光系统,两个检测、显示系统,但每一个光源所发出的光均分为两束,一束通过原子化器,另一束则不通过原子化器,只作为参比光束。该类仪器可以同时测定两种元素,能消除光源强度波动的影响及原子化系统的干扰,准确度高,稳定性好,但仪器结构复杂,价格昂贵。
67.答:应用原子吸收光谱法进行定量测定时,常用的定量分析方法主要有四种,分别为标准曲线法、直接比较法、标准加入法和内标法。此外,还有浓度直读法和紧密内插法等。
标准曲线法是常用的分析方法。该方法主要在样品组成简单或共存元素无干扰且样品浓度比较低的情况下使用,可用于大批量同种样品的分析。
直接比较法要求标准曲线是一条通过坐标原点的直线,适用于干扰少、浓度低的试样测定,并要求试样溶液与标准溶液的吸光度非常接近。该方法操作比较简单。
标准加入法可以消除基体效应带来的影响,并在一定程度上消除化学干扰和电离干扰,但不能消除背景吸收干扰。该方法适用于在基体组成未知或基体较复杂,干扰不宜消除的情况下使用。该方法的准确度较高。
内标法在一定程度上可以消除由于仪器工作条件(如气体流量、火焰状态、石墨炉温度等)的波动,试液黏度、表面张力的变化,以及基体效应等因素给测定带来的误差,故准确度高。但该方法比较麻烦,其应用受到测量仪器的限制,若采用双道双光束型的仪器进行测定则十分方便。
浓度直读法是在标准曲线为直线的浓度范围内,应用仪器的标尺扩展或数字浓度直读装置测量,人为地使读数和标准溶液的浓度值一致。该方法省去了绘制标准曲线的手续,加快了分析速度。应用浓度直接方法时,必须用标准曲线反复校正后再进行测定,喷雾时,标准溶液与试样溶液消耗的体积应一致,才能获得较好的重复性,每一试样要重复读数2~3次,取其平均值。
紧密内插法在原子吸收的工作曲线在高浓度区发生弯曲的情况下使用。运用紧密内插法可以使原子吸收法进行高含量组分的分析,其所得结果的准确度和精密度可以与化学法相媲美。
68.答:在火焰原子吸收法中,标准溶液的浓度单位通常是μg/mL;在无火焰原子吸收法中,标准溶液的浓度单位通常是μg/L。标准溶液通常使用各被测元素合适的盐类(基准物)来配制,当没有合适的盐类可供选择时,也可直接溶解相应的高纯(质量分数为99.99%)的金属丝、棒、片于合适的溶剂中,然后稀释成所需浓度范围的标准溶液,但不能使用海绵状金属或金属粉末来配制。金属在溶解之前,要磨光并利用稀酸清洗,以除去表面的氧化层。至于非水标准溶液,可将金属有机物溶于适宜的有机溶剂中配制(或将金属离子转化为萃取的化合物),用合适的溶剂萃取,通过测定水相中的金属离子含量间接加以标定。
当所需标准溶液的浓度低于0.1mg/mL时,应先配成比使用的浓度高1~3个数量级的浓溶液(大于1mg/mL)作为储备液,然后经稀释配成。在配制标准溶液时应注意使用去离子水,尤其在测定常见元素如钙、镁、铁、铜、锌、钠等时更应注意保证去离子水的纯度及所用的玻璃器皿(如容量瓶、刻度移液管等)的洁净和不被沾污。溶解高纯金属通常使用优级纯的硝酸或盐酸,而避免使用磷酸或硫酸。储备液应保存在玻璃或聚乙烯试剂瓶中(金、银等元素的储备液应保存在棕色试剂瓶中,有些含氟的储备液只能用聚乙烯试剂瓶储存),且储备液应保持一定的酸度,以防止金属离子水解,达到能存放较长时间的目的。浓度很小(小于1μg/mL)的标准溶液不稳定,使用时间不应超过1~2天。
69.答:使用标准加入法定量时,应该注意以下几个问题:
1)在用作图外推法时,要求相应的标准曲线应是一条通过坐标原点的直线,且待测试液的浓度应在此线性范围内。这是因为标准加入法也是建立在吸光度与浓度成正比的基础之上的(遵循朗伯-比尔定律)。
2)待测元素的加入浓度应适当,加入浓度过高或过低,将使标准曲线的斜率过大或过小,从而产生较大误差。一般情况下,所加入的第一份标准溶液的浓度与试样溶液的浓度应当接近,以免给测定结果引入较大的误差。
3)为了保证能够得到较为准确的外推结果,至少要采用四个点来绘制外推曲线。
70.答:根据火焰的性质,可将火焰分为三类:中性火焰、贫燃性火焰和富燃性火焰。
中性火焰也叫化学计量火焰。这种火焰的燃烧气与助燃气之比(即助燃比)是按照它们之间化学反应的化学计量关系供给的。其特点是:火焰温度较高,干扰少,稳定性好,适合于多数元素的原子化。富燃性火焰也叫还原性火焰。此种火焰的燃助比大于化学计算量,即燃烧气过量。其特点是:火焰燃烧不充分,温度较中性火焰稍低,具有较强的还原性,适合于易形成、难离解的元素(Cr、Mo等)的原子化。贫燃性火焰也叫氧化性火焰。此种火焰的燃助比小于化学计算量,即助燃气过量。其特点是:火焰燃烧充分,温度比富燃性火焰高,不具有还原性,适合于易电离、易离解元素(如碱金属)的原子化。
四、计算题
1.解 算术平均值为
平均偏差为
相对平均偏差为
标准偏差为
相对标准偏差为
2.解 (1)首先将各数按递增顺序排列 15.48%,15.51%,15.52%,15.52%,15.53%,15.53%,15.54%,15.56%,15.56%,15.68%。
(2)求出最大值与最小值之差
xn-xn-1=15.68%-15.48%=0.20%
(3)求出可疑数据与最邻近数据之差
xn-xn-1=15.68%-15.56%=0.12%
(4)计算Q值
查表可知:n=10时,Q0.90=0.41,Q>Q表,所以最高值15.68%必须弃去。
此时,分析结果的范围为15.48%~15.56%,n=9。
同样,可以检查最低值15.48%:
查表可知,n=9时,Q0.90=0.44,Q<Q表,故最低值15.48%应予以保留。
综上可知:有可疑值,15.68%需弃去。
3.解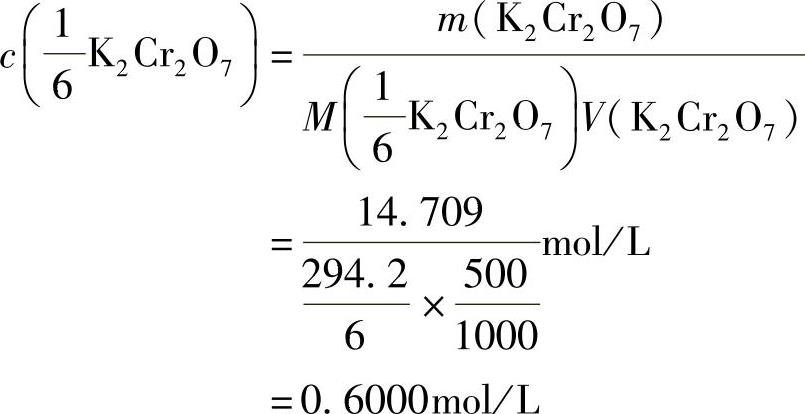
4.解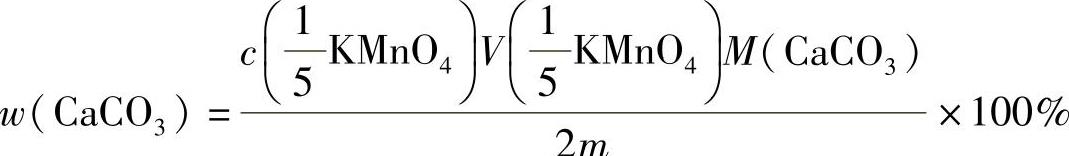
5.解 1)由于c(CH3COONa)/Kb>105,c(CH3COONa)Ka>10Kw,所以可以使用最简式计算,即
2)由于c(NH4Cl)/Ka>105,c(CH3COONa)/Kb>10Kw,所以可以使用最简式计算,即
5)由于cKa2>10Kw,c/Ka1>105,所以可以用最简式计算,即
6.解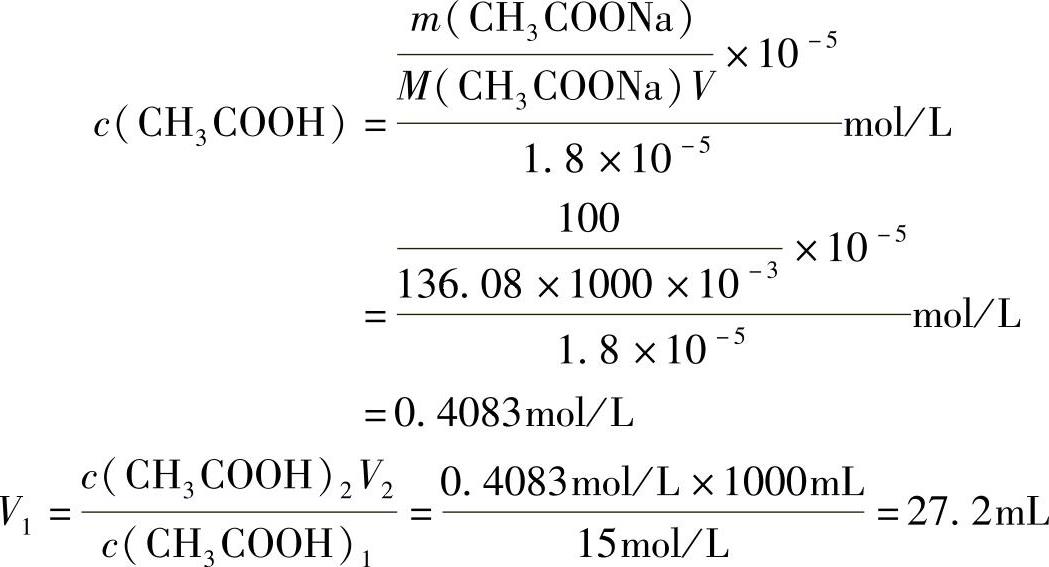
7.解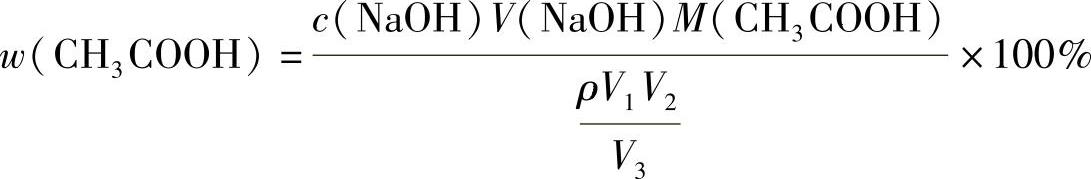
8.解
9.解 此混合碱组成是NaHCO3和Na2CO3。
10.解 lgαY(H)=lgKCuY-8=18.80-8=10.80
pH=2.91
11.解 lgK′CoY=lgKCoY-lgαY(H)=16.31-6.45=9.86
因为lgK′CoY>6,所以在pH=5.0时能用EDTA准确滴定。
12.解
13.解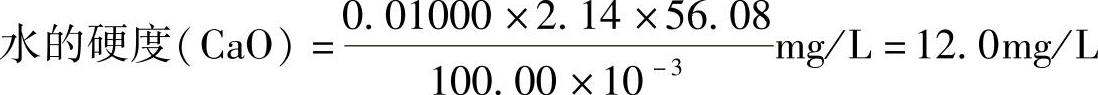
14.解

15.解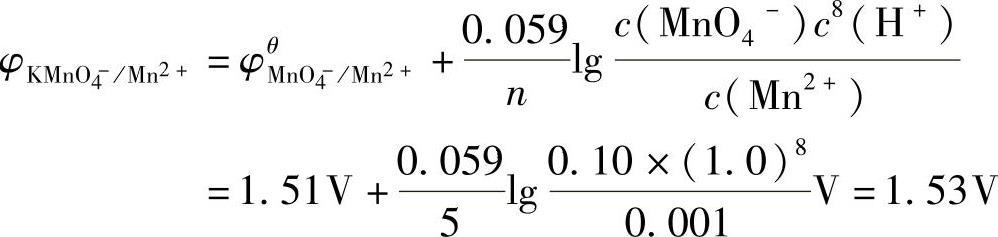
16.解
17.解
18.解
19.解
20.解
21.解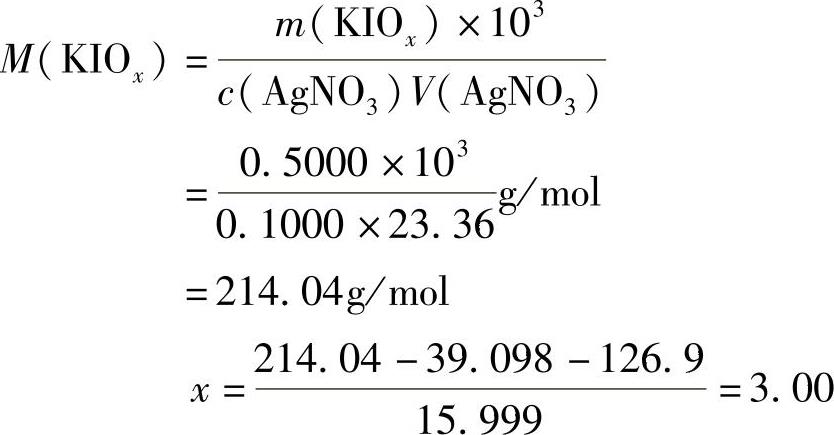 (www.daowen.com)
(www.daowen.com)
所以该盐的化学式为KIO3。
22.解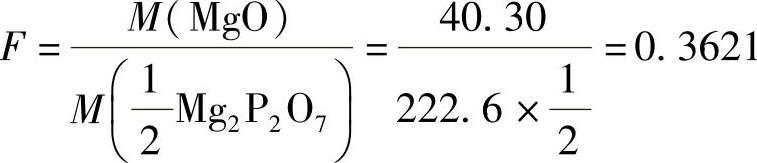
23.解 因为0.00593gI2存在于KI水溶液中,则进入CCl4中的I2质量为0.120g-0.00539g=0.115g。
碘的分配系数
24.解 用40mLCCl4一次萃取:
每次用20mLCCl4连续萃取两次:
25.解 因为在萃取后HA在25.0mL水相中的量为
20.0mL×0.0500mol/L=1.00mmol
则HA在25.0mL乙醚相中的量为
100mL×0.100mol/L-100÷25×1.00mmol=6.00mmol所以HA在有机相中的量与水相中的量之比为
26.解 利用萃取多次后的萃取率计算公式
则有
解得n=4。
27.解 萃取一次后的萃取效率为
利用萃取多次后的萃取率计算公式,学生乙的萃取率为
可见,学生乙比学生甲的萃取率提高了约4%。
28.解 UO2+2的比移值为
La3+的比移值为
29.解 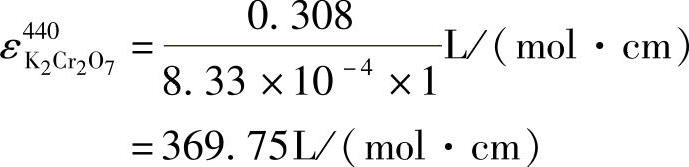
由(1)和(2)可得
c(K2Cr2O7)=9.72×10-4mol/L
c(KMnO4)=2.72×10-4mol/L
30.解 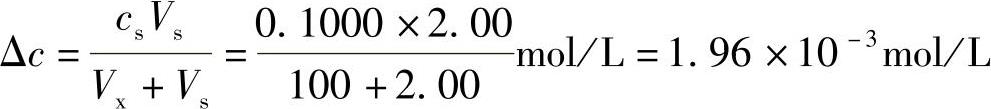
31.解 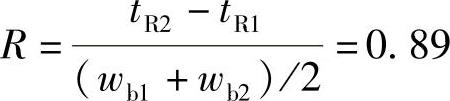
两个峰分不开。
32.解 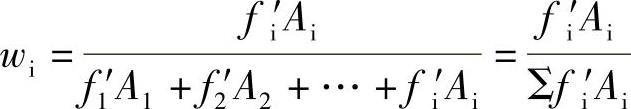
w(甲酸)=4.41%
w(乙酸)=10.06%
w(丙酸)=3.53%
33.解 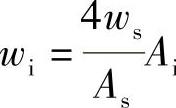
wi=0.5%
34.解 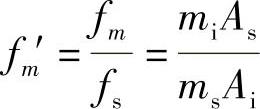
f甲′=1.00
f乙′=1.07
f丙′=1.10
f丁′=0.99
35.解 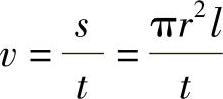
v=81mL/min该柱载气的体积流速是81mL/min。
36.解 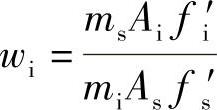
w甲醇=10.11%
37.解 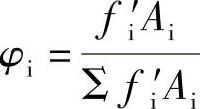
φ甲烷=58.86%
φ乙烷=30.02%
φCO=8.17%
φCO2=2.96%
38.解 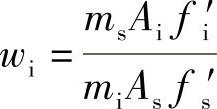
w=0.189%
39.解 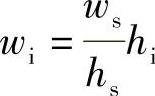
样品的含水量为71.4×10-4%。
40.解 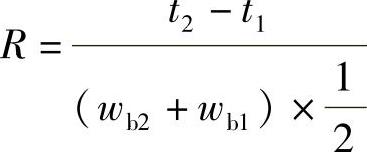
R=1.53,大于1.5,能完全分开。
41.解 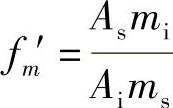
42.解
fm′=0.75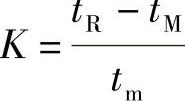
K=3.04
n=7830m
43.解 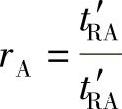
rA=1.00
rB=1.30
44.解 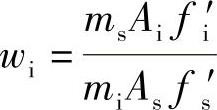
w甲醇=1.99%
45.解 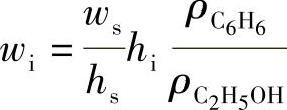
无水乙醇样品中含水量是512×10-4%。
46.解 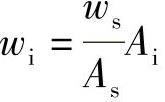
水样中C2H2的含量是69.6mg/L。
47.解 由待测试液测出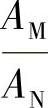 的比值,在内标工作曲线上用内插法查出试液的浓度并计算试样中待测元素的含量。未知样的浓度是17.1g/L。
的比值,在内标工作曲线上用内插法查出试液的浓度并计算试样中待测元素的含量。未知样的浓度是17.1g/L。
48.解 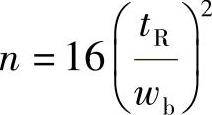
n=2645
H=0.76m
49.解 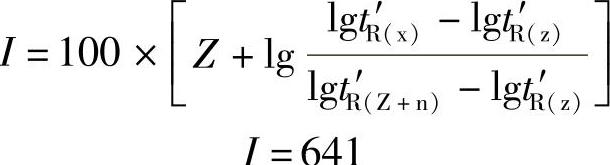
50.解 A苯=1.26cm2,A甲苯=0.95cm2,A邻=2.55cm2,A对=1.04cm2。由归一化法得:f苯=0.780,f甲苯=0.794,f邻=0.840,f对=0.812。
Y=f苯A苯+f甲苯A甲苯+f邻A邻+f对A对
=0.780×1.26+0.794×0.95+0.840×2.55+0.812×1.04
=0.9828+0.7543+2.142+0.8445=4.7236
51.解 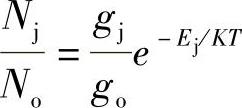
52.解 吸光度在0.15~0.60范围内,相应钙的浓度范围是0.14~0.55μg/mL。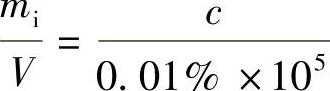 的适宜范围为0.0014~0.0055μg/mL,所以,应称取0.075~0.275g试样制成50mL溶液测量较为合适。
的适宜范围为0.0014~0.0055μg/mL,所以,应称取0.075~0.275g试样制成50mL溶液测量较为合适。
53.解 用加入的铜的浓度及相应的吸光度值进行线性回归计算。当A=0时,所求浓度即为铜的浓度。所以,铜的含量为3.56μg/mL。
54.解 用标准曲线法求得水中钙的含量,或者进行线性回归,根据回归方程计算水中钙的含量。天然水样中钙的含量为0.042mg/mL。
55.解 在原子吸收分析中,吸光度在0.15~0.60的范围内的测量误差比较小,根据特征浓度的表达式S=c×0.0044/A[单位为:μg/(mL·1%)],求出各元素的测量浓度的合适范围,结果均高于各元素的测量浓度合适范围,故均应稀释。经计算,锌需稀释2000倍,铜需稀释200倍,铬需稀释50倍。
五、设计题
1.解
××农用化工有限公司“50g/L氟虫腈悬浮剂”标准检验
(1)前言
本标准代替Q/320381GI39—2007。
本标准由××农用化工有限公司提出并起草。
本标准主要起草人:××。
本标准于×年×月×日首次发布,标准号为Q/320381GI39—2016。
本标准于×年×月×日第一次修订。
(2)引言
产品介绍(略)。
(3)50g/L氟虫腈悬浮剂性质(略)。
(4)适用范围(略)。
(5)规范性引用文件(略)。
(6)项目指标要求(略)。
(7)试验方法(略)。
(8)氟虫腈含量的测定(略)。
(9)pH值的测定(略)。
(10)悬浮率的测定(略)。
(11)筛析(略)。
(12)持久起泡性试验(略)。
(13)倾倒性的测定(略)。
(14)低温稳定性试验(略)。
(15)热储稳定性试验(略)。
(16)产品的检验与验收(略)。
(17)标志、标签、包装、储运(略)。
2.解
化验室发生火灾的紧急预案
1)发现火灾、爆炸事故初起时,发现人员要及时向事故应急领导小组、公司值班领导和地方消防队报警,并讲明发生火灾或爆炸的地点、燃烧(爆炸)物质的种类和数量、火势情况、报警人姓名、联系电话等详细情况。
2)事故应急领导小组接到报警电话后,接报人员要立即通知各小组赶赴火场,拨打“119”报警电话报警并指派专人到路口迎接消防队,同时通知有关部门立即切断火场电源。医疗救治组联系医院派出医生一起赶赴火场并做好准备抢救受伤人员的工作。现场抢救人员接到报警后应立即戴好安全帽及其他防护用具,携带消防器材赶赴现场。
3)抵达火场后,要立即进行灭火工作。扑救火灾在应急小组组长的领导下统一进行,灭火指挥应佩戴明显的标志,各灭火队伍由组长统一调度。在地方消防队到达后,应急组长向地方消防队汇报火灾情况,火场交由地方消防队统一指挥。如果火势较大,则应等消防队到达后再由消防队统一指挥灭火,应急小组先组织火源隔离、易燃易爆物等的搬离等工作,以免由于指挥不当出现不必要的人身伤害。
4)现场抢救组负责抢救被困人员及贵重物资,在人员集中的场所,要有计划、有组织地疏散人员,抢险救灾按“先人员,后物资;先重点,后一般”的原则进行。抢救人员要戴齐防护用具,注意自身安全,防止发生意外事故。
5)安全保卫组负责火灾现场及周围的安全保卫、危险区警戒、交通管制等任务,对现场抢救出的人、财、物进行管理和疏散,预防破坏、哄抢、盗窃等案件的发生,并在扑救过程中及扑救工作结束后对火灾现场加以保护。
6)医疗救护组主要负责火场上各种受伤人员的抢救、医治、转移工作,并协助做好防中毒、防中暑等防护工作。
7)后勤保障组负责火场上器材装备、供水排水、供电照明、运输工具、食品衣物等灭火工作所需的各种物资供应保障工作。
8)在灭火总指挥的统一指挥下,首先要查明火场情况、燃烧物质及周围的情况,特别是有无剧毒、爆炸等危险品,火势大小,烟雾大小,有无毒性气体,火场电源是否切断等,查明后由义务消防队按照“先控制,后消灭,救人第一,分清主次,快速准确”的扑救原则,针对不同的燃烧物质,采用隔离灭火法、窒息灭火法、冷却灭火法、抑制灭火法等方法组织火灾扑救。灭火时要加强个人防护意识,防止意外事故的发生。
9)火场有有毒气体时,要迅速查明火场上毒气的性质、扩散范围、来源和数量,以此为依据来决定能否在佩戴防毒面具和防护用具的情况下,安全地出入火场进行各种扑救工作。
①对泄气口要做“关堵”处理(关闭阀门、堵塞洞),以切断毒气来源。
②对已弥散在火场周围的毒气进行通风驱散或用雾状水流令可溶于水的毒气溶解,降低空气中的毒气含量。
③针对毒气对人身的特殊毒害作用,调集医疗队等有关队伍协同作战,做预防和救护工作。
④根据有毒物质的化学性质和物理性质,选择合适的灭火剂和灭火方法,避免实施无效扑救或造成“火上浇油”的后果。
⑤当爆炸物品着火或火场上有爆炸物品时,要及时疏散并冷却爆炸物品。疏散时要防止摔、掷、抛、拖、拉。对于燃烧的爆炸物品,可用水扑救,但应注意避免用强大水流冲击。
⑥火灾扑灭之后,参加灭火的人员应进行清洗,消除余毒,并进行必要的专项体检以减少后患。
10)应急响应的终止。在火灾、爆炸事故处理完全、受伤人员得到妥善救治后,经事故应急领导小组确定,即可终止应急状态。
11)善后处理工作
①应急响应终止后,事故应急领导小组人员必须做好事故过程、损失及其他相关情况的整理记录工作。
②事故现场调查完毕,即可对现场进行善后处理并恢复其正常状态。
③组织相关人员参加事故调查处理工作,认真总结经验教训,做好防范工作。
④对损坏的设备、设施进行维修,尽快恢复正常的生产工作。
3.解
仪器总电源线指示灯不亮故障的排除方案
(1)故障原因
1)仪器电源线路断路或接触不良。
2)仪器熔断器熔丝熔断。
3)电源输入线路中有断路处。
4)仪器中的电路系统有短路处,因而将熔断器熔丝熔断,或某点电压突然增高。
5)指示灯灯泡烧坏。
6)灯座接触不良。
(2)排除方法
1)将电源线接好,压紧插头插座,若仍接触不良,则应更换新电源线。
2)更换新熔断器熔丝。
3)卡紧熔断器使其接触良好。
4)用万用表检查,并用观察法寻找断路处,将其焊好。
5)短路现象产生的原因一般是元件损坏,应更换损坏的元件,或找到电压增高的原因进行排除。
6)更换指示灯灯泡。
7)改善灯座接触状态。
4.解
灵敏度低故障的排除方案
(1)故障原因
1)元素灯发射背景太大。
2)元素灯工作电流太大,原子的自蚀效应致使谱线变宽,灵敏度降低。
3)火焰温度选择不当,燃气与助燃气之比选择不当。
4)火焰高度选择不当。
5)雾化器调整不好,或因长期不用,喷嘴被盐或脏东西堵塞,使样品提升量减少,这是仪器灵敏度下降的主要原因。
6)撞击球与喷嘴的相对位置没有调好。
7)燃烧器与外光路不平行。
8)光谱通带选择不当。
9)波长选择不合适。
10)燃气不纯。
11)空白溶液被污染,造成火焰状态不好,使空白吸收干扰增大,灵敏度降低。
12)雾化筒和燃烧缝严重锈蚀,雾化样品变成水珠。
13)雾化筒内有油膜或因长期不用而生锈,筒内积水,废液流动不通畅。
14)样品与标准样品存放时间过长而变质,容器的吸附作用或化学反应的结果造成灵敏度降低。
15)火焰状态不好,摆动严重或呈锯齿形,使测定结果偏低。
16)燃气漏气或阀门开关不灵,造成工作条件改变。
17)气源不足。
(2)排除方法
1)选择与发射背景适合的元素灯作光源。
2)在发射光强度能满足需要的前提下使用尽可能低的工作电流,以提高仪器的灵敏度。
3)根据不同金属选择合适的助燃比。
4)合理选择火焰高度。
5)将助燃气体流量开到最大,用手指堵住喷嘴,使助燃气体吹到通畅为止。
6)调整撞击球与喷嘴相切,相对位置主要看喷雾质量如何。
7)使光轴通过火焰中心,不使燃烧缝与光轴有夹角。
8)根据不同元素选择适宜的光谱通带。
9)选择较灵敏的共振线作为分析线。
10)采取措施纯化燃气。
11)更换空白溶液。
12)更换雾化筒,除去燃烧缝的锈蚀。
13)用丙酮去锈,用乙醚-乙醇混合液清洗除油。
14)将容器清洗干净,重新配制样品和标准溶液。
15)清洗燃烧缝,改变助燃气,检查气路是否有水存在。
16)封堵漏气处,加润滑油使阀门开关自如。
17)加大气源压力。
5.解
噪声过大故障的排除方案
(1)故障原因
1)由于火焰的高度吸收,当测定远紫外区域的元素时,分析噪声可能较大。
2)空心阴极灯能量不足,伴随从火焰或溶液组分来的强发射,引起光电倍增管的高度噪声。
3)吸喷有机样品试剂时沾污了燃烧器。
4)灯电流、狭缝、乙炔气和助燃气流量的设置不当。
5)废液管状态不当,排液异常。
6)燃烧器缝隙被污染。
7)雾化器调整不当,雾滴过大。
8)乙炔钢瓶或空气压缩机输出压力不足。
9)检查空气过滤器,尤其当火焰中存在过量的钠发射时,不纯的乙炔也会有此类发射。
(2)排除方法
1)采用背景校正有时可有所改善。
2)在允许的最大电流值内,增大灯的工作电流,换用能量大的新灯,试用其他吸收线进行分析,用化学方法去除溶液中能通过火焰产生强发射的干扰组分。
3)清洗助燃器。
4)重新设置至合适。
5)更换排液管,重新设置水封。
6)清洗缝隙。
7)重新调整雾化器。
8)增加气源压力。
9)采取措施,纯化空气或乙炔气。
6.解
氢火焰已点燃,或用热导池检测器时进样不出峰
或灵敏度显著下降故障的排除方案
(1)故障原因
1)灵敏度过低。
2)进样口密封垫漏气。
3)柱前汽化室漏气或检测器管道接头漏气。
4)注射器漏气或被堵塞。
5)汽化室温度太低。
6)氢焰同轴电缆线断路。
7)收集极的位置过高或过低。
8)极化极负高压不正。
9)更换热导池钨丝时,接线不正确。
10)喷嘴漏气。
11)使用高沸点样品时,离子室温度太低。
(2)排除方法
1)提高灵敏度。
2)更换硅橡胶密封垫。
3)检漏并排除漏气处。
4)排除漏气处或疏通堵塞处。
5)提高汽化室温度。
6)更换同轴电缆线。
7)调整好收集极的位置。
8)调整极化电压。
9)重新接线,桥路中对角线的钨丝应在热导池的同一腔体内。
10)将喷嘴拧紧。
11)提高温度,防止样品在离子室管道中凝结,并提高氢气流量。
7.解
运行时记录仪衰减不呈线性故障的排除方案
(1)故障原因
1)接地不良。
2)“增益”调得太低,“阻尼”太大。
3)电气和机械零点不重合。
4)放大器部分的某些管子已坏。
5)“量程调节”偏离校准点太远。
(2)排除方法
1)使接地良好。
2)重调放大器增益可变电阻,并把“阻尼”调至适当。
3)将零点调至重合。
4)更换已损坏的管子。
5)对于有调节功能的仪器,可将“量程调节”调到校准点。
8.解仪器运行时检测器不加热故障的排除方案
(1)故障原因
1)主电源、柱恒温箱或程序控制器熔断器熔丝已坏。
2)加热器元件已断。
3)连接线脱落。
4)上限控制开关调得太低或有故障。
5)温度敏感元件有缺陷。
6)检测器恒温箱控制器中有的管子已坏。
(2)排除方法
1)更换损坏的熔断器熔丝。
2)更换加热元件。
3)焊好脱落的连接线。
4)调高上限控制开关,或用细砂纸磨光开关触点,然后用酒精清洗。
5)更换温度敏感元件。
6)检测出已损坏的管子,更换。
其余略。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







