金属结晶必须在一定的过冷条件下才能进行,这是由热力学条件决定的。热力学第二定律指出:在等温等压条件下,物质系统总是自发地从自由能较高的状态向自由能较低的状态转变。也就是说,结晶只有伴随着自由能降低的过程才能自发地进行。对于结晶过程而言,结晶能否发生,要看液相和固相的自由能谁高谁低。如果液相的自由能比固相的自由能低,那么金属将自发地从固相转变为液相,即金属发生熔化。如果液相的自由能高于固相的自由能,那么液相将自发地转变为固相,即金属发生结晶,从而使系统的自由能降低,处于更为稳定的状态。液相金属和固相金属的自由能之差,就是促使这种转变的驱动力。
恒压时,有以下热力学表达式:

熵的物理意义是表征系统中原子排列的混乱程度。温度升高,原子的活动能力提高,因而原子排列的混乱程度增加,即熵值增加,系统的自由能也就随着温度的升高而降低。图2.26是纯金属液、固两相自由能随温度变化的示意图。由图可见,液相和固相的自由能都随着温度的升高而降低。由于液态金属原子排列的混乱程度比固态金属大,即 SL>SS,也就是液相自由能曲线的斜率较固相大,所以液相自由能降低得更快些。既然两条曲线的斜率不同,那么两条曲线必然在某一温度相交,此时的液、固两相自由能相等,即 GL=GS,它表示两相可以同时共存,具有同样的稳定性,既不熔化,也不结晶,处于热力学平衡状态,这一温度就是理论结晶温度 Tm。从图中还可以看出,只有当温度低于 Tm时,固态金属的自由能才低于液态金属的自由能,液态金属才可以自发地转变为固态金属。如果温度高于 Tm,液态金属的自由能低于固态金属的自由能,此时不但液态金属不能转变为固态,相反固态金属还要熔化成液态。由此可见,液态金属要结晶,其结晶温度一定要低于理论结晶温度 Tm,此时固态金属的自由能低于液态金属的自由能,两相自由能之差构成了金属结晶的驱动力。(https://www.daowen.com)
要获得结晶过程所必需的驱动力,一定要使实际结晶温度低于理论结晶温度,这样才能满足结晶的热力学条件。过冷度越大,液、固两相自由能的差值越大,即结晶驱动力越大,结晶速度便越快。这就说明了金属结晶时为什么必须过冷的根本原因。
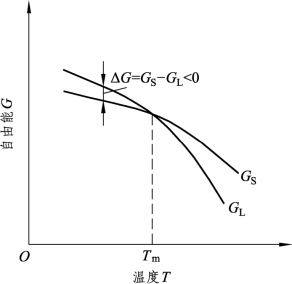
图2.26 液态金属和固态金属自由能随温度变化示意图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







