
细胞致突变试验分为体内试验(in vivo)和体外试验(in vitro)两大类,其中体内试验通常选择哺乳动物活体染毒,测试结束时,处死哺乳动物提取目标细胞检查测试终点。目标细胞可以是可遗传的生殖细胞(如精原细胞、精细胞、卵细胞等)或体细胞(如骨髓嗜多染红细胞)作为试验对象。体外试验的试验是指直接体外培养细胞,并对细胞直接染毒的实验方法,对象较为广泛,例如细菌、哺乳动物生殖细胞,或哺乳动物体细胞等,具体如表17-25所示。
表17-25 生殖细胞致突变性试验方法(www.daowen.com)
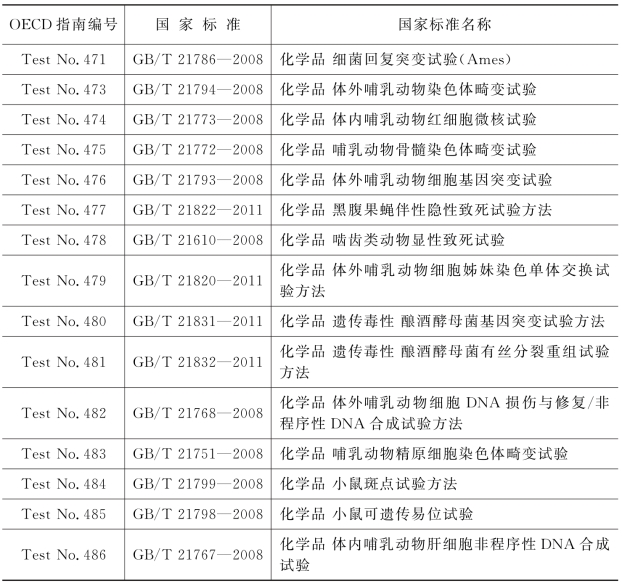
在对化学品进行生殖细胞致突变性分类时,可优先选择体外试验,例如Ames试验,体外哺乳动物细胞基因突变试验等。由于体外测试是直接对培养的细胞进行测试,为了模拟体内的代谢环境,通常在测试中还要加入代谢活化物(一般为氧化酶,最多使用的是小鼠肝脏的微粒体酶S9)用以模拟体内氧化代谢过程,防止测试物质的代谢产物致突变在体内阳性而在体外测试中带来的假阳性结果。需要注意的是来自非生殖细胞为试验对象的阳性结果需要结合专家经验,才可类推至生殖细胞。国际上对于化学品基因毒性和致突变性的评估通常是通过智选实验方案(ITS)进行的。方案一般首先选用体外测试,细胞包含原核生物细胞(471)和哺乳动物体细胞,终点要包含基因突变、染色体畸变和DNA损伤。在体外测试这些终点均为阴性时,一般不再要求后续进行体内测试。当体外测试中,哺乳动物体细胞任何测试结果为阳性时(基因突变、染色体畸变和DNA损伤),则继续做相应测试终点哺乳动物体细胞的体内测试,仍然为阳性时,继续做动物生殖细胞体内测试。这种测试方案可以显著减少测试动物的使用,并可以一步一步地深入鉴别哺乳动物的基因毒性的程度,为GHS分类提供数据支持。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








