地下水不是化学成分纯的H2O,而是含有多种化学元素的复杂溶液。天然条件下,赋存于岩石圈中的地下水,不断与岩土发生化学反应,并与大气圈、地表水圈和生物圈的水进行化学元素的交换,化学成分随空间及时间而演变。因此,地下水的化学成分,是在很长的时间内经过各种作用形成的。自然界中存在的元素,绝大多数已经在地下水中发现。
(1)地下水中主要离子成分
地下水中的主要离子成分有:
地下水中分布最广、含量较多的离子共7种,即氯离子(Cl-)、硫酸根离子(SO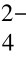 )、重碳酸根离子(HC
)、重碳酸根离子(HC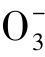 )、钠离子(Na+)、钾离子(K+)、钙离子(Ca2+)及镁离子(Mg2+)。构成这些离子的元素,有的是地壳中含量较高,且较易溶于水的,如O,Ca,Mg,Na,K等;有的是地壳中含量并不很大,但是溶解度相当大的,如Cl。某些元素(如Si,Fe等)虽然在地壳中含量很大,但由于其溶解于水的能力很弱,所以在地下水中的含量一般并不高。
)、钠离子(Na+)、钾离子(K+)、钙离子(Ca2+)及镁离子(Mg2+)。构成这些离子的元素,有的是地壳中含量较高,且较易溶于水的,如O,Ca,Mg,Na,K等;有的是地壳中含量并不很大,但是溶解度相当大的,如Cl。某些元素(如Si,Fe等)虽然在地壳中含量很大,但由于其溶解于水的能力很弱,所以在地下水中的含量一般并不高。
地下水中所含各种离子、分子与化合物的总量称为矿化度,以每升水中所含克数(g/L)表示。习惯上在105~110℃温度下将水样蒸干后所得的干涸残余物总量来表示矿化度(degree of mineralization)。也可以将分析所得阴阳离子含量相加,求得理论干涸残余物总量。由于在蒸干时有将近一半的HC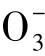 分解生成CO2及H2O而逸失。因此,阴阳离子相加时,HC
分解生成CO2及H2O而逸失。因此,阴阳离子相加时,HC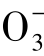 只取质量的一半。
只取质量的一半。
由于盐类在地下水中的溶解度不同,使得离子成分与地下水矿化度之间存在一定的规律。总体上看,氯盐的溶解度最大,硫酸盐次之,碳酸盐较小,钙的硫酸盐,特别是钙、镁的碳酸盐溶解度最小。随着矿化度增大,钙、镁的碳酸盐首先达到饱和并沉淀析出,矿化度继续增大时,钙的硫酸盐也饱和析出。因此,高矿化水中便以易溶的氯和钠占优势了。
(2)地下水中主要气体成分
地下水中常见的气体成分主要有O2,N2,CO2及H2S等。一般情况下,地下水中气体含量不高,每升水中只有几毫克到几十毫克。但是,气体成分能够很好地反映地球化学环境。同时,地下水中某些气体含量能够影响盐类在水中的溶解度以及其他化学反应。(www.daowen.com)
①氧气(O2)和氮气(N2) 地下水中的氧气和氮气主要来自大气层。它们随同大气降水及地表水补给地下水。地下水中溶解氧含量越高,越利于氧化作用,在较封闭的地球化学环境中,O2将耗尽而只残留N2。因此,N2的单独存在,通常可说明地下水起源于大气并处于还原环境。
②硫化氢(H2S) 地下水中出现硫化氢,其意义恰好与O2相反,说明处于缺氧的还原环境。地下水处在与大气较为隔绝的环境中,当有有机质存在时,由于微生物的作用,S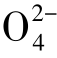 将还原生成H2S。因此,H2S一般出现于封闭地质构造的地下水中。
将还原生成H2S。因此,H2S一般出现于封闭地质构造的地下水中。
③二氧化碳(CO2) 地下水中的二氧化碳主要有两个来源。一种由植物根系的呼吸作用及有机质残骸的发酵作用形成。这种作用发生在大气、土壤及地表水中,生成的CO2随同水一起入渗补给地下水,浅部地下水中主要含有这种成因的CO2。另一种是深部变质形成的。含碳酸盐类的岩石,在深部高温影响下,会分解生成CO2,即
特别地,由于近代工业的发展,大气中人为产生的CO2有显著增加,尤其在某些集中的工业区,补给地下水的降水中CO2含量往往很高。
(3)地下水中的胶体成分与有机质
以碳、氢、氧为主的有机质,经常以胶体方式存在于地下水中。大量有机质的存在,有利于进行还原作用,从而使地下水化学成分发生变化。
地下水中还有未离解的化合物构成的胶体,其中分布最广的是Fe(OH)3,Al(OH)3及SiO2。这些都是很难以离子状态溶于水的化合物,但以胶体方式出现时,在地下水中的含量可以大大提高。例如,SiO2虽然极难溶解,但可以以胶体方式出现,在矿化度很低的水中往往占有不可忽视的比例。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







