(1)在腐蚀介质中工作的铸铁件,导致其易腐蚀的最普遍形式——电化学腐蚀的原因不可不究 在实际应用中,有些铸铁件是在腐蚀介质中工作的,对于这些铸件不仅要求具有一定的力学性能,而且必须考虑它们抵抗腐蚀的能力,以保证有较高的使用寿命。尤其石油、化工、化肥、冶金等工业的迅速发展,对成本较低廉、生产工艺较为简单的耐蚀铸铁的需要量已愈来愈多,要求也愈来愈高。因此,寻求减缓某些用于耐蚀工况的铸铁的腐蚀速度,甚至于防止其发生腐蚀,将具有相当重要的意义。
所谓腐蚀,主要是指金属在周围介质作用下发生化学及电化学作用而破坏的过程。金属腐蚀可分为四大类:化学腐蚀、电化学腐蚀、在机械因素作用下的腐蚀和生物腐蚀。几种腐蚀中,电化学腐蚀是金属最普遍的腐蚀形式,是金属在电解质(如湿空气、酸、碱、盐溶液)中,由于发生“原电池”作用而引起的破坏。比如,含有杂质的金属或多相合金放在电解质溶液中,由于金属和杂质具有不同的电极电位,这种电位差的存在就造成许多微小的“原电池”,电位高的金属或相形成阴极,电位低的金属或相形成阳极,两者之间的电位差就是“原电池”的电动势。结果,阳极金属溶解为离子形式进入电解质溶液,同时把当量的电子留在金属中:
[ne·Mn+e]→[Mn+e]+[ne-]
而从阳极迁移过来的电子被电解质溶液中能够吸收电子的物质D所接受:
[ne-]+[D]→[D·ne-]
结果阳极不断地被腐蚀侵蚀掉,而造成了电化学腐蚀。以铸铁为例,铸铁的金相组织中,各相的电位存在着很大的差异。在电解质中,石墨的电极电位最高(+0.37V),渗碳体次之,铁素体的电极电位最低(-0.44V)。所以铸铁在电解质溶液中,形成以石墨和渗碳体为阴极,铁素体为阳极的原电池,使铸铁不断地发生腐蚀。而且由于石墨的大量存在,还能使外界介质侵入铸铁内部造成晶间腐蚀。粗大的石墨还能形成大量的相互沟通的沟槽,使腐蚀剂沿石墨浸入铸件内部。所以铸铁中石墨和总碳含量越少,则耐蚀性也越高。石墨呈球状和絮状,其耐蚀性比片状石墨高。
从腐蚀过程最主要的两种腐蚀形式看,化学腐蚀,也就是金属由于与周围干燥气体或非电解质液体接触直接发生的化学反应所引起的破坏,其危害性较小,仅限于金属表层不深的地方,当形成一层保护膜之后,腐蚀速度就显著下降。电化学腐蚀则不同,它是逐层深入的,并能深入到金属内部。所以抵抗电化学腐蚀最为重要。
(2)不可忽视提高铸铁耐蚀性的主要途径 提高铸铁的耐腐蚀性主要靠加入合金元素,以得到有利的组织和形成良好的保护膜。铸铁的基体组织最好是致密均匀的单相组织,即奥氏体或铁素体,因为多相组织会形成较多的原电池,促成电化学腐蚀的进行。在其他条件相同时,珠光体不如铁素体基体耐蚀性好。碳的存在形式以碳化物状态最为有利,因为渗碳体与铁素体组成的原电池比石墨与铁素体组成的原电池电动势小。石墨的大小、数量有着相互矛盾的影响。就石墨本身来说,石墨在大部分腐蚀介质中呈惰性,铸铁的腐蚀主要通过金属基体进行,随腐蚀的进行,石墨在表面逐渐沉积积累,形成网络状石墨层,内含其他腐蚀残留物,粘附在其中,可起机械阻塞,增加电阻的作用,抑制层下金属的侵蚀。另一方面,因石墨是电极电位很高的阴极,加速基体的腐蚀。故石墨是既有利又有弊的组成相。石墨大小,数量对铸铁耐蚀性的影响,也有类似的规律。粗大石墨使原电池数量减少,对耐腐蚀有利,但粗大的石墨又使铸铁组织疏松,电解液易渗入内部,使腐蚀加剧。相反,细小石墨增加了原电池数量,增加腐蚀速率;但由于细小石墨的铸铁组织致密,电解液不易渗入,不利于腐蚀的进行。因此,石墨大小适中又互不相连贯的石墨对耐蚀性提高有利。至于石墨形态,球状优于蠕虫状,蠕虫状又优于片状。
加入合金元素,主要从以下三方面提高铸铁的耐蚀性:
1)改变某些相在腐蚀剂中的电位,降低原电池的电动势,使耐蚀性提高。如铬、钼、铜、镍、硅等元素能提高铸铁基体的电极电位。
2)改善铸铁组织,使基体组织,石墨大小、形状和分布得到改善,进而减少原电池数量,及减小电动势。例如,在铸铁中加入硅的质量分数w(Si)=14%~18%,可得到单相的铁素体基体和少量石墨,同时硅又提高了铁素体的电极电位,使耐蚀性显著提高。
3)在铸铁表皮层下形成一层致密、牢固的保护膜,如SiO2、Al2O3和Cr2O3膜,都具有很好的保护性。
(3)加入合金元素来提高铸铁基体的耐蚀性,其加入量未满足一定的要求时,效果不会明显 加入合金元素进入铸铁基体,形成均匀的固溶体时,要起到良好的耐腐蚀作用,必须达到一定的浓度。有关实验结果表明,当合金元素在基体中的原子份数比为1/8、2/8、3/8、…、11/8,即n/8时,可使铸铁的耐蚀性有显著提高,这就是通常所说的塔曼定律。若将原子百分数换算成质量分数,则如表3-72所示。
表3-72 铸铁中加入合金元素的需要量
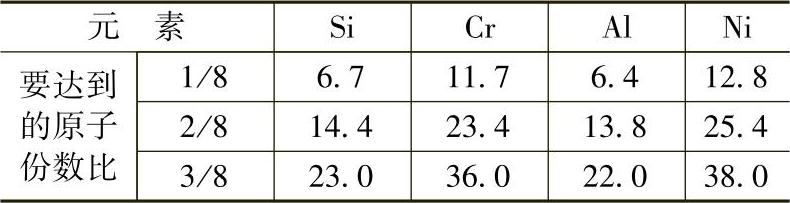
需要强调的是,只有固溶体中的实际含量达到表3-72中的数值时,才能显著提高铸铁的耐蚀性。比如铸铁中的铬含量达到11.7%,仍不能保证铸铁有良好的耐蚀性,因为铸铁中有一部分铬与碳结合为碳化物,使固溶体中实际铬的质量分数仍低于11.7%。因此,必须相应提高铸铁中总的铬含量,以保证在固溶体中的实际铬的质量分数大于11.7%。
(4)高硅耐蚀铸铁及其禁忌
1)高硅耐蚀铸铁中硅的质量分数不可太低,但也不宜太高 高硅铸铁是良好的耐酸铸铁,由于硅的大量加入,使铸铁的表面形成比较致密与完整的SiO2保护膜,这种膜具有很高的电阻率和较高的化学稳定性。铸铁表面的这种保护膜使铸铁在酸中处于钝化状态。当铸铁中硅的质量分数在14.5%以下时,耐蚀性较差;达到14.5%及以上时,在稀硫酸和盐酸中的耐蚀性均明显提高(见图3-52~53)。硅的质量分数大于18%时,铸铁耐蚀性不能进一步提高,但脆性大大增加,所以高硅铸铁的质量分数为w(Si)=14.5%~18.0%。
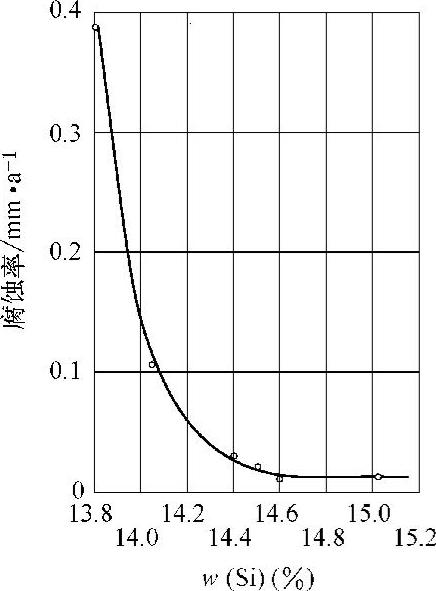
图3-52 高硅铸铁在质量分数为10%的H2SO4(80℃)中的腐蚀率与硅含量的关系
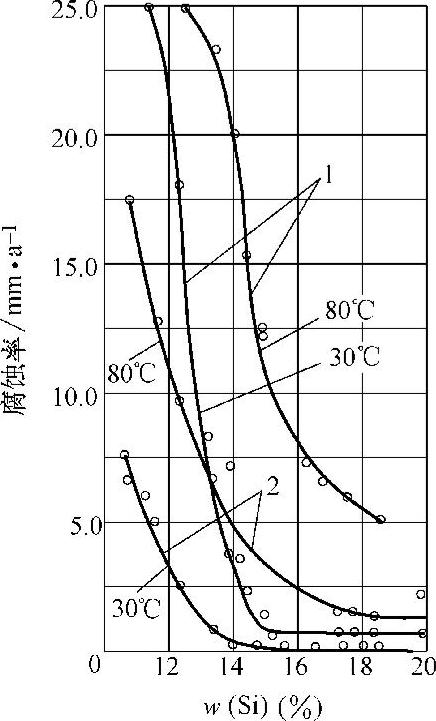
图3-53 硅含量对铸铁在盐酸溶液中腐蚀率的影响(试验时间:100h)
1—w(HCl)=35% 2—w(HCl)=10%
2)氢氟酸和碱液等不宜采用高硅耐蚀铸铁作容器或零件。高硅耐蚀铸铁对各种温度和质量分数的硝酸、硫酸及两者的混合酸都有很好的耐蚀性。在各种质量分数和温度的磷酸、醋酸和蚁酸、脂肪酸、乳酸等有机酸中,高硅耐蚀铸铁也都很耐蚀。但高硅耐蚀铸铁在氢氟酸、苛性碱、亚硫酸、氟化物、卤素等介质中是不耐蚀的。在碱和氢氟酸中,SiO2保护膜与介质之间发生下列反应:
SiO2+2NaOH=Na2SiO3+H2O
SiO2+4HF=SiF4↑+2H2O
使高硅耐蚀铸铁表面的SiO2保护膜被破坏,金属基体受到腐蚀,因此,不宜将这种耐蚀铸铁制成的工件用于氢氟酸、苛性碱等这类工况。
(5)高铬耐蚀铸铁及其禁忌
1)高铬耐蚀铸铁的铬含量不宜太低。高铬耐蚀铸铁中由于加入了相当多的铬,不仅会在铸件表面形成一层致密的Cr2O3保护层,同时其金相显微组织,是合金基体加分布较均匀的碳化物,而合金化基体可以是铁素体、奥氏体或铁素体加奥氏体混合基体。一般说来,不含稳定奥氏体合金元素(Ni、Cu、N)或含量很少的高铬耐蚀铸铁,当碳含量较低(w(C)<1.3%)时,易得到铁素体基体;反之,当碳含量较高,或含一定量奥氏体稳定化合金元素时,基体易得到奥氏体,或奥氏体加铁素体混合基体。而基体本身耐蚀性的提高主要取决于其铬含量。高铬耐蚀铸铁在20℃饱和盐水中的动腐蚀试验表明,基体铬的质量分数超过12.5%时,才具有较好的耐蚀性(见图3-54),从图中曲线知,其腐蚀率下降很缓;铬的质量分数低于12.5%时,随铬量增加,腐蚀率迅速降低。因此,要使高铬铸铁有好的耐蚀性,其基体中的铬含量不可低。另外,高铬耐蚀铸铁中的铬除固溶于基体中外,同时有很大一部分铬存在于碳化物中,为保证这种铸铁具有高的耐蚀性,其铬含量还应满足以下条件
w(Cr)%≥10×w(Cr)%+12.5%
而碳的选择,应遵循图3-55的原则:铬量较低而碳量较高时,耐蚀性恶化;但当铬量为30%时,1.5%以下的碳均能显示出好的耐蚀性。因为铬的质量分数较高时,形成的(Cr,Fe)23C6型碳化物与基体电位大致相同;如果铬含量较低,而出现(Cr,Fe)7C3型碳化物时,基体电位较低,由于原电池作用,促进了腐蚀的进行;另一方面,当铸铁总铬含量增加时,其基体铬含量也会相应增加,从而提高了基体的电位,耐蚀性增强。因此,在耐蚀环境应用的高铬耐蚀铸铁的铬的质量分数通常都不低,大都在w(Cr)=26%~36%。
如果希望适量降低铬的质量分数,又要求该铸铁有好的耐蚀性,通常大都加入钼、镍和铜来增加耐蚀性,特别是在酸性介质中的耐蚀性。但随镍和铜加入量增加,铸铁基体由铁素体变为奥氏体,耐相间腐蚀(与晶间腐蚀一致)性能下降,这是由于碳化物附近的奥氏体基体中铬的扩散速度慢,从而出现贫铬所引起的。(https://www.daowen.com)
2)不可忽视高铬耐蚀铸铁的适用性。高铬耐蚀铸铁对氧化性酸(尤其是硝酸)有良好的耐蚀性。它也可用于氧化态下的弱酸、许多盐溶液、有机酸溶液和一般的大气暴露条件下。
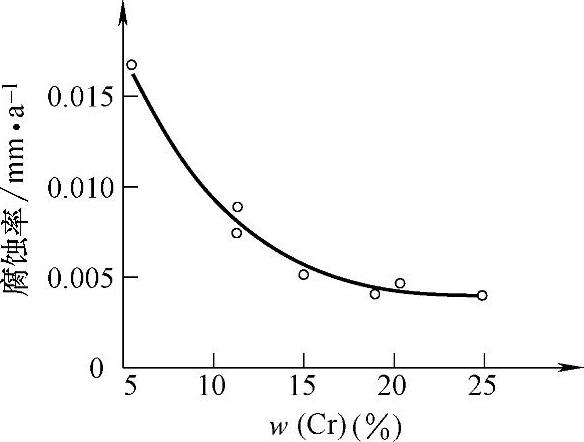
图3-54 高铬铸铁在20℃饱和食盐水中的腐蚀率与基体固溶铬量的关系
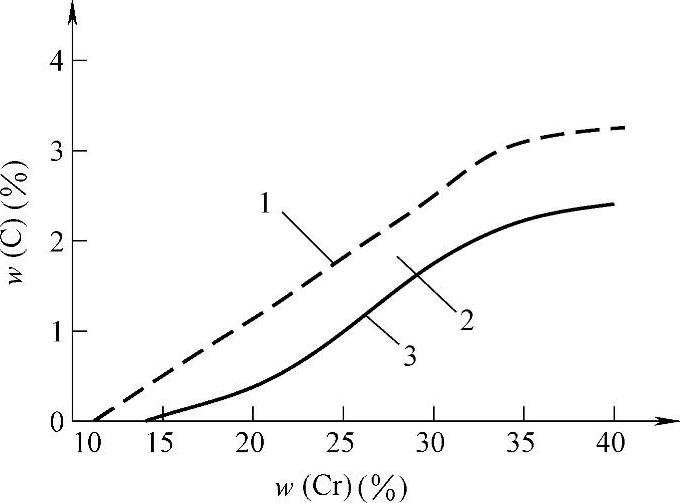
图3-55 碳、铬含量对铸铁氧化性能的影响
1—不抗氧化 2—部分抗氧化 3—完全抗氧化
高铬耐蚀铸铁对硝酸的耐蚀性极好,在室温下,耐质量分数为95%以下的各种浓度的硝酸腐蚀;对于质量分数小于70%的硝酸,在沸点以下的所有温度条件下,其腐蚀率小于0.127mm/a。在处理硝酸方面,高铬耐蚀铸铁和高硅耐蚀铸铁是互相补充的,因为高铬耐蚀铸铁除了沸腾的浓硝酸外,它能耐所有含量和温度的硝酸,而高硅耐蚀铸铁对热浓硝酸耐蚀性良好。
高铬耐蚀铸铁对79℃以下全含量亚硫酸、造纸工业中的亚硫酸盐废液、室温下的次氯酸漂白液、质量分数为5%以下的冷硫酸铝以及中性的或某些水解后产生酸性的盐类水溶液都是耐蚀的。它也可用于磷酸、硫酸铵、尿素、碳酸氢铵、温度不高的氢氧化钠和氢氧化钾等介质中。高铬耐蚀铸铁不能用于盐酸、氢氟酸、稀硫酸等还原性介质中。
高铬耐蚀铸铁也有很好的抗磨性,因此一些既需要承受苛刻电化学腐蚀,又受到悬浮着的某些固体颗粒强烈磨损的设备,如泵、阀、旋塞、管道、旋流器等均可选用高铬耐蚀铸铁铸造。生产实践证明,效果好,使用寿命较长。
(6)高镍奥氏体耐蚀铸铁及其禁忌
1)为使高镍奥氏体耐蚀铸铁有好的耐蚀性,其镍含量不可太少。高镍奥氏体耐蚀铸铁也称奥氏体耐蚀铸铁,是以镍为主要合金元素的高合金铸铁,其基体组织为奥氏体。在国外这种铸铁的商业名称是“Ni-Resist”,早在20世纪30年代就开始用于工业,50年代末、60年代初工业发达国家相继建立了奥氏体铸铁国家标准。目前我国尚没有奥氏体铸铁国家标准。
奥氏体耐蚀铸铁中镍含量越高,耐蚀性越好。图3-56所示是镍含量与铸铁在烧碱中的腐蚀率的关系。无论是电解法碱还是苛化法碱中,随镍含量的增加,铸铁腐蚀率降低。苛化碱中,镍质量分数在20%以上的铸铁,就有很好的耐蚀性。电解碱中含少量次氯酸钠等氧化性物质,增强了腐蚀反应的阴极过程,镍的质量分数达到30%时,铸铁才有很好的耐蚀性。镍质量分数为13.5%~36.0%的铸铁是高镍奥氏体铸铁,按镍的质量分数为四个基本等级:Ni=15%、Ni=20%、Ni=30%和Ni=35%,它们在许多腐蚀环境中都有很好的耐蚀性,应用很广。
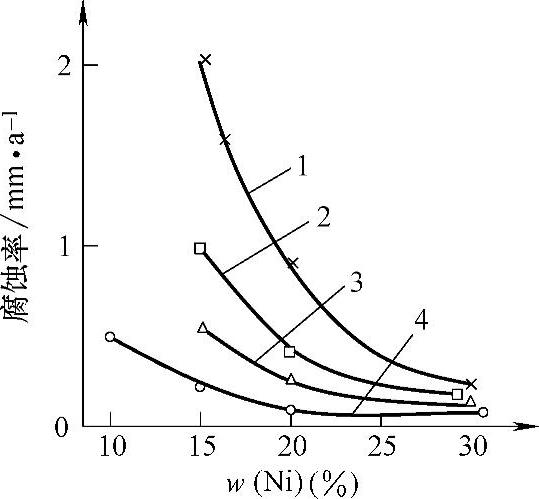
图3-56 铸铁在烧碱中的腐蚀率与镍含量的关系
介质条件:曲线1—150℃,电解法碱2—150℃,苛性碱3—120℃,电解法碱4—80℃,w苛性碱=50%
2)高镍奥氏体耐蚀铸铁中大都不可无铬。高镍奥氏体耐蚀铸铁中,常加入不同量的合金元素Cr、Cu、Mn、Si、Mo、Nb等来形成不同的牌号,以适应不同的腐蚀介质和使用条件。大部分牌号奥氏体耐蚀铸铁中加有铬。加铬可以提高奥氏体耐蚀铸铁的强度和硬度,同时改善耐腐蚀性和耐热性能。奥氏体耐蚀铸铁中铬的质量分数从2%增加到3%,其抗冲蚀性能大大提高。铬的质量分数为5%的奥氏体耐蚀铸铁具有优良的抗固液两相流磨损腐蚀的性能,而且镍、铬含量越高,抗磨蚀性能越好。在含泥沙的海水和含固体盐颗粒的盐水中,含铬的奥氏体耐蚀球墨铸铁抗磨蚀性能优于铜合金和普通不锈钢。
3)高镍奥氏体耐蚀铸铁有良好的耐蚀性,不可忽视其适宜使用的工况。奥氏体耐蚀铸铁在海水、盐卤、海洋大气、烧碱、石油、硫及硫化物、常温还原性稀酸、许多有机酸及高温氧化等腐蚀条件下,都有很好的耐蚀性。在海水淡化、发电、化工、石油、食品、造纸、污水处理及汽车、船舶等许多工业部门都有广泛的应用。
①海水和污水。奥氏体耐蚀铸铁对海洋大气、海水和中性盐类水溶液很耐蚀。在海水中奥氏体耐蚀铸铁的耐腐蚀率显著优于普通铸铁、碳钢及常用不锈钢,与铜合金相当。抗缝隙腐蚀和孔蚀的能力比不锈钢好,这是奥氏体耐蚀铸铁的最大特点。各种含量的氯化钠和氯化钙、氢化钡、氯化锌等氯化物,以及溴化钠等,其腐蚀特性与海水类似,奥氏体耐蚀铸铁在这类介质中都有很好的耐蚀性。沿海油田、化工厂等使用的地下水往往含有较多的氯离子,以及工业生活污水等,这些水对普通铸铁和碳钢的腐蚀严重,但使用奥氏体耐蚀铸铁可获得良好的应用效果。我国奥氏体铸铁件应用实践表明,在海水类氯离子腐蚀场合,用奥氏体耐蚀铸铁制造的泵、阀类设备使用效果很好。奥氏体耐蚀球墨铸铁泵叶轮在海水中的实际年腐蚀率为0.21mm/a,而同种条件下使用的铸铁叶轮和铜合金叶轮腐蚀率分别是8mm/a和1.1mm/a。
②碱溶液。在碱性介质中奥氏体耐蚀铸铁的耐蚀性极为优越。从在不同条件碱液中,用不同材料得到的腐蚀率看:在电解法烧碱中,Ni30型奥氏体耐蚀铸铁耐蚀性是1Cr18Ni9Ti不锈钢的8~20倍;在苛性碱中,两者腐蚀性差别更大。温度越高,奥氏体耐蚀铸铁相对不锈钢的耐碱腐蚀性能越优。Ni30型奥氏体耐蚀铸铁可适用于各种含量和温度的碱液。碱厂的使用经验表明,Ni30型奥氏体耐蚀铸铁泵、阀件的使用寿命,比1Cr18Ni9Ti不锈钢件成倍增加。
在高温熔融碱中,奥氏体耐蚀铸铁件可能产生应力腐蚀开裂现象,例如大型碱锅的出锅泵。奥氏体耐蚀球墨铸铁碱脆倾向低于奥氏体耐蚀灰铸铁。消除铸造应力可降低碱脆倾向。
③石油和硫化氢。奥氏体耐蚀铸铁在硫化氢腐蚀环境中,表面能生成硫化物保护膜,阻止金属基体被进一步腐蚀。石油工业中的腐蚀主要是硫化氢的腐蚀,石油含硫高,腐蚀性大。奥氏体耐蚀铸铁有良好的耐硫化氢腐蚀性能,因此在石油工业中获得广泛的应用。
④酸溶液。在无机酸中,奥氏体耐蚀铸铁可用于室温、质量分数为5%以下的脱气盐酸;5O℃以下的、质量分数不超过10%和质量分数大于80%的脱气的硫酸(见图3-57)中。在硝酸中,奥氏体耐蚀铸铁腐蚀率很高,在磷酸中的耐蚀性也不好。在许多有机酸中,例如醋酸、脂肪酸、甲酸、草酸、乙二酸和油酸,奥氏体耐蚀铸铁耐蚀性相当好。在氟硅酸、铬酸和柠檬酸中,奥氏体耐蚀铸铁也有较好的耐蚀性。
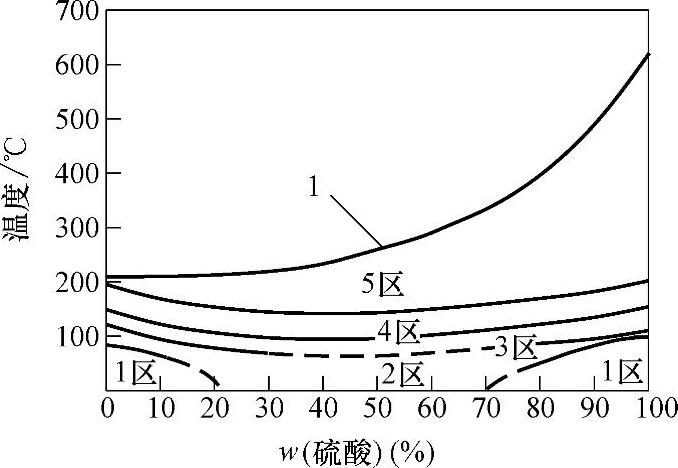
图3-57Ni15型奥氏体耐蚀铸铁在脱气硫酸中的等蚀曲线
1—沸点曲线
腐蚀率:1区:<0.125mm/a
2区:0.125~0.5mm/a
3区:0.5~1.25mm/a
4区:1.25~5mm/a
5区:>5mm/a
⑤其他介质。奥氏体耐蚀铸铁在造纸、化肥、食品等工业的大多数介质中,都有很好的耐蚀性。在熔融锌中,奥氏体耐蚀铸铁的浸蚀速度是普通铸铁的1/7。在低温和高温热腐蚀条件下,奥氏体耐蚀铸铁也有很好的使用性能。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







