高镍三元材料具有能量密度高,电化学性能稳定的优点。目前商业应用的主要高镍三元材料是523型和622型三元材料。近些年来,由于高镍三元NCM811和NCA材料单体的能量密度很高,可达300 Wh·kg-1以上,且这两种材料比容量高、钴含量低、成本低廉,所以开始被越来越多的人研究,成为主要的研发对象,呈现逐步替代磷酸铁锂和普通三元正极材料的趋势。
高镍正极材料商业化最重要的方面是电化学性能和热稳定性,许多研究团队也在朝着提高电化学性能和热稳定性的方向努力研究。尽管各种改性方法可以显著提高高镍材料的电化学性能,但大多数研究小组报道的高镍正极材料的改性方案都是在低电极密度(<3.0 g·cm-3)和低负载水平(<8 mg·cm-2)下进行的,这会导致学术研究与高镍正极材料的实际应用之间存在巨大差距,在工业电极条件下实现商业化的可行性较小。因此,弄清楚在工业电极条件下高镍三元正极材料的局限性是非常重要的。
实现商业化需要考虑材料的长期循环稳定性,提高结构和循环稳定性也是当前研发的一个热点。然而,由于形态坍塌和相变的产生,循环性能在很大程度上取决于电极密度。但当电极密度大于3.3 g·cm-3(商业化的镍基阴极的可用电极密度约为3.4 g·cm-3)时,高镍电极在前期表现出剧烈的容量衰减,限制了高镍正极材料的发展。因此许多科研人员将目光对准了单晶正极材料。单晶材料长期循环稳定性好、安全性高,在连续的电化学循环中,抑制单晶正极中的微裂纹演变可以减轻气体逸出,防止与电解质的副反应发生。此外,每个一次颗粒之间均不存在空隙空间,单晶正极材料可以具有相对小的表面积,这减少了高温储存期间的气体逸出。然而,目前的合成方法在加工时间、粉末密度等方面无法满足商业可行性的要求,还需要进一步研究。
据报道,在完全充电(4.45 V)和高温储存(85 ℃)的状态下,单晶NCM811正极材料(LiNi0.8Co0.1Mn0.1O2)比商业LiNi0.5Co0.2Mn0.3O2正极材料逸出的气体少[71]。多晶正极材料的表面积约为0.64 m2·g-1,而单晶正极的表面积较小,约为0.47 m2·g-1。由于抑制了与电解质的副反应,单晶正极材料在充电状态和85 ℃下储存10天后,显示出比商业常用的三元正极材料更低的气体释放量。
Li及其同事[72]发现单晶材料LiNi0.5Mn0.3Co0.2O2(SC-532)的电解质稳定性优于氧化铝涂层的多晶材料LiNi0.5Mn0.3Co0.2O2(AC-532)。他们将电池充电至4.4 V,4.5 V和4.6 V并保持100 h,然后测量了在较恶劣条件下的气体释放量,发现AC-532电池随着充电电压的增加产生更多的气态产物。通常无论电池电压为多少,单晶材料SC-532都只产生极少量的气体,这些气体可以忽略不计,这意味着单晶正极材料对氧化电解质具有高度耐受性。所以单晶材料的特性可以解决普通正极材料的气体逸出、长期循环和热稳定性差的问题,有很好的发展前景。
此外,Liu等[73]制备了一种新型的微混合器以辅助共沉淀法,不仅可以提高高镍正极材料的循环稳定性,还能缩短反应时间,将反应时间从12 h减少到数秒。微结构反应器可以提供均匀环境和产生优异的可控尺寸及形态,帮助颗粒在生长和结晶过程中沉淀。在该项研究中,他们将微混合器与微滤膜结合,合成了一系列高镍正极材料前驱体NixCoyMn1-x-y(OH)2。微混合器有助于混合过渡金属盐溶液和碱液的均相共沉淀反应,微滤膜可以分散介质以加速混合过程,有助于反应物的微混合,并提供均匀的环境。他们还研究了膜孔径对高镍正极材料的电化学性能的影响,以筛选出合适的微混合器,见表2-3。
表2-3 通过ICP-AES测定的LiNi0.8Co0.1Mn0.1O2正极材料的元素组成[73]
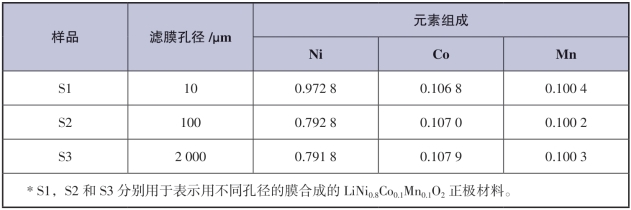
他们将高镍正极材料在25 ℃,0.2 C倍率,2.75~4.3 V电压下充、放电,以评价S1,S2和S3样品的电化学性质。结果发现S1的初始放电比容量为188.5 mAh·g-1,高于S2(178.0 mAh·g-1)和S3(175.7 mAh·g-1)。在50次循环后,S1仍然能够提供179.9 mAh·g-1的高放电比容量和95.4%的容量保持率,均高于S2(94.3%)和S3(93.3%)。为了探究不同微混合器对容量保持率的影响,将三个样品在1.75~4.3 V,1 C下充、放电循环100次。在100次循环后,S1,S2和S3的放电比容量分别为149.9 mAh·g-1,138.5 mAh·g-1和135.5 mAh·g-1,分别对应82.2%,77.2%和75.4%的容量保持率。可以看出,S1的电化学性能最为优异,这可能是由于其较低的Li+/Ni2+阳离子混排,阻碍了Li+转移;另一方面,具有更多空隙的S2和S3倾向于暴露更多的电极/电解质界面,使得电解质侵蚀更为严重。这些结果意味着微混合器合成方法为具有优异循环稳定性的高镍正极材料的快速合成提出了新的方向。
另外,通过对高镍三元正极材料进行表面改性和合成浓度梯度材料,在温和电极条件和半电池水平测试下显著提高了其电化学性能。但是这些方法面临同一个问题:忽略了工业电极的制造条件,不适合大规模合成。且大多数单晶正极材料不能达到多晶正极材料所提供的可逆容量。但是相信随着研发水平的提升,在未来,具有单晶特性的高镍正极材料可以成为高能量和安全的下一代锂离子电池[74]。
高镍三元正极材料对生产工艺要求严格,其对应的生产工艺要求大幅提高,体现在智能化和低能耗等方面。为满足动力电池对三元材料高性能、低成本的要求,生产设备将逐渐向智能化、大产能、低能耗、环境友好的方向发展。高镍三元材料的生产工艺较为复杂。由于高镍三元材料的结构稳定性相对较低,且生产组装时不能接触空气,因此需要全自动化生产线。高镍三元材料的生产线对环境要求更高,原有NCM523与NCM622生产线不能通过技术改造升级来生产高镍三元材料,而需要重新设计和新建生产线。
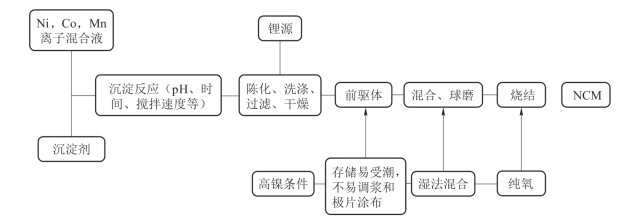
共沉淀法(图2-29)是用于工业制备高镍NCM正极材料前驱体的最常用的方法,优化生产工艺参数必不可少。该方法是在由N2惰性气氛保护的CSTR中加入过渡金属元素(TM)盐,同时用NaOH和NH4OH溶液调节pH,该过程由计算机精确监测。高镍NCM材料有一些缺点,如对空气和湿度的耐受性低、颗粒形态不规则、可循环性差等,为了克服这些缺点,Ren等[75]研究了高镍三元材料合成参数的影响,包括pH、搅拌速度和煅烧温度对LiNi0.6Mn0.2Co0.2O2(NCM622)正极材料的结构性质、颗粒形态和电化学性能等影响。结果表明,pH为10.8时,晶体生长和核形成两个过程可以达到平衡;搅拌速度对是否能形成规则球形颗粒有一定的影响,他们发现颗粒在低搅拌速度(600 r/min)下呈现出不规则和松散的聚集,而随着搅拌速度的增加会形成致密堆积的球形颗粒。但是过高的搅拌速度(>1 200 r·min-1)会破坏颗粒的物理完整性,严重的会导致颗粒破裂或变形。该小组认为,在共沉淀合成高镍NCM正极材料前驱体的过程中最佳搅拌速度为1 000 r·min-1;通过X射线粉末衍射(XRD)比较晶体结构研究煅烧温度,I(003)/I(104)的强度比随着温度的增加(从780 ℃升至860 ℃)而增加,这代表着阳离子混排减少。然而,当温度继续升高至900℃时,该比值较低,这可能与少量锂的蒸发和煅烧过程中部分Ni2+取代Li+位点有关[76]。在860 ℃下煅烧的样品放电比容量最高(温度为0.5 ℃,截止电压为4.45 V时,放电比容量为205 mAh·g-1),容量保持率最佳(100次循环后容量保持率为89.9%)。
 (https://www.daowen.com)
(https://www.daowen.com)
图2-29 NCM系列产品的共沉淀法制备过程
为了让Ni2+更好地氧化成为Ni3+,往往需要通纯氧来辅助,这样使得成本大大提高,Vu等[77]引入了过氧化技术来氧化NCM811中的Ni2+,该技术用KMnO4来处理材料的前驱体,并在空气气氛中煅烧处理过的前驱体对材料进行优化。为了比较过氧化作用,未处理的前驱体在纯氧气氛中烧结。XPS分析显示,用KMnO4处理前驱体煅烧后的NCM811材料,Ni离子的价态比其他前驱体更高,即拥有更多的Ni3+,阳离子混排度最低。经过KMnO4处理的NCM811材料,在截止电压分别为4.3 V和4.5 V下表现出比在空气中煅烧的原始NCM材料更好的倍率性能、更高的容量和循环稳定性。
Zhang等[78]采用Mn(NO3)2预氧化工艺合成了高镍正极材料,该方法有助于在空气气氛下合成高性能的高镍正极材料,是一种进一步提高高镍正极材料循环稳定性的新方法,该方法经济有效并且可以更好地抑制阳离子混排,具有巨大的工业化潜力。LiNi0.8Co0.1Mn0.1O2的预氧化过程如图2-30所示。在预氧化过程中,大量Ni2+被氧化成Ni3+,减少了煅烧过程中Li+/Ni2+阳离子混排。将质量分数为3%的Mn(NO3)2处理过的LiNi0.8Co0.1Mn0.1O2材料命名为NCM-N,再选择相同质量分数的非氧化性Mn(CH3COO)2代替Mn(NO3)2处理Ni0.8Co0.1Mn0.1(OH)2前驱体而制备的正极材料命名为NCM-AC。
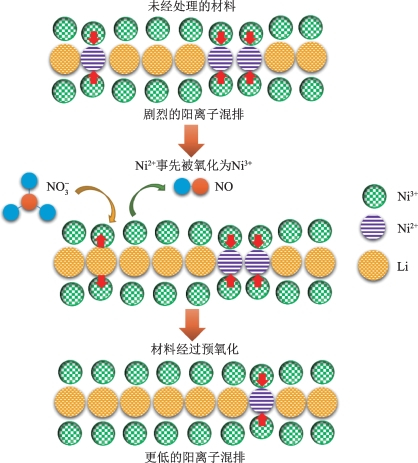
图2-30 用Mn(NO3)2对NCM材料进行预氧化处理的示意图[78]
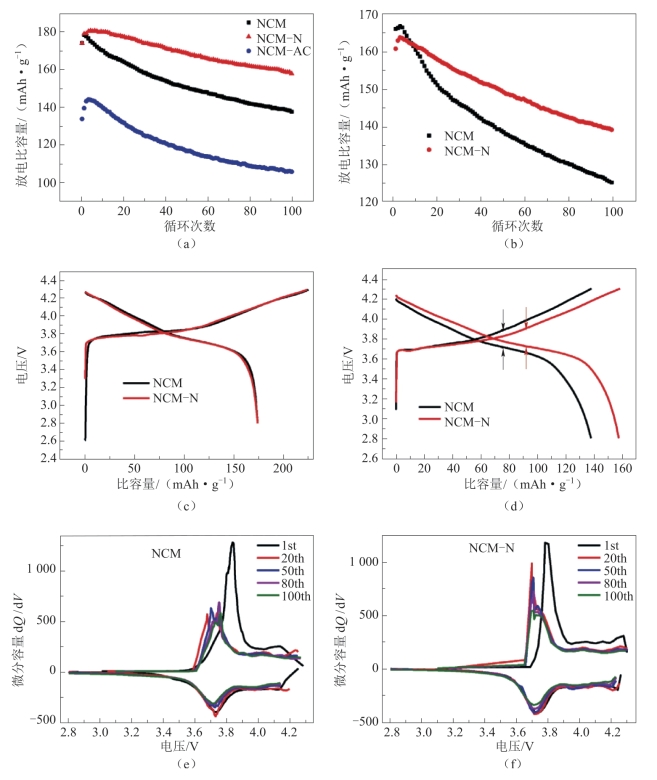
图2-31 (a)NCM,NCM-N和NCM-AC在0.2 C和2.8~4.3 V电压下的循环特性;(b)NCM和NCM-N在2 C和2.8~4.3 V电压下的循环特性;(c)第1次循环后,NCM和NCM-N在0.2 C的充、放电曲线;(d)第100次循环后,NCM和NCM-N在0.2 C的充、放电曲线;(e)原始 NCM的长循环期间的dQ/dV曲线;(f)NCM-N的长循环期间的dQ/dV曲线[78]
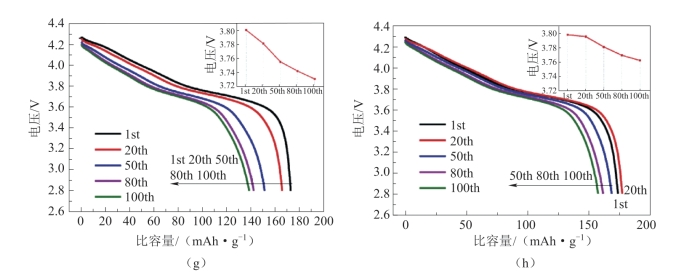
图2-31 (g)NCM在第1,20,50,80和100次循环,2.8~4.3 V电压,0.2 C下的放电曲线;(h)NCM-N在第1、20、50、80和100次循环,2.8~4.3 V电压,0.2 C下的放电曲线(续)[78]
他们测试了NCM,NCM-N和NCM-AC三种材料在2.8~4.3 V范围内,25℃下的电化学性能,结果如图2-31所示。图2-31(a)显示了NCM,NCM-N和NCM-AC在0.2 C下循环100周的性能。与NCM相比,NCM-N在0.2 C时的初始放电比容量约175 mAh·g-1,而NCM-AC仅为133 mAh·g-1。NCM-AC比容量的急剧下降可能是由于锂镍混排的加重和Mn元素的过度扩散引起的。NCM-N在前五个循环中观察到活化过程,可能是由于电解质和电极之间接触不充分造成的。在激活之后,NCM-N显示出比NCM更好的循环性能。NCM-N的容量保持率为90.73%,而NCM在100次循环后容量保持率仅为79.04%,推断NCM-N的循环性能的增强归因于锂镍混排程度的降低。
图2-31(b)显示了NCM和NCM-N在2 C和2.8~4.3 V电压下的循环性能。NCM的初始比容量更高,为166.1 mAh·g-1,但是其容量衰减比NCM-N更快。经过100次循环后,NCM和NCM-N的剩余比容量分别为125.4 mAh·g-1和139.4 mAh·g-1。该结果证明了Mn(NO3)2处理后NCM-N材料的快速充电/放电性能得到增强。
图2-31(c)、(d)是NCM和NCM-N在第1次循环和第100次循环的充、放电曲线。两种样品的充、放电曲线类似,初始库仑效率接近,分别为77.3%和77.8%,这表明两者在初始阶段的电化学性质相同,但在100个循环后,NCM和NCM-N之间存在明显差异。图2-31(d)中的箭头清楚地表明了NCM和NCM-N材料的充、放电平台之间的间隙,NCM-N材料的较窄间隙预示着较小的极化过程。这可以用来解释NCM-N材料循环性能的改善。在图2-31(e)、(f)所示的dQ/dV图中,氧化还原峰的位置可以更清楚地表现出这种现象。与NCM-N的dQ/dV曲线相比,在NCM的dQ/dV曲线中观察到更大的极化程度。NCM-N中的氧化和还原峰没有显著变化,确保了其在长循环过程中的循环稳定性。图2-31(g)、(h)分别显示了NCM和NCM-N在0.2 C条件下,第1,20,50,80和100次循环的放电曲线。在图2-31(h)中,NCM-N材料在第20次循环时的比容量高于第一次循环的,这与前几周的活化过程有关,同时在放电曲线中可以观察到电压的下降。图2-31(g)、(h)中的插图显示了循环时在半点位放电电压的变化。与NCM相比,NCM-N材料的电压损失更少,仅为0.94%,电压损失得到一定程度的缓解,说明NCM的预氧化可以缓解锂镍混排。
总体而言,减少生产过程中的阳离子紊乱以及氧缺陷也非常重要,这将直接影响高镍正极材料的性能。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






