1.1.2.1 锂离子电池的组成
锂离子电池主要由正极、负极、隔膜、电解质(液)、外包装五部分组成。
电池正极是锂离子电池的重要组成部分,承担着参与化学反应和提供锂离子的重要作用。锂离子电池正极由活性物质、导电剂、黏合剂和集流体组成。其正极活性物质是控制电池容量的关键性因素。理想正极活性物质应具备如下性能:
(1)金属离子应具有较高的氧化还原电位,从而提高锂离子电池的输出电压;
(2)锂的含量尽可能大,确保有足够量的锂发生嵌入和脱嵌,提高容量;
(3)Li+在嵌入/脱嵌过程中高度可逆,并且材料的结构要具有一定的稳定性;
(5)具有良好的化学稳定性。
正极活性物质为满足上述要求,一般采用电势较高(相对金属锂电极电位一般大于3 V)并且在空气中能稳定嵌锂的过渡金属氧化物,如钴酸锂(LiCoO2)、镍酸锂(LiNiO2)、锰酸锂(LiMn2O4)等。正极集流体通常采用铝箔。
电池负极也是电池中参与电化学反应的重要组成部分,负极由活性物质、黏合剂和集流体组成。理想的负极应具备以下性能:
(1)锂在负极的活度要接近纯金属锂的活度,以使电池具有较高的开路电压;
(2)在充、放电过程中,电极材料主体结构稳定,确保良好的循环性;
(3)电化学当量低,可嵌入和脱嵌锂容量大,以获取尽可能大的比容量;
(4)锂在负极中的扩散系数足够大,可承受大电流充、放电;
(5)材料导电性好,锂离子在负极中的嵌入和脱嵌过程中,极化程度低;
(7)与电解质生成良好的固体电解质界面(Solid Electrolyte Interface,SEI)膜,在SEI膜形成后不与电解质等发生反应;
(8)成本低、易制备、无污染。
为尽可能满足上述要求,目前锂离子电池负极活性物质一般采用电位尽可能接近金属锂电势的可逆脱嵌锂材料,如石墨和中间相碳微球(Mesocarbon Microbeads,MCMB)等。负极集流体通常采用铜箔。
隔膜的主要作用是分隔正、负极,防止电子在电池内部传导引起短路,同时能够让锂离子通过。这要求隔膜满足以下基本要求:
(1)对于电子绝缘;
(2)可以高效传输离子;
(3)机械性能稳定,同时易于加工;
(4)化学性能稳定,不与电解液、电化学反应副产物发生化学反应;(www.daowen.com)
(5)能有效阻止两极之间颗粒、胶体或可溶物质的迁移;
(6)与电解液具有亲和性;
(7)安全环保。
如今广泛使用的隔膜材料一般为聚烯烃系树脂,如Celgard2400隔膜为PP/PE/PP三层微孔隔膜。
电解质(液)的作用是在电化学反应过程中在正、负极之间传输离子。由于锂离子电池负极电位与锂接近,比较活泼,在水溶液体系中不稳定,因此锂离子电池电解质(液)使用非水、非质子有机溶剂作为锂离子的载体,或采用固体电解质材料。对于最广泛使用的电解液而言,在理想状态下其应满足如下要求:
(1)在较宽的温度范围内为液体,一般希望范围为-40~70 ℃;
(2)锂离子电导率高,在较宽的温度范围内电导率在3×10-3~2×10-2 S·cm-1;
(3)具有良好的热稳定性,在较宽的温度范围内不发生分解反应;
(4)具有良好的化学稳定性,与电池内的正、负极材料、集流体、隔膜、黏合剂等不发生化学反应;
(5)电化学窗口较宽,可以在较宽的电压范围内保持稳定(稳定到4.5 V或更高);
(6)具有良好的成膜(SEI)特性,能在负极材料表面形成稳定钝化膜;
(7)对离子具有较好的溶剂化性能,能尽量促进电极可逆反应进行;
(8)无毒,蒸汽压低,使用安全,容易制备,成本低,无环境污染。
目前市场上的锂离子电池主要使用的是如LiPF6,LiClO4,LiBF4等锂盐的有机溶液。
锂离子电池外包装可采用金属外壳、铝塑软包装等。根据用途的不同可制作成圆柱形、棱柱形、扣式等形状,以满足便携式移动设备、航天飞行器、电动汽车、智能电网等不同领域的需求,如图1-3所示。
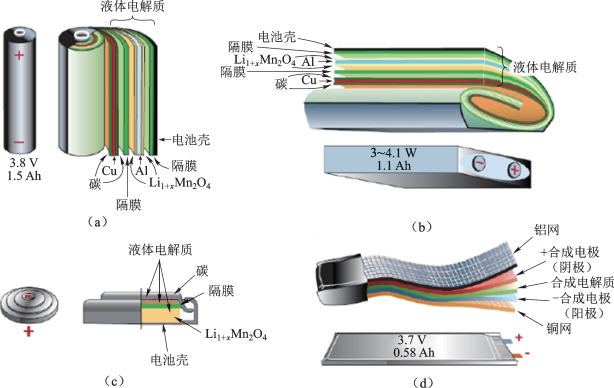
图1-3 几种常见的锂离子电池外形和构成的示意图[11]
1.1.2.2 锂离子电池的工作原理
锂离子电池实质是一种浓差电池,其充放电过程示意如图1-4所示。充电时,Li+从正极中脱出,经过电解质和隔膜嵌入负极层状材料中,正极处于贫锂状态,而负极处于富锂状态。同时电子通过外电路由正极流向负极使电荷得到补偿。放电时则相反,Li+从负极脱出,经电解质和隔膜嵌入正极,负极处于贫锂状态而正极处于富锂状态。电子经外电路由负极流向正极并对负载供电。充、放电时Li+嵌入和脱出的过程就像摇椅一样摇来摇去,故锂离子电池也被称作“摇椅电池”。
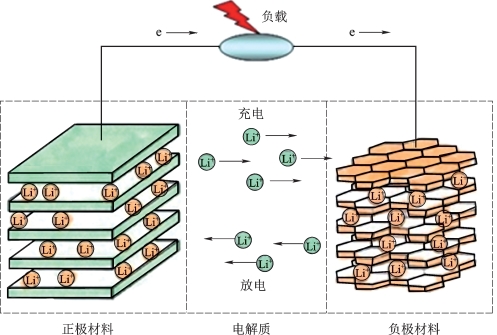
图1-4 锂离子电池充放电过程示意[11]
以常见的锂离子电池负极材料石墨和正极材料LiCoO2为例:充电时,锂离子从正极LiCoO2中脱嵌,释放一个电子,Co3+氧化成为Co4+,Li+进入电解液穿过隔膜嵌入负极石墨层间,负极得到一个电子生成LiC6;放电时,过程相反,负极碳材料中锂离子从层间脱出进入电解液,并释放一个电子,锂离子在电势作用下重新嵌入LiCoO2,使Co4+得到一个电子还原为Co3+。充、放电循环过程中,Li+分别在正、负极上发生“嵌入-脱出”反应,Li+便在正负极之间来回移动,其化学反应方程式如下:
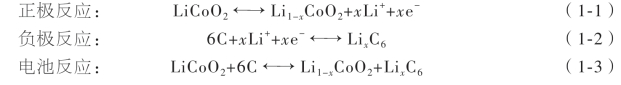
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






