迄今为止,总能系统的研究仍局限于物理能梯级利用范围(物理能的梯级利用大多所指稳流工质的热的梯级利用),不涉及化学反应过程中化学能的能量转换利用问题。很久以来,直接燃烧几乎成为能量转换的主要方式。但是,直接燃烧方式存在的诸多弊端(如燃烧品位损失大、易产生环境污染物等)与能源环境相容协调发展相悖。但传统的观点认为,燃烧过程的能损失是由燃烧的不可逆性造成的,因而是无法避免的。所以,长久以来,人们忽视了对减少燃烧过程能损失的研究,而将精力放在热力循环和热的梯级利用上。传统的化石能源动力系统中,借助燃烧技术,燃料化学能以热的形式释放出来,再由热力学循环实现热转功来输出有效功。
长期以来,热力循环的研究大多仅仅关注Carnot循环效率曲线下方,而热力系统中损失最大之处并非发生在物理能的传递与转换过程,而是发生在化学能转换物理能的燃烧过程。图3.5从能的品位的观点反映了燃烧过程燃料化学的利用。图中,纵坐标A表示能的品位,能的品位指能源所含有用成分的百分率。有用成分百分率越高,则品位越高。通常燃料化学能的品位都比较高,例如甲烷在燃烧时化学能品位A约为1.0。由于目前燃烧过程物理能的品位Ath可达到0.6~0.8,由此燃烧过程中燃料化学能与物理能之间存在较大的品位差(A1-Ath),这一现象是造成燃烧反应损失大的根本原因。为了减小燃料化学能与物理能之间的品位差,真正实质性的突破应着眼于有效降低燃料燃烧侧化学能的品位。为此,需要在能源动力系统中对传统的燃烧过程进行革新,采取新的能量释放方式,研究能量释放过程化学能品位梯级利用的机理。
新的能量释放方式首先与化学反应过程相结合,通过化学反应过程可实现品位A1到品位A3的燃料物质化学能的有效利用,当具有A3品位的燃料化学能通过燃烧转换为物理能时,由于燃料的化学能品位已在化学反应过程中从A1下降到A3,进而燃烧过程中化学能与物理能之间的品位差也由直接燃烧时的(A1-Ath)降低到(A3-Ath),从而减小燃烧过程能的损失。换言之,与传统的直接燃烧方式相比较,新的能量释放方式可以使燃料在燃烧前实现其化学能的有效利用。
图3.5 化学能与物理能综合梯级利用概念
2.化学能与物理能梯级利用原理
在能源动力系统中,物质化学能通过化学反应实现其能量转换。因此,物质能的转换势必与其发生化学反应的做功能力(Gibbs自由能变化ΔG)和物理能的最大做功能力(物理)紧密相关。
(1)物质、化学反应Gibbs自由能、物理关联性
根据热力学Gibbs自由能和的一般函数,对于一个化学反应的微分过程,其化学反应Gibbs自由能变化dG和变化dE可以表达为
式中,dH为过程的总能量变化(kJ/mol);TdS为过程中以热形式出现的能量(kJ/mol);dS为过程熵变化(kJ/K·mol);T为反应温度(K);T0为环境温度(K)。将式(3.18)代入式(3.19)中,得到(www.daowen.com)
式中,TdS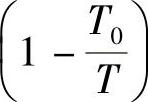 代表了过程中以热形式出现的热
代表了过程中以热形式出现的热 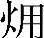 。热是物理
。热是物理 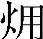 的一种表现形式。
的一种表现形式。 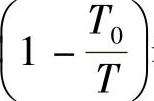 表示Carnot循环效率ηc,即
表示Carnot循环效率ηc,即 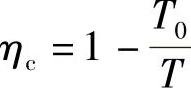 。由此,式(3.20)可以写为
。由此,式(3.20)可以写为
式(3.21)描述了物质 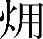 、化学反应Gibbs自由能和物理
、化学反应Gibbs自由能和物理 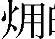 的普遍关系。对于物质能转换利用的体系,物质能的最大做功能力dE由两部分组成:一部分是化学反应的做功能力dG,另一部分是过程产生的热
的普遍关系。对于物质能转换利用的体系,物质能的最大做功能力dE由两部分组成:一部分是化学反应的做功能力dG,另一部分是过程产生的热 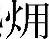 TdSηc。可见,物质能的最大做功能力的有效转换利用涉及与Gibbs自由能变化紧密联系的化学反应和与热利用相关的热力循环。值得注意的是,dG不再单纯是化学反应的推动力,而是更注重其在化学反应过程中对外的做功能力。
TdSηc。可见,物质能的最大做功能力的有效转换利用涉及与Gibbs自由能变化紧密联系的化学反应和与热利用相关的热力循环。值得注意的是,dG不再单纯是化学反应的推动力,而是更注重其在化学反应过程中对外的做功能力。
(2)物质能、化学反应Gibbs自由能和物理能的品位基本方程
能的品位是用来评价某种形式能量转换为有用功能力的大小。品位A的概念是日本石田教授在1982年提出的,随后得到了广泛的应用与发展。通常,热的品位用Carnot循环效率来表征。接下来将阐述对于如何表征化学反应Gibbs自由能的品位,并介绍在物质能转换利用过程中,物质能、化学反应Gibbs自由能和物理能三者之间品位的关联。
对于物质能转换利用过程,将式(3.21)两侧同时除以过程总焓变化dH,可以得到如下的无量纲化的表达式:
式中,等号左边项dE/dH表示物质能的品位A,等号右边第一项dG/dH表示了化学反应体系每单位能量总焓变化dH的Gibbs自由能变化的大小。定义dG/dH为无因次量B,则
B的物理意义表征了化学反应Gibbs自由能的品位。B与特定化学反应过程有关,对于同一物质,因不同的化学反应过程,其化学Gibbs自由能的品位B也不尽相同。式(3.22)等号右边第二项TdS/dH反映了过程中以热形式出现的能量占过程总焓值变化dH的份额,即令Z=TdS/dH;等号右边第二项Carnot循环效率ηc表征了热流TdS的品位。因此,式(3.22)可以改写为
从式(3.24)可以清楚地看出,物质能的品位A等于化学反应Gibbs自由能的品位B和反映物理能品位的Carnot循环效率ηc与Z的乘积之和。该式将物质能的转换利用以无量纲的形式表达,建立了物质能、化学反应Gibbs自由能和物理能的三者之间品位基本方程。式(3.24)与式(3.21)一样,对于任何物质能通过化学反应进行有效转换利用过程是普遍适用的。图3.6形象地表示了物质能的总品位A被分解为化学反应Gibbs自由能的品位B和Carnot循环效率ηc。
图3.6 物质能、化学反应Gibbs自由能、热能三者品位关系示意图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。





